Trắc nghiệm chương 1: Nguyên tử phần 2
Chuyên đề Hóa học lớp 10: Trắc nghiệm chương 1: Nguyên tử phần 1 được VnDoc sưu tầm và giới thiệu tới các bạn học sinh cùng quý thầy cô tham khảo. Nội dung tài liệu sẽ giúp các bạn học sinh học tốt môn Hóa học lớp 10 hiệu quả hơn. Mời các bạn tham khảo.
Bài tập trắc nghiệm chương 1
Bài 1: Nguyên tử gồm:
A. Các hạt electron và nơtron
B. Hạt nhân mang điện dương và lớp vỏ mang điện âm
C. Các hạt proton và nơtron
D. Các hạt proton và electron
Chọn đáp án: B.
Giải thích: Nguyên tử được cấu tạo bởi hai phần : Hạt nhân và lớp vỏ.
Bài 2: Trong nguyên tử, hạt không mang điện là:
A. Nơtron và Proton
B. Proton
C. Electron
D. Nơtron
Chọn đáp án: D.
Bài 3: Khối lượng nguyên tử tập trung hầu hết ở hạt nhân và được tính bằng
A. Tổng số hạt proton và tổng số hạt nơtron
B. Tổng khối lượng của proton, nơtron và electron có trong nguyên tử
C. Tổng khối lượng của các hạt nơtron và electron
D. Tổng khối lượng của proton và electron
Chọn đáp án: A
Giải thích: Do khối lượng của các eletron là không đáng kể so với khối lượng nguyên tử.
Bài 4: Mệnh đề nào sau đây sai:
A. Số proton bằng trị số điện tích hạt nhân
B. Số hiệu nguyên tử bằng trị số của điện tích hạt nhân nguyên tử
C. Số proton bằng số electron
D. Số proton bằng số nơtron
Chọn đáp án: D
Bài 5: Chọn đáp án đúng: Các hạt cấu tạo nên hạt nhân của hầu hết nguyên tử là:
A. Proton và nơtron
B. Electron và proton.
C. Electron , proton và nơtron.
D. Nơtron và electron
Chọn đáp án: A.
Giải thích: Hạt nhân của các nguyên tử đều được cấu tạo nên từ hai loại hạt: Proton và nơtron (trừ nguyên tử Hidro).
Bài 6: Ion có 18 electron và 16 proton mang điện tích là
A. 16+. B. 2−. C. 18−. D. 2+.
Chọn đáp án: B.
Bài 7: Tổng số hạt proton, nơtron và electron trong 1 nguyên tử nguyên tố X là 155, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 33 hạt. X là nguyên tố nào dưới đây?
A. Cu B. Ag C. Fe D. Al
Chọn đáp án: B
Giải thích:
Tổng số hạt proton, nơtron và electron trong 1 nguyên tử nguyên tố X là 155:
P + e + n = 155 hay 2p + n = 155 (do p = e) (1)
Số hạt mang điện (p và e) nhiều hơn số hạt không mang điện (n) là 33 hạt
(p+e) – n = 33 hay 2p – n = 33 (2)
Giải (1), (2) ta có p = e = 47
Bài 8: Kí hiệu nguyên tử biểu thị đầy đủ đặc trưng cho một nguyên tử của một nguyên tố hoá học vì nó cho biết
A. số khối A
B. số hiệu nguyên tử Z
C. nguyên tử khối của nguyên tử
D. số khối A và số hiệu nguyên tử Z
Chọn đáp án: D.
Bài 9: Tổng số hạt p, n, e trong nguyên tử ![]() là
là
A. 19. B. 28. C. 30. D. 32.
Chọn đáp án: B.
Giải thích:
Số hạt p = e = 9, số n = A-P = 19 – 9 = 10.
Tổng số hạt p + n + e = 28.
Bài 10: Phát biểu nào dưới đây không đúng?
A. Số khối bằng tổng số hạt proton và electron.
B. Số khối là số nguyên.
C. Số khối bằng tổng số hạt proton và nơtron.
D. Số khối kí hiệu là A.
Chọn đáp án: A.
Giải thích: Số khối bằng tổng số hạt proton và nơtron.
Bài 11: Một nguyên tố hoá học có thể có nhiều nguyên tử có khối lượng khác nhau vì lí do nào dưới đây?
A. Hạt nhân có cùng số nơtron nhưng khác nhau về số proton.
B. Hạt nhân có cùng số proton nhưng khác nhau về số nơtron.
C. Hạt nhân có cùng số nơtron nhưng khác nhau về số electron.
D. Hạt nhân có cùng số proton và số electron.
Chọn đáp án: B.
Giải thích: Sự khác nhau về số nơtron tạo ra các đồng vị của cùng một nguyên tố.
Bài 12: Phân lớp 3d có số electron tối đa là
A. 6. B. 18. C. 10. D. 14.
Chọn đáp án: C.
Giải thích: Số electron tối đa trên phân lớp s = 2, p =6, d = 10, f = 14.
Bài 13: Cho cấu hình electron nguyên tử các nguyên tố sau:
a) 1s22s1
b) 1s22s22p5
c) 1s22s22p63s23p1
d) 1s22s22p63s2
e) 1s22s22p63s23p4
Cấu hình của các nguyên tố phi kim là
A. a, b. B. b, c. C. c, d. D. b, e.
Chọn đáp án: D.
Giải thích:
Nguyên tố có 5, 6, 7 electron lớp ngoài cùng là phi kim.
a) 1e lớp ngoài cùng b) 7e lớp ngoài cùng c) 3e lớp ngoài cùng
d) 2e lớp ngoài cùng e) 6e lớp ngoài cùng
Bài 14: Các ion và nguyên tử: Ne, Na+, F− có điểm chung là
A. có cùng số khối.
B. có cùng số electron.
C. có cùng số proton.
D. có cùng số nơtron.
Chọn đáp án: B
Giải thích: Cấu hình electron của Ne, Na+, F- : 1s22s22p6
Bài 15: Có bao nhiêu electron trong ion ![]() ?
?
A. 21 B. 27 C. 24 D. 49
Chọn đáp án: A.
Giải thích: Crom có p = e = 24 hạt, Cr3+ có e = 21 (do Cr3+ đã nhường 3 e).
Bài 16: Các đồng vị của nguyên tố hóa học được phân biệt bởi yếu tố nào dưới đây?
A. Số nơtron.
B. Số electron hoá trị.
C. Số proton.
D. Số lớp electron.
Chọn đáp án: A.
Giải thích: Đồng vị là những nguyên tố hóa học có cùng số proton nhưng khác nhau về số nơtron.
Bài 17: Trong tự nhiên oxi có 3 đồng vị bền: ![]() còn cacbon có 2 đồng vị bền
còn cacbon có 2 đồng vị bền![]() .
.
Số lượng phân tử CO2 tạo thành từ các đồng vị trên là
A. 10. B. 12. C. 11. D. 13.
Chọn đáp án: B
Giải thích:
Với 12C lần lượt có
12C16O16O 12C17O17O
12C18O18O 12C16O17O
12C16O18O 12C17O18O
Tương tự với 13C cũng có 6 phân tử CO2 được lập thành.
Bài 18: Trong nguyên tử một nguyên tố A có tổng số các loại hạt là 58. Biết số hạt p ít hơn số hạt n là 1 hạt. Kí hiệu của A là
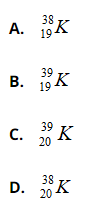
Chọn đáp án: B.
Giải thích:
Tổng số hạt proton, nơtron và electron trong 1 nguyên tử nguyên tố A là 58:
p + e + n = 58 hay 2p + n = 58 (do p = e) (1)
Số hạt p ít hơn số hạt n là 1 hạt:
n- p =1 (2)
Giải (1), (2) ta có p = e = 19, n = 20
Bài 19: Trên vỏ nguyên tử, các electron chuyển động xung quanh hạt nhân................
Hãy chọn cụm từ thích hợp đối với chỗ trống ở trên.
A. với vận tốc rất lớn trên những quỹ đạo xác định
B. với vận tốc rất lớn không theo quỹ đạo xác định
C. một cách tự do
D. với vận tốc rất lớn có quỹ đạo hình elip hay hình tròn
Chọn đáp án: B.
Giải thích: Các electron chuyển động xung quang hạt nhân với vận tốc lớn và không theo quỹ đạo xác định.
Bài 20: số hiệu nguyên tử của các nguyên tố cho biết
A. số electron hoá trị và số nơtron.
B. số proton trong hạt nhân và số nơtron.
C. số electron trong nguyên tử và số khối.
D. số electron và số proton trong nguyên tử.
Chọn đáp án: D
Giải thích: Số hiệu nguyên tử = số proton = số electron
Bài 21: Phát biểu nào sau đây là sai?
A. Tất cả hạt nhân nguyên tử được cấu tạo bởi 2 loại hạt là proton và nơtron
B. Trong nguyên tố số proton bằng số electron
C. Trong nguyên tử số proton luôn bằng số hiệu nguyên tử Z.
D. Khối lượng của nguyên tử tập trung chủ yếu ở khối lượng của hạt nhân nguyên tử
Chọn đáp án: A.
Giải thích: Hầu hết hạt nhân của các nguyên tử đều cấu tạo bởi proton và nơtron, trừ hạt nhân nguyên tử Hiđro.
Bài 22: Số proton, số electron, số notron trong ion ![]() lần lượt là:
lần lượt là:
A. 26, 26, 30
B. 26, 28, 30
C. 26, 28, 30
D. 26, 24, 30
Chọn đáp án: D.
Giải thích: Fe2+ có số p = 26, n = A – Z = 56 – 26 = 30.
E = 24.
Bài 23: Một nguyên tử X có số hiệu nguyên tử Z =19. Số lớp electron trong nguyên tử X là
A. 4 B. 5 C. 3 D. 6
Chọn đáp án: A.
Giải thích: Cấu hình e của X: 1s22s22p63s23p64s1
Bài 24: Cho hai nguyên tố M và N có số hiệu nguyên tử lần lượt là 11 và 13. Cấu hình electron của M và N lần lượt là
A. 1s22s22p7 và 1s22s22p63s2.
B. 1s22s22p63s1 và 1s22s22p63s23p1.
C. 1s22s22p63s1 và 1s22s22p63s2.
D. 1s22s22p63s1 và 1s22s22p63s3.
Chọn đáp án: B
Bài 25: Trong số các kí hiệu sau đây của obitan, kí hiệu nào là sai?
A. 2d B. 2p C. 3d D. 4f
Chọn đáp án: A.
Giải thích: Lớp L chỉ có các phân lớp 2s, 2p.
Bài 26: Phân lớp 3d có nhiều nhất là?
A. 14 e B. 10 e C. 18 e D. 6 e
Chọn đáp án: B.
Bài 27: Trong tự nhiên H có 3 đồng vị: 1H, 2H, 3H. Oxi có 3 đồng vị 16O, 17O, 18O. Hỏi có bao nhiêu loại phân tử H2O được tạo thành từ các loại đồng vị trên:
A. 3 B. 16 C. 18 D. 9
Chọn đáp án: C
Giải thích:
Với 16O lần lượt có các phân tử:
1H1H16O 2H2H16O 3H3H16O
1H2H16O 1H3H16O 2H3H16O
Tương tự với 17O, 18O lần lượt lập được 6 phân tử H2O với mỗi nguyên tử oxi
Bài 28: Nitơ trong thiên nhiên là hỗn hợp gồm hai đồng vị có % về số nguyên tử tương ứng 147N là (99,63%) và 157N (0,37%). Nguyên tử khối trung bình của nitơ là
A. 14,7 B. 14,0 C. 14,4 D. 13,7
Chọn đáp án: B
Giải thích: 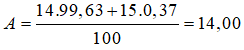
Bài 29: Cacbon có hai đồng vị, chúng khác nhau về:
A. Số hiệu nguyên tử.
B. Số P
C. Số nơtron
D. Cấu hình electron.
Chọn đáp án: C
Giải thích: Đồng vị là những nguyên tử có cùng số proton nhưng khác nhau về số nơtron.
Bài 30: Oxi có 3 đồng vị![]() số kiếu phân tử O2 có thể tạo thành là:
số kiếu phân tử O2 có thể tạo thành là:
A. 3 B. 4 C. 5 D. 6
Chọn đáp án: D
Giải thích: Các phân tử O2 tương ứng là:
16O16O 17O17O 18O18O
16O17O 17O18O 16O18O.
Bài 31: Nguyên tử của một nguyên tố có điện tích hạt nhân là 13+, số khối A=27.Số electron của nguyên tử đó là bao nhiêu?
A. 13 e B. 14 e C. 5 e D. 3 e
Chọn đáp án: A.
Giải thích: Số hạt p = e = 13.
Bài 32: Nguyên tử X, Y, Z có kí hiệu nguyên tử lần lượt:![]() . X, Y, Z là
. X, Y, Z là
A. ba đồng vị của cùng một nguyên tố.
B. các đồng vị của ba nguyên tố khác nhau.
C. ba nguyên tử có cùng số nơtron.
D. ba nguyên tố có cùng số khối.
Chọn đáp án: A.
Bài 33: Oxi có 3 đồng vị![]() . Chọn câu trả lời đúng.
. Chọn câu trả lời đúng.
A. Số proton của chúng lần lượt là 8, 9, 10.
B. Số nơtron của chúng lần lượt là 16, 17, 18.
C. Số nơtron của chúng lần lượt là 8, 9, 10.
D. Trong mỗi đồng vị số nơtron lớn hơn số proton.
Chọn đáp án: C.
Giải thích:
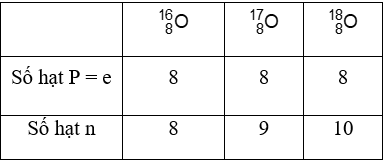
Bài 34: Nguyên tử của nguyên tố R có 56e và 81n. Kí hiệu nguyên tử của nguyên tố R là
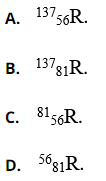
Chọn đáp án: A.
Giải thích: Kí hiệu hóa học của một nguyên tố X:![]()
A = Z + n = 56 + 81 = 137.
P = e = Z = 56.
Bài 35: Khi nói về số khối, điều khẳng định nào sau đây luôn đúng ?
A. Trong nguyên tử, số khối bằng tổng khối lượng các hạt proton và nơtron.
B. Trong nguyên tử, số khối bằng tổng số hạt các hạt proton và nơtron.
C. Trong nguyên tử, số khối bằng tổng các hạt proton, nơtron và electron.
D. Trong nguyên tử, số khối bằng nguyên tử khối.
Chọn đáp án: B.
Bài 36: Nguyên tử khối trung bình của đồng KL là 63,546. Đồng tồn tại trong tự nhiên với 2 đồng vị 63Cu và 65Cu thành phần trăm theo số nguyên tử của 65Cu là?
A. 23,7% B. 76,3% C. 72,7% D. 27,3%
Chọn đáp án: C.
Giải thích: Ta có, gọi % của đồng vị 63Cu = x, thì % đồng vị 65Cu = 100-x
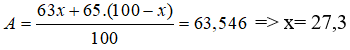
%65Cu = 72,7%.
Bài 37: Cho 3 nguyên tố:![]()
A. X và Y là 2 đồng vị của nhau
B. Y và Z là 2 đồng vị của nhau
C. X và Z là 2 đồng vị của nhau
D. Không có chất nào là đồng vị
Chọn đáp án: D
Giải thích: Đồng vị là những nguyên tử có cùng số proton. 3 nguyên tố X, Y, Z đều có số proton khác nhau ( px = 8, py = 9, pz = 18).
Bài 38: Cho 5 nguyên tử sau :![]() . Hỏi cặp ng tử nào là đồng vị của nhau?
. Hỏi cặp ng tử nào là đồng vị của nhau?
A. C và D B. C và E C. A và B D. B và C
Chọn đáp án: B.
Giải thích: Nguyên tử C và E cùng có số p = 8.
Bài 39: Nguyên tử của nguyên tố hoá học nào sau đây có cấu hình electron là: 1s22s22p63s23p64s1?
A. Na B. Ca C. K D. Mg
Chọn đáp án: C.
Giải thích: Tổng số e = 19 = p, nên nguyên tố là K.
Bài 40: Nguyên tố Agon có ba đồng vị khác nhau ,Ứng với số khối 36;38 và A3.% các đồng vị tương ứng lần lượt bằng 0,34%; 0,06% và 99,6%.Biết rằng nguyên tử khối trung bình của Agon bằng 39,985 .Số khối A3 của nguyên tố Agon là?
A. 41 B. 39 C. 40 D. 42
Chọn đáp án: C
Giải thích: Ta có phương trình:
![]()
Trên đây VnDoc đã giới thiệu tới các bạn lý thuyết Hóa học 10: Trắc nghiệm chương 1: Nguyên tử phần 1. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Chuyên đề Hóa học 10, Giải bài tập Hóa học lớp 10, Giải bài tập Vật Lí 10, Tài liệu học tập lớp 10 mà VnDoc tổng hợp và giới thiệu tới các bạn đọc.
