Trắc nghiệm chương 4: Phản ứng oxi hóa - khử phần 3
Chuyên đề Hóa học lớp 10: Trắc nghiệm chương 4: Phản ứng oxi hóa - khử phần 3 được VnDoc sưu tầm và giới thiệu tới các bạn học sinh cùng quý thầy cô tham khảo. Nội dung tài liệu sẽ giúp các bạn học sinh học tốt môn Hóa học lớp 10 hiệu quả hơn. Mời các bạn tham khảo.
Bài tập trắc nghiệm chương 4
Bài 1: Cho sơ đồ phản ứng: Fe(OH)2 + HNO3 → Fe(NO3)3 + NO + H2O. Sau khi cân bằng, hệ số của các chất tương ứng là
A. 3, 10, 3, 1, 8. B. 3, 28, 9, 1, 14.
C. 3, 26, 9, 2, 13. D. 2, 28, 6, 1, 14.
Đáp án A
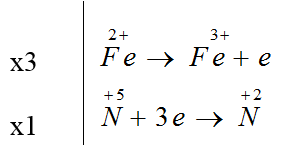
3Fe(OH)2 + 10HNO3 → 3Fe(NO3)3 + NO + 8H2O
Bài 2: Hòa tan hoàn toàn 2,4 gam kim loại Mg vào dung dịch HNO3 loãng, giả sử chỉ thu được V lít khí N2 là sản phẩm khử duy nhất (đktc). Giá trị của V là:
A. 0,672 lít. B. 6,72 lít. C. 0,448 lít. D. 4,48 lít.
Đáp án C.
nMg = 0,1 (mol)
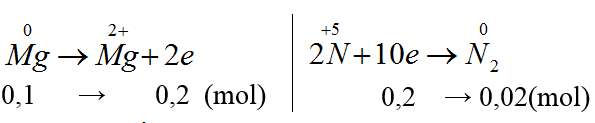
VN2 = 0,02.22,4 = 4,48 l
Bài 3: Phản ứng nào sau đây là phản ứng thế?
A. 4S + 8NaOH → Na2SO4 + 3Na2S + 4H2O
B. Fe + CuSO4 → FeSO4 + Cu.
C. 3Zn + 8HNO3 → 3Zn(NO3)2 + 2NO + 4H2O
D. Fe(NO3)2 + AgNO3 → Fe(NO3)3 + Ag
Đáp án B.
Phản ứng thế là phản ứng hóa học trong đó nguyên tử của đơn chất thay thế nguyên tử của một nguyên tố khác trong hợp chất.
Bài 4: Phản ứng nào sau đây là phản ứng trao đổi?
A. SO3 + H2O → H2SO4
B. 2Cu(NO3)2 → 2CuO + 4NO2 + O2
C. CO2 + C → 2CO
D. H2S + CuCl2 → CuS + 2HCl
Đáp án D.
Bài 5: Cho phản ứng:
aFe + bHNO3 → cFe(NO3)3 + dNO + eH2O
Các hệ số a,b, c, d, e là những số nguyên, đơn giản nhất. Tổng (a + b) bằng:
A. 4. B. 3. C. 6. D. 5.
Đáp án D
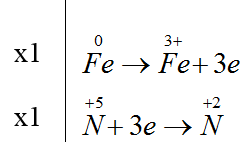
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
Tổng (a + b) bằng = 1+4 = 5
Bài 6: Nitơ trong chất nào sau đây vừa có tính oxi hoá, vừa có tính khử?
A. NH4Cl. B. NH3. C. N2. D. HNO3.
Đáp án C.
Bài 7: Cho phản ứng: Mg + H2SO4 → MgSO4 + H2S + H2O
Khi hệ số cân bằng phản ứng là nguyên và tối giản thì số phân tử H2O tạo thành là:
A. 3. B. 10. C. 5. D. 4.
Đáp án D.
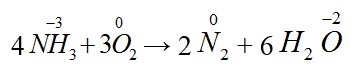
4Mg + 5H2SO4 → 4MgSO4 + H2S + 4H2O
Bài 8: Phản ứng nào sau đây là phản ứng oxi hóa – khử?
A. NH3 + HCl → NH4Cl
B. H2S + 2NaOH → Na2S + 2H2O
C. 4NH3 + 3O2 → 2N2 + 6H2O
D. H2SO4 + BaCl2 → BaSO4 ↓ + 2HCl
Đáp án C.
Sự thay đổi số oxi hóa của các chất:
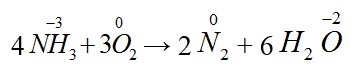
Bài 9: Trong phản ứng: CaCO3 → CaO + CO2, nguyên tố cacbon
A. chỉ bị oxi hóa.
B. chỉ bị khử.
C. vừa bị oxi hóa, vừa bị khử.
D. không bị oxi hóa, cũng không bị khử
Đáp án D.
Số oxi hóa của C trước và sau phản ứng không thay đổi.
Bài 10: Cho phản ứng hoá học sau: Al + HNO3 → Al(NO3)3 + NH4NO3 + H2O
Hệ số cân bằng của các chất trong sản phẩm lần lượt là:
A. 8, 3, 15. B. 8, 3, 9. C. 2, 2, 5. D. 2, 1, 4.
Đáp án B
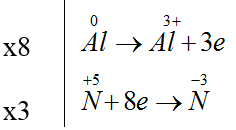
8Al + 30HNO3 → 8Al(NO3)3 + 3NH4NO3 + 9H2O
Bài 11: Mg có thể khử được axit HNO3 thành khí N2 theo phản ứng hoá học:
aMg + bHNO3 → cMg(NO3)2 + dN2 + eH2O
Tỉ lệ a:b là
A. 1:3. B. 5:12. C. 3:8. D. 4:15.
Đáp án B.
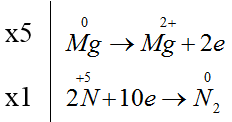
5Mg + 12HNO3 → 5Mg(NO3)2 + N2 + 6H2O
Bài 12: Chất nào sau đây trong các phản ứng chỉ đóng vai trò là chất oxi hóa?
A. S B. F2 C. Cl2 D. N2
Đáp án B.
F2 là nguyên tố có độ âm điện lớn nhất trong bảng tuần hoàn, là phi kim mạnh nhất.
Bài 13: Số oxi hóa của oxi trong các hợp chất HNO3, H2O2, F2O, KO2 theo thứ tự là
A. -2, -1, -2, -0,5. B. -2, -1, +2, -0, 5.
C. -2, +1, +2, +0,5. D. -2, +1, -2, +0,5.
Đáp án B.
Bài 14: Trong phản ứng oxi hóa – khử, chất bị oxi hóa là
A. chất nhận electron. B. chất nhường electron.
C. chất làm giảm số oxi hóa. D. chất không thay đổi số oxi hóa.
Đáp án B
Chất bị oxi hóa (chất khử) là chất nhường electron và có sự tăng số oxi hóa.
Bài 15: Cho phản ứng: Ca +Cl2 → CaCl2. Kết luận nào sau đây đúng
A. Mỗi nguyên tử Ca nhận 2e. B. Mỗi nguyên tử Cl nhận 2e.
C. Mỗi phân tử Cl2 nhường 2e. D. Mỗi nguyên tử Ca nhường 2e.
Đáp án D.
Bài 16: Oxit nào sau đây bị oxi hoá khi phản ứng với dung dịch HNO3 loãng?
A. MgO. B. Fe2O3. C. FeO. D. Al2O3.
Đáp án C.
Trong đáp án A,B,D các kim loại đều đã có số oxi hóa cao nhất. Không bị oxi hóa bởi HNO3.
Bài 17: Phản ứng nào dưới đây không phải phản ứng oxi hoá - khử?
A. 2NaOH + 2NO2 to→ NaNO2 + NaNO3 + H2O
B. 2KMnO4 to→ K2MnO4 + MnO2 + O2
C. 2Fe(OH)3 to→ Fe2O3 + 3H2O
D. 4Fe(OH)2 + O2 to→ 2Fe2O3 + 4H2O
Đáp án C.
Trong phản ứng, không xảy ra sự thay đổi số oxi hóa của các nguyên tố.
Bài 18: Phản ứng nào sau đây lưu huỳnh đóng vai trò là chất oxi hoá?
A. S+ O2 to→ SO2
B. S+ Na to→ Na2S
C. S+ H2SO4 → 3SO2 + 2H2O
D. S+ 6HNO3 to→ H2SO4 + 6NO2 + 2H2O
Đáp án B.
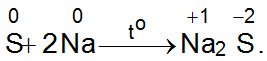
Bài 19: Chất hoặc ion nào sau đây có cả tính khử và tính oxi hoá?
A. SO2. B. F2. C. Al3+. D. Na.
Đáp án A.
Bài 20: Lưu huỳnh trong chất nào sau đây vừa có tính oxi hoá vừa có tính khử?
A. Na2SO4. B. SO2. C. H2S. D. H2SO4.
Đáp án B.
Trong SO2, số oxi hóa của S là +4, có khả năng tăng lên +6, thể hiện tính khử, hay giảm xuống -2 thể hiện tính oxi hóa.
Bài 21: Trong phản ứng: NO2 + H2O → HNO3 + NO, nguyên tố nitơ
A. chỉ bị oxi hóa.
B. chỉ bị khử.
C. vừa bị oxi hóa, vừa bị khử.
D. không bị oxi hóa, cũng không bị khử.
Đáp án C.
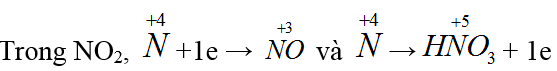
Bài 22: Trong phản ứng: Cu + 2H2SO4 (đặc, nóng) → CuSO4 + SO2 + 2H2O, axit sunfuric
A. là chất oxi hóa.
B. vừa là chất oxi hóa, vừa là chất tạo môi trường.
C. là chất khử.
D. vừa là chất khử, vừa là chất tạo môi trường.
Đáp án B.
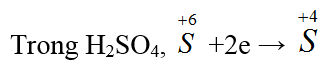
Bài 23: Trong phản ứng oxi hóa – khử, chất oxi hóa là
A. chất nhận electron.
B. chất nhường electron.
C. chất làm tăng số oxi hóa.
D. chất không thay đổi số oxi hóa.
Đáp án A.
Chất oxi hóa là chất nhận electron và có sự giảm số oxi hóa.
Bài 24: Cho phương trình hoá học của phản ứng: 2Cr + 3Sn2+ → 2Cr3+ + 3Sn
Nhận xét nào sau đây về phản ứng trên là đúng?
A. Cr là chất oxi hoá, Sn2+ là chất khử.
B. Sn2+ là chất khử, Cr3+ là chất oxi hoá.
C. Cr là chất khử, Sn2+ là chất oxi hoá.
D. Cr3+ là chất khử, Sn2+ là chất oxi hoá.
Đáp án C.
Cr có sự tăng số oxi hóa : chất khử, Sn2+ có sự giảm số oxi hóa : chất oxi hóa.
Bài 25: Cho phản ứng hoá học: Br2 + 5Cl2 + 6H2O ⇔ 2HBrO3 + 10HCl
Câu nào sau đây diễn tả đúng tính chất của các chất phản ứng?
A. Br2 là chất oxi hoá, Cl2 là chất khử.
B. Br2 là chất oxi hoá, H2O là chất khử.
C. Br2 là chất khử, Cl2 là chất oxi hoá.
D. Cl2 là chất oxi hoá, H2O là chất khử.
Đáp án C.
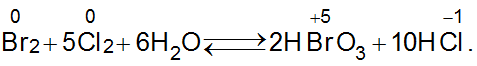
Br2 tăng số oxi hóa: chất khử, Cl2 giảm số oxi hóa: chất oxi hóa.
Trên đây VnDoc đã giới thiệu tới các bạn lý thuyết Hóa học 10: Trắc nghiệm chương 4: Phản ứng oxi hóa - khử phần 3. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Chuyên đề Hóa học 10, Giải bài tập Hóa học lớp 10, Giải bài tập Vật Lí 10, Tài liệu học tập lớp 10 mà VnDoc tổng hợp và giới thiệu tới các bạn đọc.
