Hóa học 10 bài 38: Cân bằng hóa học
Chuyên đề Hóa học lớp 10: Cân bằng hóa học được VnDoc sưu tầm và giới thiệu tới các bạn học sinh cùng quý thầy cô tham khảo. Nội dung tài liệu sẽ giúp các bạn học sinh học tốt môn Hóa học lớp 10 hiệu quả hơn. Mời các bạn tham khảo.
Cân bằng hóa học
A/ Lý thuyết Hóa học 10 bài 38
I. Phản ứng một chiều, phản ứng thuận nghịch và cân bằng hóa học
1. Phản ứng một chiều
Phản ứng một chiều là phản ứng trong đó các sản phẩm phản ứng không tác dụng được với nhau để tạo ra các chất tham gia phản ứng.
Ví dụ:
2KClO3 ![]() \(\overset{t^{\circ },MnO_{2} }{\rightarrow}\) 2KCl + 2O2
\(\overset{t^{\circ },MnO_{2} }{\rightarrow}\) 2KCl + 2O2
O2 tạo ra không tác dụng được với KCl để tạo thành KClO3.
2. Phản ứng thuận nghịch
Phản ứng thuận nghịch là phản ứng trong đó các chất tham gia phản ứng tác dụng với nhau để tạo thành sản phẩm đồng thời các sản phẩm phản ứng được với nhau để tạo ra các chất tham gia phản ứng.
Ví dụ: 3H2 + N2 ⇋ 2NH3
NH3 được tạo thành đồng thời lại bị phân hủy sinh ra H2 và N2 là các chất tham gia phản ứng.
3. Cân bằng hóa học
Cân bằng hóa học là trạng thái của phản ứng thuận nghịch khi tốc độ phản ứng thuận bằng tốc độ của phản ứng nghịch.
II. Hằng số cân bằng
1. Cân bằng trong hệ đồng thể
Hệ đồng thể là hệ không có bề mặt phân chia trong hệ.
Ví dụ hệ gồm các chất khí, hệ gồm các chất tan trong dung dịch.
Xét phản ứng thuận nghịch trong hệ đồng thể:
aA + bB ⇋ cC + dD
Trong đó A, B, C, D là những chất khí hay những chất tan trong một dung dịch. Khi phản ứng ở trạng thái cân bằng ta có:
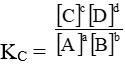
KC là hằng số cân bằng nồng độ của phản ứng chỉ phụ thuộc vào nhiệt độ, không phụ thuộc vào nồng độ các chất ban đầu.
Chú ý: Giá trị của hằng số KC phụ thuộc vào cách viết phương trình phản ứng hóa học.
2. Cân bằng trong hệ dị thể
Hệ dị thể là hệ là hệ có bề mặt phân chia trong hệ, qua bề mặt này có sự thay đổi đột ngột tính chất.
Ví dụ: hệ gồm chất rắn và chất khí, hệ gồm chất rắn và chất tan trong dung dịch.
Xét hệ cân bằng: C + CO2 ⇋ 2CO.
Hằng số cân bằng:
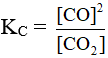
Nồng độ chất rắn coi là hằng số, nên trong biểu thức tính KC không tính chất rắn.
III. Sự chuyển dịch cân bằng hóa học
- Sự chuyển dịch cân bằng hóa học là sự chuyển từ trạng thái cân bằng này sang trạng thái cân bằng khác do tác động của các yếu tố từ bên ngoài lên cân bằng.
IV. Các yếu tố ảnh hưởng đến cân bằng hóa học
1. Ảnh hưởng của nồng độ
Khi tăng hoặc giảm nồng độ của một chất trong cân bằng thì cân bằng chuyển dịch theo chiểu làm giảm tác dụng của việc tăng hoặc giảm nồng độ của chất đó.
Lưu ý: Đối với hệ cân bằng có chất rắn thì việc thêm hay bớt lượng chất rắn không ảnh hưởng đến cân bằng, nghĩa là cân bằng không chuyển dịch.
2. Ảnh hưởng của áp suất Khi tăng hoặc giảm áp suất chung của hệ cân bằng thì cân bằng chuyển dịch theo chiều làm giảm tác dụng của việc tăng hoặc giảm áp suất đó.
Lưu ý: Khi hệ cân bằng có số mol khí ở 2 về bằng nhau hoặc trong hệ không có chất khí thì việc tăng, giảm áp suất chung của hệ không làm cho cân bằng chuyển dịch.
3. Ảnh hưởng của nhiệt độ
Khi tăng nhiệt độ thì cân bằng chuyền dịch theo chiều phản ứng thu nhiệt, nghĩa là làm giảm tác dụng của việc tăng nhiệt độ. Còn khi giảm nhiệt độ thì cân bằng chuyển dịch theo chiều phản ứng tỏa nhiệt, nghĩa là làm giảm tác dụng của việc giảm nhiệt độ.
Nguyên lí chuyển dịch cân bằng (Nguyên lí Lơ Sa-tơ-li-ê): "Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu một tác động bên ngoài, như biến đổi nồng độ, áp-suất, nhiệt độ sẽ chuyển dịch cân bằng theo chiều làm giảm tác động bên ngoài đó”.
4. Vai trò của chất xúc tác
Chất xúc tác không ảnh hưởng đến cân bằng vì không làm thay đổi nồng độ, áp suất và hằng số cân bằng.
Nhưng chất xúc tác làm tăng tốc độ phản ứng cả thuận và nghịch nên hệ nhanh chóng đạt đến cân bằng.
V. Ý nghĩa của tốc độ phản ứng và cân bằng hóa học trong sản xuất hóa học
Trong công nghiệp và sản xuất việc tăng tốc độ phản ứng và chuyển dịch cân bằng giúp phản ứng thực hiện nhanh và đạt hiệu suất cao.
B/ Trắc nghiệm Hóa học 10 bài 38
Câu 1: Hằng số cân bằng KC của một phản ứng xác định chỉ phụ thuộc vào
A. Nồng độ các chất
B. Áp suất
C. Nhiệt độ phản ứng
D. Hiệu suất phản ứng
Câu 2: Khi tăng áp suất của hệ phản ứng: CO(k) + H2O(k⇌ CO2(k) + H2(k)
thì cân bằng sẽ:
A. Chuyển dời theo chiều nghich
B. Chuyển dời theo chiều thuận
C. Không chuyển dịch
D. Chuyển dời theo chiều thuận rồi cân bằng
Câu 3: Phản ứng sản xuất vôi: CaCO3 (r) ⇌ CaO (r) + CO2 (k) ΔH> 0
Biện pháp kĩ thuật tác động vào quá trình sản xuất để tăng hiệu suất phản ứng là
A. Tăng nhiệt độ
B. Giảm áp suất
C. Tăng áp suất
D. Cả A và B
Câu 4: Ở 1000K hằng số cân bằng Kp của phản ứng
2SO2 + O2 ⇌ 2SO3
bằng 3,5 atm−1. Tính áp suất riêng úc cân bằng của SO2 nếu áp suất chung của hệ bằng 1atm và áp suất cân bằng của O2 bằng 0,1atm.
A. 0,18
B. 0,33
C. 0,57
D. Kết quả khác
Câu 5: Nén 2mol N2 và 8 mol H2 vào bình kín có thể tích là 2 lít (chỉ chứa sẵn chất xúc tác với thể tích không đáng kể) đã được giữ ở nhiệt đô khổng đổi. Khi phản ứng trong bình đạt cân bằng, áp suất các kí trong bình bằng 0,8 lần áp suất lúc đầu (khi mới cho vào bình, chưa xảy ra phản ứng). Nồng độ N2 thời điểm cân bằng là:
A. 2M
B. 2,5M
C. 0,5M
D. Kết quả khác
Câu 6: Cho cân bằng hóa học sau: 2SO2 (k) + O2 (k) ⇌ 2SO3 (k) ; ΔH < 0
Cho các biện pháp:
- Tăng nhiệt độ;
- Tăng áp suất chung của hệ phản ứng;
- Hạ nhiệt độ;
- Dùng thêm chất xúc tác V2O5;
- Giảm nồng độ SO3;
- Giảm áp suất chung của hệ phản ứng.
Trong các biện pháp trên, những biện pháp nào làm cân bằng chuyển dịch theo chiều thuận?
A. (1), (2), (4), (5)
B. (2), (3), (5)
C. (2), (3), (4), (6)
D. (1), (2), (5)
Câu 7: Cho cân bằng hóa học: 2SO2 (k) + O2 (k) ⇌ 2SO3 (k)
Khi tăng nhiệt độ thì tỉ khối của hỗn hợp khí so với H2 giảm đi. Phát biểu nào sau đây đúng khi nói về cân bằng hóa học này?
A. Phản ứng thuận thu nhiệt, cân bằng dịch chuyển theo chiều nghịch khi tăng nhiệt độ.
B. Phản ứng nghịch tỏa nhiệt, cân bằng chuyển dịch theo chiều thuận khi tăng nhiệt độ.
C. Phản ứng nghịch thu nhiệt, cân bằng chuyển dịch theo chiều thuận khi tăng nhiệt độ.
D. Phản ứng thuận tỏa nhiệt, cân bằng chuyển dịch theo chiều nghịch khi tăng nhiệt độ.
Câu 8: Cho cân bằng hóa học sau trong bình kín: 2NO2 (k) ⇌ N2O4 (k)
(màu nâu đỏ) (không màu)
Biết khi hạ nhiệt độ của bình thì màu nâu đỏ nhạt dần. Phản ứng thuận có
A. ΔH > 0, phản ứng tỏa nhiệt
B. ΔH < 0, phản ứng tỏa nhiệt
C. ΔH > 0, phản ứng thu nhiệt
D. ΔH <0, phản ứng thu nhiệt
Câu 9: Cho cân bằng hóa học: 2SO2 (k) + O2 (k) ⇌ 2SO3 (k)
Phản ứng thuận là phản ứng tỏa nhiệt. Phát biểu nào sau đây đúng?
A. Cân bằng chuyển dịch theo chiều thuận khi tăng nhiệt độ
B. Cân bằng chuyển dịch theo chiều nghịch khi giảm nồng độ O2
C. Cân bằng chuyển dịch theo chiều thuận khi giảm áp suất hệ phản ứng
D. Cân bằng chuyển dịch theo chiều nghịch khi giảm nồng độ SO3
Câu 10: Cho các cân bằng hóa học sau:
- 2SO2 (k) + O2 (k) ⇌ 2SO3 (k)
- N2 (k) + 3H2 ⇌ 2NH2 (k)
- 3CO2 (k) + H2 (k) ⇌ CO (k) + H2O (k)
- 2HI (k) ⇌ H2(k) + I2 (k)
Khi thay đổi áp suất, các cân bằng hóa học đều không bị chuyển dịch là
A. (1) và (3)
B. (2) và (4)
C. (1) và (2)
D. (3) và (4)
Câu 11: Xét cân bằng sau: CaCO3 (r) ⇌ CaO (r) + CO2 (k) ΔH= 178,5kJ
Người ta thực hiện các biện pháp sau:
- Tăng nhiệt độ
- Thêm lượng CaCO3 vào
- Lấy bớt CO2 ra
- Tăng áp suất chung bằng cách nén cho bớt thể tích của hệ giảm xuống
Có bao nhiêu yếu tố làm cân bằng trên sẽ chuyển dịch theo chiều thuận
A. 4
B. 3
C. 1
D. 2
Câu 12: Xét cân bằng: CO (k) + H2O (k) ⇌ CO2 (k) + H2 (k)
Biết rằng nếu thực hiện phản ứng giữa 1 mol CO và 1 mol H2O thì ở trạng thái cân bằng, có 2/3 mol CO2 được sinh ra. Tính hằng số cân bằng của phản ứng.
A. 0,4 mol
B. 1,2 mol
C. 0,9 mol
D. 0,6 mol
Câu 13: Cho cân bằng hóa học: 2A (k) ⇌ B (k) + C (k) (1)
Giả sử ở một nhiệt độ nào đó, hăng số cân bằng K của phản ứng bằng 1729.
Có bao nhiêu phần trăm A bị thủy phân ở nhiệt độ đó?
A. 7,9%
B. 6,9%
C. 3,8%
D. Kết quả khác
Câu 14: Ở nhiệt độ không đổi, hệ cân bằng nào sẽ chuyển dịch về phía bên phải nếu áp suất tăng?
A. 2H2 (k) + O2 ⇌ 2H2O
B. 2SO3 (k) ⇌ 2SO2 (k) + O2 (k)
C. 2NO (k) ⇌ N2 (k) + O2 (k)
D. 2CO2 (k) ⇌ 2CO (k) + O2 (k)
Câu 15: Trạng thái cân bằng của một phản ứng thuận nghịch xảy ra khi
A. Tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch
B. Phản ứng thuận và phản ứng nghịch dừng lại
C. Nồng độ các chất phản ứng bằng nồng độ các chất sản phẩm
D. Nồng độ các chất phản ứng giảm, còn nồng độ các chất sản phẩm tăng
Câu 16: Trong một bình kín có cân bằng hóa học sau: 2NO2(k) ⇌ N2O2 (k)
Tỉ khối hơi của hỗn hợp khí trong bình so với H2 ở nhiệt độ T1 bằng 27,6 và ở nhiệt độ T2 bằng 34,5. Biết T1 > T2
Phát biểu nào sau đây về cân bằng trên là đúng?
A. Phản ứng thuận là phản ứng tỏa nhiệt.
B. Khi tăng nhiệt độ, áp suất chung của hệ cân bằng giảm.
C. Khi giảm nhiệt độ, áp suất chung của hệ cân bằng tăng.
D. Phản ứng nghịch là phản ứng tỏa nhiệt.
Câu 17: Cho các cân bằng:
- H2 (k) + I2 (k) ⇆ 2HI (k)
- 2NO (k) + O2 (k) ⇆ 2NO2 (k)
- CO (k) + Cl2 (k) ⇆ COCl2 (k)
- CaCO2 (r) ⇆ CaO (r) + CO2 (k)
- 3Fe (r) + 4H2O (k) ⇆ Fe2O2 (r) + 4H2 (k)
Các cân bằng chuyển dịch theo chiều thuận khi tăng áp suất là
A. (1), (4).
B. (1), (5).
C. (2), (3), (5).
D. (2), (3).
Câu 18: Cho cân bằng (trong bình kín) sau:
CO (k) + H2O (k) ⇆ CO2 (k) + H2 (k); ΔH < 0
Trong các yếu tố:
- Tăng nhiệt độ;
- Thêm một lượng hơi nước;
- Thêm một lượng H2;
- Tăng áp suất chung của hệ;
- Dùng chất xúc tác.
Dãy gồm các yếu tố đều làm thay đổi cân bằng của hệ là
A. (1), (4), (5).
B. (1), (2), (3).
C. (2), (3), (4).
D. (1), (2), (4).
Câu 19: Trong phòng thí nghiệm người ta điều chế NO2 bằng cách cho Cu tác dụng với HNO3 đặc, đun nóng. NO2 có thể chuyển thành N2O4 theo cân bằng:
2NO2 ⇆ N2O4
Cho biết NO2 là khí có màu nâu và N2O4 là khí không màu. Khi ngâm bình chứa NO2 vào chậu nước đá thấy màu trong bình khí nhạt dần. Hỏi phản ứng thuận trong cân bằng trên là
A. Tỏa nhiệt.
B. Thu nhiệt.
C. Không toả hay thu nhiệt.
D. Một phương án khác.
Câu 20: Phản ứng : 2SO2 + O2 ⇆ 2SO3 ΔH < 0. Khi giảm nhiệt độ và khi giảm áp suất thì cân bằng của phản ứng trên chuyển dịch tương ứng là
A. Thuận và thuận.
B. Thuận và nghịch.
C. Nghịch và nghịch.
D. Nghịch và thuận.
Câu 21: Phát biểu nào sau đây là đúng?
A. Bất cứ phản ứng nào cũng đạt đến trạng thái cân bằng hóa học
B. Khi phản ứng thuận nghịch ở trạng thái cân bằng thì phản ứng dừng lại
C. Chỉ có những phản ứng thuận nghịch mới có trạng thái cân bằng hóa học
D. Sự có mặt của chất xúc tác không làm nồng độ các chất trong hệ cân bằng biến đổi
Câu 22: Xét phản ứng thuận nghịch sau: CO k + H2O(h) ⇌ CO2(k) + H2(k)
Ở 300∘C, hằng số cân bằng KC= 2. Nếu nồng độ ban đầu của [CO]= 3M và [H2] = 4M thì khi đạt trạng thái cân bằng (ở cùng nhiệt độ) thì nồng độ CO là:
A. 1M
B. 1,5M
C. 2M
D. 0,5M
Câu 23: Xét phản ứng: N2O4 (k) ⇌ 2NO2 (k)
Ban đầu nạp 0,12 mol khí N2O4 vào bình thủy tinh có dung tích 0,2 lít. Khi hệ đạt trạng thái cân bằng thì N2O4 có nồng độ là 0,25M. Hằng số cân bằng KC của phản ứng trên là bao nhiêu?
A. 1,00
B. 1,5
C. 1,96
D. 2,00
Câu 24: Người ta cho N2 và H2 vào trong bình kín dung tích không đổi và thực hiện phản ứng:
N2 + 3H2 ⇆ 2NH3
Sau một thời gian, nồng độ các chất trong bình như sau: [N2] = 2M; [H2] = 3M; [NH3] = 2M. Nồng độ mol/l của N2 và H2 ban đầu lần lượt là :
A. 3 và 6.
B. 2 và 3.
C. 4 và 8.
D. 2 và 4.
Câu 25: Thực hiện phản ứng tổng hợp amoniac: N2 + 3H2 ⇆ 2NH3
Nồng độ mol ban đầu của các chất như sau: [N2] = 1 mol/l; [H2] = 1,2 mol/l. Khi phản ứng đạt cân bằng nồng độ mol của [NH3] = 0,2 mol/l. Hiệu suất của phản ứng là
A. 43%.
B. 10%.
C. 30%.
D. 25%.
Câu 26. Cho cân bằng hóa học:
H2 (k) + I2 (k) ⇌ 2HI (k); ΔH > 0
Cân bằng không bị chuyển dịch khi
A. tăng nhiệt độ của hệ
B. giảm nống độ HI
C. tăng nồng độ H2
D. giảm áp suất chung của hệ.
Câu 27. Trong bình kín có hệ cân bằng hóa học sau:
CO2 (k) + H2 (k) ↔ CO (k) + H2O (k); ΔH >O
Xét các tác động sau đến hệ cân bằng:
a) Tăng nhiệt độ
b) Thêm một lượng hơi nước
c) giảm áp suất chung của hệ
d) dùng chất xúc tác
e) thêm một lượng CO2
Trong những tác động trên, tác động làm hệ cân bằng chuyển dịch theo chiều thuận là:
A. a); e)
B. b); c); d)
C. d), e)
D. a), c), e)
Câu 28. Cân bằng hóa học là:
A. Trạng thái của phản ứng thuận nghịch khi tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
B. trạng thái của phản ứng khi tốc độ phản ứng bằng nhau.
C. trạng thái của phản ứng khi tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch
D. trạng thái của phản ứng thuận nghịch khi tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
Câu 29. Sự dịch chuyển cân bằng hóa học là:
A. Sự chuyển dịch cân bằng hóa học là sự phá vỡ trạng thái cân bằng cũ để chuyển sang một trạng thái cân bằng mới do các yếu tố bên ngoài tác động lên cân bằng.
B. Sự chuyển dịch cân bằng hóa học là sự phá vỡ trạng thái cân bằng cũ để chuyển sang một trạng thái cân bằng mới.
C. Sự chuyển dịch cân bằng hóa học là sự phá vỡ trạng thái cân bằng này chuyển sang một trạng thái cân bằng khác.
D. Sự chuyển dịch cân bằng hóa học là sự chuyển trạng thái cân bằng cũ sang một trạng thái cân bằng.
Câu 30. Phát biểu nào trong 4 phát biểu về chất xúc tác không đúng?
A. Chất xúc tác làm tăng tốc độ phản ứng
B. Chất xúc tác làm giảm thời gian đạt tới cân bằng của phản ứng
C. Chất xúc tác được hoàn nguyên sau phản ứng
D. Chất xúc tác làm cho phản ứng dịch chuyển theo chiều thuận.
C/ Đáp án trắc nghiệm cân bằng hóa học
| 1C | 2B | 3D | 4B | 5C | 6B | 7D | 8B | 9B | 10D |
| 11D | 12C | 13 | 14A | 15A | 16A | 17D | 18B | 19A | 20B |
| 21C | 22 | 23C | 24A | 25D | 26D | 27A | 28A | 29A | 30B |
--------------------------------------
Trong phần chuyên đề trên đây chúng ta có thể hiểu biết thêm về Cân bằng hóa học gồm các khái niệm, ý nghĩa thực tiễn, các yếu tổ ảnh hưởng đến cân bằng hóa học.
Như vậy VnDoc đã giới thiệu các bạn tài liệu Lý thuyết Hóa học lớp 10 bài 38: Cân bằng hóa học. Mời các bạn tham khảo thêm tài liệu: Trắc nghiệm Sinh học 10, Giải bài tập Sinh học lớp 10, Giải Vở BT Sinh Học 10, Giải bài tập Sinh học 10 ngắn nhất, Tài liệu học tập lớp 10.
Để tiện trao đổi, chia sẻ kinh nghiệm về giảng dạy và học tập các môn học lớp 10, VnDoc mời các thầy cô giáo, các bậc phụ huynh và các bạn học sinh truy cập nhóm riêng dành cho lớp 10 sau: Nhóm Tài liệu học tập lớp 10. Rất mong nhận được sự ủng hộ của các thầy cô và các bạn.
