Hóa học 10 bài 24: Hợp chất chứa Oxi của Clo
Chuyên đề Hóa học lớp 10: Hợp chất chứa Oxi của Clo được VnDoc sưu tầm và giới thiệu tới các bạn học sinh cùng quý thầy cô tham khảo. Nội dung tài liệu sẽ giúp các bạn học sinh học tốt môn Hóa học lớp 10 hiệu quả hơn. Mời các bạn tham khảo.
Lý thuyết: Hợp chất chứa Oxi của Clo
A/ Lý thuyết Hóa học 10 bài 24
I. Sơ lược về các oxit và các axit có oxi của clo
- Axit chứa oxi của clo gồm: axit hipoclorơ HClO, axit clorơ HClO2, axit clorit HClO3, axit peclorit HClO4.
- Tính axit trong dung dịch tăng dần và tính oxi hóa giảm dần theo thứ tự: HClO, HClO2, HClO3, HClO4.
| Tính chất | HClO | HClO2 | HClO3 | HClO4 |
| Tính axit | Axit yếu | Axit trung bình | Axit mạnh | Axít rất mạnh |
| Tính bền | Kém bền | Kém bền | Kềm bền khi > 50% | Kém bền khi đun với P2O5 |
| Phản ứng minh họa | NaClO + CO2 + H2O → NaHCO3 + HClO 2HClO → 2HCl + O2 |
3HClO2 → 2HClO3 + HCl | 3HClO3 → HClO4 + Cl2O + H2O | HClO4 → Cl2O7 + H2O |
- Ngoài ra có các muối chứa oxi của Clo gồm: Nước gia-ven, clorua vôi, muối clorat.
- Trong các hợp chất chứa ôxi của Clo, Clo có số oxi hóa dương, được điều chế gián tiếp.
Cl2O Clo (I) oxit Cl2O7 Clo(VII) oxit
HClO Axit hipoclorơ NaClO Natri hipoclorit
HClO2 Axit clorơ NaClO2 Natri clorit
HClO3 Axit cloric KClO3 kali clorat
HClO4 Axit pecloric KClO4 kali peclorat
Tất cả hợp chất chứa oxi của clo điều là chất ôxi hóa mạnh.
II. Nước Gia-ven, clorua vôi, muối clorat
1. Nước Gia- ven:
Hỗn hợp gồm NaCl, NaClO và H2O có tính ôxi hóa mạnh, có tính tẩy màu, được điều chế bằng cách dẫn khí Clo vào dung dịch NaOH (KOH)
Cl2 + 2NaOH → NaCl + NaClO + H2O
NaClO + CO2 + H2O → NaHCO3 + HClO (có tính tẩy màu)
(Cl2 + 2KOH → KCl + KClO + H2O)
2. Clorua vôi
- Công thức phân tử CaOCl2.
- CT cấu tạo:
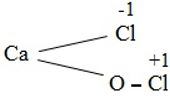
- Là chất ôxi hóa mạnh, được điều chế bằng cách dẫn clo vào dung dịch Ca(OH)2 đặc: Cl2 + Ca(OH)2 → CaOCl2 + H2O
Nếu Ca(OH)2 loãng: 2Ca(OH)2 + 2Cl2 → CaCl2 + Ca(OCl)2 + 2H2O
- Clorua vôi là chất bột màu trắng, có mùi xốc của khí clo.
- Clorua vôi cũng được dùng để tẩy trắng sợi, vải, giấy, để tẩy uế các hố rác, cống rãnh và một lượng lớn clorua vôi được dùng trong việc tinh chế dầu mỏ.
3. Muối clorat
- Công thức phân tử KClO3 là chất ôxi hóa mạnh thường dùng điều chế O2 trong phòng thí nghiệm
![]()
- KClO3 được điều chế khi dẫn khí clo vào dung dịch kiềm đặc đã được đun nóng đến 100oC.
![]()
- KClO3 được dùng chế tạo thuốc nổ, sản xuất pháo hóa, ngòi nổ và những hợp chất dễ cháy khác.
B/ Trắc nghiệm Hóa học 10 bài 24
Câu 1: Nước Gia- ven và clorua vôi có tính tẩy màu giấy, vải, sát trùng, tẩy uế môi trường vì
A. Oxi nguyên tử có tính oxi hóa mạnh.
B. Cl+ có tính oxi hóa mạnh.
C. Cl- và oxi nguyên tử có tác dụng phá hủy mạnh.
D. Do các muối tự phân hủy.
A. Clorua vôi rẻ tiền hơn.
B. Clorua vôi có hàm lượng hipoclorit cao hơn.
C. Clorua vôi để bảo quản và dễ chuyên chở hơn.
D. Tất cả đều đúng
A. Clorua vôi là muối tạo bởi một kim loại liên kết với một loại gốc axit
B. Clorua vôi là muối tạo bởi một kim loại liên kết với hai loại gốc axit
C. Clorua vôi là muối tạo bởi hai kim loại liên kết với một loại gốc axit
D. Clorua vôi không phải là muối
A. HCl, HClO, H2O
B. NaCl, NaClO, H2O
C. NaCl, NaClO3, H2O
D. NaCl, NaClO4, H2O
A. Do chất NaOCl phân hủy ra oxi nguyên tử có tính oxi hóa mạnh
B. Do chất NaOCl phân hủy ra Cl2 là chất oxi hóa mạnh
C. Do chất NaOCl, nguyên tử Cl có số oxi hóa là +1, thể hiện tính oxi hóa mạnh.
D. Do chất NaOCl trong nước Gia-ven có tính tẩy màu và sát trùng .
A. Muối trung hòa
B. Muối kép.
C. Muối của 2 axit.
D. Muối hỗn tạp
A. Nước Gia-ven là dung dịch hỗn hợp muối NaCl và NaClO.
B. Clorua vôi là chất bột màu trắng, xốp, có tính oxi hóa mạnh.
C. Nước Gia-ven dung để tẩy trắng vải, sợi và tẩy uế chuồng trại chăn nuôi, nhà vệ sinh.
D. Clorua vôi là muối tạo bởi một kim loại liên kết với một loại gốc axit.
A. Điện phân dung dịch NaCl có màng ngăn.
B. Điện phân dung dịch NaCl không có màng ngăn.
C. Cho khí clo tác dụng với dung dịch NaOH.
D. Cho khí flo tác dụng với dung dịch NaOH.
- Cl2 + NaOH → NaCl + NaClO + H2O
-
NaClO + CO2 + H2O → NaHCO3 + HClO
-
Cl2 + Ca(OH)2 → CaOCl2 + H2O
CaOCl2 + CO2 + H2O → CaCO3 + CaCl2 + HClO
Trong các phản ứng trên, số phản ứng thuộc loại phản ứng oxi hóa – khử là
A. 2 B. 3 C. 4 D. 1
Câu 10: Trong một loại nước clo ở 25℃, người ta xác định được nồng độ của clo là 0,06M, còn nồng độ của HCl và HClO đều là 0,03M. Thể tích khí clo (đktc) cần dùng để điều chế 5 lít nước clo trên là
A. 6,72 lít.
B. 3,36 lít.
C. 10,08 lít.
D. 13,44 lít.
Câu 11: Dẫn 4,48 lít hỗn hợp khí gồm N2 và Cl2 vào dung dịch Ca(OH)2 dư. Sau khi phản ứng xảy ra hoàn toàn, còn lại 1,12 lít khí thoát ra. Biết thể tích các khí đo ở điều kiện tiêu chuẩn. Thành phần phần trăm thể tích của Cl2 trong hỗn hợp trên là
A. 88,38%
B. 75,00%
C. 25,00%
D. 11,62%
Đáp án: B
Câu 12: Hấp thụ hoàn toàn 2,24 lít khí Cl2 (đktc) vào 200 ml dung dịch NaOH (ở nhiệt độ thường). Sau phản ứng, nồng độ NaOH còn lại là 0,5M (giả thiết thể tích dung dịch không thay đổi). Nông độ mol ban đầu của dung dịch NaOH là
A. 0,5M
B. 0,1M
C. 1,5M
D. 2,0M
Đáp án: C
nCl2 = 0,1; nNaOH (dư) = 0,2 . 0,5 = 0,1 mol
Cl2 + 2NaOH → NaCl + NaClO + H2O
⇒ nNaOH (bd) = 0,2 + 0,1 = 0,3 mol
⇒ CM NaOH = 0,3 / 0,2 = 1,5 M
Câu 13: Trong một loại nước clo ở 25℃, người ta xác định được nồng độ của clo là 0,06M, còn nồng độ của HCl và HClO đều là 0,03M. Thể tích khí clo (đktc) cần dùng để điều chế 5 lít nước clo trên là
A. 6,72 lít.
B. 3,36 lít.
C. 10,08 lít.
D. 13,44 lít.
Đáp án: C
nCl2 dư = 0,06 . 5 = 0,3 mol, nHCl = 0,03 . 5 = 0,15 mol
Cl2 + H20 → HCl + HClO
⇒ nCl2 (bd) = 0,3 + 0,15 = 0,45 (mol) ⇒ V = 0,45.22,4 = 10,08 (lít)
Câu 14: Hỗn hợp X gồm KClO3, Ca(ClO3)2, CaCl2 và KCl có khối lượng 82,3 gam. Nhiệt phân hoàn toàn X thu được 13,44 lít O2 (đktc), chất rắn Y gồm CaCl2 và KCl. Toàn bộ Y tác dụng vừa đủ với 0,3 lít dung dịch K2CO3 1M thu được dung dịch Z. Lượng KCl trong Z nhiều gấp 5 lần lượng KCl trong X. Thành phần phần trăm khối lượng KCl trong X là
A. 25,62%
B. 12,67%
C. 18,10%
D. 29,77%
Đáp án: C
nO2= 0,6 mol; nK2CO3= 0,3 mol ⇒ nCaCl2= nK2CO3 = 0,3 mol
Bảo toàn khối lượng: mY = 82,3 – 0,6.32 = 63,1 (gam).
⇒ mKCl (Y) = 63,1 – 0,3.111 = 29,8 (gam) ⇒ nKCl (Y)= 0,4 mol
⇒ nKCl (Z) = nKCl (Y) + 2nK2CO3 = 0,4 + 2.0,3 = 1 (mol)
⇒ nKCl (X) = 1/5.1 = 0,2 (mol)
⇒ %mKCl = 0,2.74,5/82,3.100% = 18,10%
Câu 15: Các axit : Pecloric, cloric, clorơ, hipoclorơ có công thức lần lượt là:
A. HClO4, HClO3, HClO, HClO2.
B. HClO4, HClO2, HClO3, HClO.
C. HClO3, HClO4, HClO2, HClO.
D. HClO4, HClO3, HClO2, HClO.
Đáp án: D
Câu 16: Cho sơ đồ:
Cl2 + KOH → A + B + H2O
Cl2 + KOH → A + C + H2O
Công thức hoá học của A, B, C, lần lược là :
A. KCl, KClO, KClO4.
B. KClO3, KCl, KClO.
C. KCl, KClO, KClO3.
D. KClO3, KClO4, KCl.
Đáp án: C
Câu 17: Dãy nào được xếp đúng thứ tự tính axit giảm dần?
A. HClO, HClO3, HClO2, HClO4.
B. HClO4, HClO3, HClO2, HClO.
C. HClO, HClO2, HClO3, HClO4.
D. HClO4, HClO2, HClO3, HClO.
Đáp án: C
Câu 18: Clorua vôi, nước Gia-ven (Javel) và nước clo thể hiện tính oxi hóa là do
A. chứa ion ClO-, gốc của axit có tính oxi hóa mạnh.
B. chứa ion Cl-, gốc của axit clohiđric điện li mạnh.
C. đều là sản phẩm của chất oxi hóa mạnh Cl2 với kiềm.
D. trong phân tử đều chứa cation của kim loại mạnh.
Đáp án: A
Câu 19: Clorua vôi là muối của kim loại canxi với 2 loại gốc axit là clorua Cl- và hipoclorit ClO-. Vậy clorua vôi gọi là muối gì?
A. Muối trung hòa
B. Muối kép.
C. Muối của 2 axit.
D. Muối hỗn tạp
Đáp án: D
Câu 20: Ứng dụng nào sau đây không phải của KClO3?
A. Sản xuất diêm.
B. Điều chế oxi trong phòng thí nghiệm.
C. Sản xuất pháo hoa.
D. Chế tạo thuốc nổ đen.
Đáp án: D
-------------------------------------------
Trong phần chuyên đề trên đây chúng ta có thể hiểu biết thêm về Hợp chất chứa Oxi của Clo gồm các phản ứng hóa học, cấu hình nguyên tử, điều chế các hợp chất chứa oxi của clo trong phòng thí nghiệm và thực tế...
Như vậy VnDoc đã giới thiệu các bạn tài liệu Lý thuyết Hóa học lớp 10 bài 24: Hợp chất chứa Oxi của Clo. Mời các bạn tham khảo thêm tài liệu: Trắc nghiệm Sinh học 10, Giải bài tập Sinh học lớp 10, Giải Vở BT Sinh Học 10, Giải bài tập Sinh học 10 ngắn nhất, Tài liệu học tập lớp 10.
Để tiện trao đổi, chia sẻ kinh nghiệm về giảng dạy và học tập các môn học lớp 10, VnDoc mời các thầy cô giáo, các bậc phụ huynh và các bạn học sinh truy cập nhóm riêng dành cho lớp 10 sau: Nhóm Tài liệu học tập lớp 10. Rất mong nhận được sự ủng hộ của các thầy cô và các bạn.
