Khoa học tự nhiên 9 Cánh diều bài 15
Giải bài tập Khoa học tự nhiên lớp 9 bài 15: Tính chất chung của kim loại chi tiết sách Cánh diều giúp học sinh xem và so sánh lời giải từ đó biết cách làm bài tập môn KHTN 9.
Bài: Tính chất chung của kim loại
Mở đầu trang 77 Bài 15 KHTN 9: Kim loại có vai trò quan trọng trong lịch sử phát triển của nhân loại. Từ khi được phát hiện, kim loại đã được khai thác và ứng dụng trong mọi mặt của cuộc sống.
Hãy quan sát và tìm hiểu tính chất của một số vật dụng được làm từ vật liệu kim loại xung quanh em.
Trả lời:
Xung quanh em có rất nhiều vật dụng được làm từ vật liệu kim loại. Ví dụ:
+ Con dao, cái liềm, cái kéo …. làm từ kim loại sắt.
+ Móc quần áo, cái nồi, hộp đựng thức ăn … làm từ kim loại nhôm.
+ Vòng tay, vòng cổ, nhẫn … được làm từ kim loại bạc và kim loại vàng …
Các kim loại khác nhau nhưng đều có một số tính chất vật lí chung như: tính dẻo, tính dẫn điện, dẫn nhiệt, tính ánh kim …
Ngoài ra, một số kim loại còn có các tính chất hoá học như: tác dụng với oxygen, tác dụng với phi kim khác, tác dụng với acid, tác dụng với muối …
I. Tính chất vật lí của kim loại
Câu hỏi 1 trang 77 KHTN 9: Các vật dụng trong hình 15.1 được chế tạo dựa trên tính chất vật lí nào của kim loại?

Trả lời:
Các vật dụng trong hình 15.1 được chế tạo dựa trên tính dẻo của kim loại.
Cụ thể: Kim loại có tính dẻo nên có thể rèn, kéo dài thành sợi hoặc dát mỏng. Dựa trên tính chất này, kim loại được dùng để tạo nên các đồ vật khác nhau như hộp đựng thức ăn bằng nhôm, giấy nhôm bọc thực phẩm, dây đồng, …
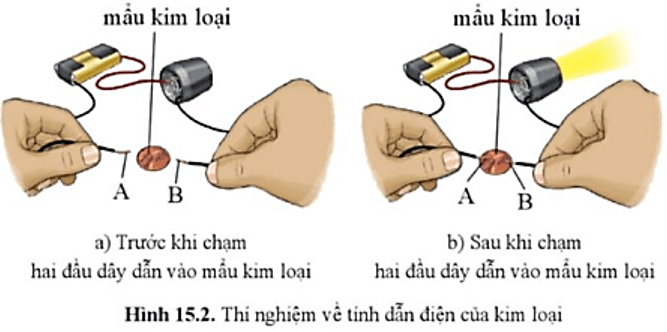
Câu hỏi 2 trang 78 KHTN 9: Quan sát hình 15.2 nêu hiện tượng trước và sau khi chạm hai đầu dây dẫn A và B vào mẩu kim loại. Giải thích.
Trả lời:
Hiện tượng:
- Trước khi chạm hai đầu dây dẫn vào mẩu kim loại, đèn không sáng.
- Sau khi chạm hai đầu dây dẫn vào mẩu kim loại, đèn sáng.
Giải thích: Do kim loại có tính dẫn điện.
Luyện tập 1 trang 78 KHTN 9: Dự đoán khả năng dẫn nhiệt của các kim loại Cu, Al, Fe và Ag theo chiều giảm dần.
Trả lời:
Kim loại dẫn điện tốt thường cũng dẫn nhiệt tốt.
Khả năng dẫn điện của các kim loại giảm dần theo thứ tự: Ag, Cu, Al, Fe.
Dự đoán khả năng dẫn nhiệt của các kim loại cũng giảm dần theo thứ tự: Ag, Cu, Al, Fe.
Câu hỏi 3 trang 79 KHTN 9: Quan sát đồ trang sức được làm bằng vàng, bạc (hình 15.5), em hãy cho biết màu sắc và vẻ sáng của chúng

Trả lời:
Vòng tay được làm bằng vàng có màu vàng, trên bề mặt có vẻ sáng lấp lánh.
Vòng tay được làm bằng bạc có màu trắng, trên bền mặt có vẻ sáng lấp lánh.
II. Tính chất hóa học
Câu hỏi 4 trang 80 KHTN 9: Viết các phương trình hóa học minh hoạ một số tính chất hoá học của kim loại mà em đã biết.
Trả lời:
Một số tính chất hoá học của kim loại mà em đã biết:
- Nhiều kim loại tác dụng với oxygen tạo thành oxide. Ví dụ:
3Fe + 2O2 ![]() \(\overset{to}{\rightarrow}\) Fe3O4
\(\overset{to}{\rightarrow}\) Fe3O4
- Nhiều kim loại tác dụng với phi kim tạo thành muối. Ví dụ:
2Fe + 3Cl2 ![]() \(\overset{to}{\rightarrow}\) 2FeCl3
\(\overset{to}{\rightarrow}\) 2FeCl3
- Nhiều kim loại tác dụng với acid (HCl, H2SO4 loãng …) tạo thành muối và giải phóng khí hydrogen. Ví dụ:
Fe + 2HCl → FeCl2 + H2
- Một số kim loại đẩy được kim loại đứng sau ra khỏi muối. Ví dụ:
Fe + CuSO4 → FeSO4 + Cu
- Một số kim loại tác dụng được với nước ở nhiệt độ thường tạo thành hydroxide và khí hydrogen. Ví dụ:
2Na + 2H2O → 2NaOH + H2
Câu hỏi 5 trang 80 KHTN 9: Quan sát hình 15.6 và cho biết khả năng phản ứng của natri với khí chlorine (b) như thế nào.

Trả lời:
Natri (sodium) nóng chảy phản ứng mãnh liệt với khí chlorine để tạo thành muối.
2Na + Cl2 ![]() \(\overset{to}{\rightarrow}\) 2NaCl
\(\overset{to}{\rightarrow}\) 2NaCl
Luyện tập 2 trang 80 KHTN 9: Thuỷ ngân dễ bay hơi và rất độc. Nếu chẳng may nhiệt kế thủy ngân bị vỡ thì có thể dùng bột lưu huỳnh rắc lên thuỷ ngân vì thuỷ ngân tác dụng với lưu huỳnh tạo thành chất mới không bay hơi và dễ thu gom hơn. Viết phương trình hoá học của phản ứng xảy ra.
Trả lời:
Phương trình hoá học:
Hg + S → HgS
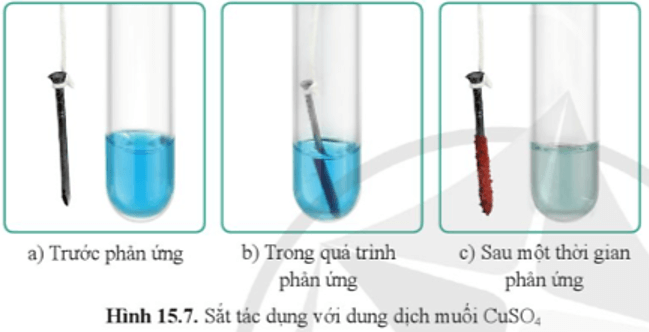
Câu hỏi 6 trang 81 KHTN 9: Quan sát hình 15.7, cho biết trước, trong và sau một thời gian phản ứng, màu của dung dịch CuSO4 và đinh sắt thay đổi như thế nào. Giải thích.
Trả lời:
|
Trước phản ứng |
Trong phản ứng |
Sau phản ứng |
|
|
Dung dịch CuSO4 |
Màu xanh |
Màu xanh nhạt dần |
Màu xanh nhạt |
|
Đinh sắt |
Màu xám trắng |
Có lớp kim loại màu đỏ bám dần vào bề mặt đinh sắt |
Có lớp kim loại màu đỏ bám ngoài bề mặt đinh sắt (phần nhúng vào dung dịch) |
Giải thích: Fe tác dụng với dung dịch CuSO4 tạo thành muối FeSO4 (làm dung dịch nhạt màu so với ban đầu) và Cu (bám ngoài đinh sắt).
Fe + CuSO4 → FeSO4 + Cu
Luyện tập 3 trang 81 KHTN 9: Viết phương trình hoá học của phản ứng xảy ra khi cho Zn tác dụng với O2, dung dịch H2SO4 loãng và dung dịch muối CuSO4
Trả lời:
Phương trình hoá học:
2Zn + O2 → 2ZnO
Zn + H2SO4loãng → ZnSO4 + H2
Zn + CuSO4 → ZnSO4 + Cu
Luyện tập 4 trang 81 KHTN 9: Giải thích vì sao thực phẩm có vị chua không nên đựng trong đồ dùng bằng kim loại mà nên đựng trong đồ dùng bằng thuỷ tinh, sành hoặc sứ.
Trả lời:
Vị chua của thực phẩm thường được gây ra bởi các acid. Không nên đựng thực phẩm có vị chua trong đồ dùng bằng kim loại do acid trong thực phẩm có thể tác dụng với kim loại trong vật đựng làm thực phẩm nhiễm độc kim loại, ảnh hưởng đến sức khoẻ người sử dụng.
III. Sự khác biệt về tính chất của một số kim loại
Câu hỏi 7 trang 82 KHTN 9: So sánh sự khác biệt về tính chất vật lí, tính chất hoá học và một số ứng dụng quan trọng của nhôm, sắt, vàng.
Trả lời:
- Khác biệt trong tính chất vật lí:
|
Kim loại Al |
Kim loại Fe |
Kim loại Au |
|
|
Tính chất vật lí chung |
- Là kim loại có màu trắng bạc, khá mềm, dẫn nhiệt, dẫn điện tốt và nhẹ. |
- Có màu trắng hơi xám, có tính dẻo, có độ cứng cao và có tính nhiễm từ. |
- Là kim loại có tính dẻo, tính dẫn điện, dẫn nhiệt tốt, có màu vàng lấp lánh. |
|
Khối lượng riêng (g/cm3) |
2,70 |
7,87 |
19,29 |
|
Nhiệt độ nóng chảy (oC) |
660 |
1 535 |
1 065 |
- Khác biệt trong tính chất hoá học:
|
Kim loại Al |
Kim loại Fe |
Kim loại Au |
|
|
Tác dụng với O2 |
Phản ứng tạo thành oxide kim loại (oxide lưỡng tính). 4Al + 3O2 |
Phản ứng tạo thành oxide kim loại (oxide base). 3Fe + 2O2 |
Không phản ứng |
|
Tác dụng với HCl |
Phản ứng tạo thành muối và giải phóng H2. 2Al + 6HCl → 2AlCl3 + 3H2 |
Phản ứng tạo thành muối và giải phóng H2. Fe + 2HCl → FeCl2 + H2 |
Không phản ứng |
- Ứng dụng quan trọng:
|
Kim loại Al |
Kim loại Fe |
Kim loại Au |
|
Nhôm thường được sử dụng làm dây dẫn điện và là nguyên liệu để sản xuất các vật dụng như khung cửa, vách ngăn, khung máy, … |
Sắt có nhiều ứng dụng trong đời sống và sản xuất, là thành phần chủ yếu trong gang và thép. |
Vàng được sử dụng làm đồ trang sức, một số chi tiết của vi mạch điện tử,.. |
Tìm hiểu thêm trang 82 KHTN 9: Vào khoảng thiên niên kỉ thứ IV trước Công nguyên, người nguyên thuỷ đã phát hiện ra một loại vật liệu mới để chế tạo công cụ và vũ khí thay thế cho đồ đá, đó là đồng.
Em hãy tìm hiểu quá trình con người phát hiện ra đồng.
Trả lời:
Học sinh tham khảo thông tin sau:
- Khu vực và thời gian phát minh ra đồng vẫn còn là chủ đề tranh cãi. Điều kiện cần thiết để người xưa phát hiện ra đồng là các mỏ đồng lộ thiên có hàm lượng đủ cao (có thể có kèm đồng nguyên sinh) nằm ở sườn hoặc hang núi thuận lợi cho trú ẩn. Người nguyên thủy đã cư trú ở đó, lấy các cây gỗ đốt lửa sưởi, tạo ra nhiệt độ cao làm than củi khử đồng khỏi quặng. Lúc đầu họ có thể sợ hãi thứ "đá lạ" đọng lại ở nền hang, nhưng rồi qua vài thế hệ sau người ta thấy "đá lạ" đó không đáng sợ mà còn dùng rất tốt cho chế tác công cụ.
- Khoảng 3500 năm TCN, cư dân Tây Á và Ai cập đã biết sử dụng đồng đỏ để chế tác công cụ lao động.
- Khoảng 2000 năm TCN, cư dân ở nhiều khu vực trên thế giới đã biết sử dụng đồng thau.
>>> Bài tiếp theo: Khoa học tự nhiên 9 Cánh diều bài 16
Trên đây là toàn bộ lời giải Giải SGK Khoa học tự nhiên lớp 9 bài 15: Tính chất chung của kim loại sách Cánh diều. Các em học sinh tham khảo thêm Ngữ văn 9 Cánh diều và Toán 9 Cánh diều. VnDoc liên tục cập nhật lời giải cũng như đáp án sách mới của SGK cũng như SBT các môn cho các bạn cùng tham khảo.

