Đáp án: C
Khoa học tự nhiên 9 bài 33: Metan
Bài 33: Metan
Khoa học tự nhiên 9 bài 33: Metan được VnDoc sưu tầm và đăng tải. Sách hướng dẫn học Khoa học Tự nhiên 9 tập 2 trang 9 nằm trong bộ VNEN của chương trình mới. Hy vọng với lời giải ngắn gọn dễ hiểu sẽ giúp các bạn học sinh củng cố lại kiến thức lớp 9. Mời các bạn tải về tham khảo chuẩn bị tốt cho bài học sắp tới của mình
- Khoa học tự nhiên 9 Bài 29: Di truyền học người
- Khoa học tự nhiên 9 Bài 30: Di truyền y học tư vấn
- Khoa học tự nhiên 9 Bài 31: Ôn tập phần Di truyền và biến dị
- Khoa học Tự nhiên 9 bài 32: Đại cương về hóa học hữu cơ
A. Hoạt động khởi động
Metan là hợp chất hữu cơ thuộc loại hirdocacbon no.
Tỉ khối của metan so với không khí xấp xỉ 0,55, trong đó hàm lượng % cacbon là 75%.
Xác định công thức phân tử và dựa vào hóa trị của C và H trong hợp chất hữu cơ viết công thức cấu tạo của metan.
Hầm biogas dùng để xử lí chất thải chăn nuôi và tạo ra khí sinh học hay còn gọi là khí biogas. Khí biogas có thành phần chính là metan. Khí biogas được dùng để làm gì trong thực tiễn? Chia sẻ hiểu biết của em với bạn bên cạnh.
Trả lời:
Gọi công thức phân tử của metan là ![]() \(C_xH_y\)
\(C_xH_y\)
Khối lượng mol của metan là: ![]() \(M_{metan} = 0,55 \times 29 = 16 = 12x+y (1)\)
\(M_{metan} = 0,55 \times 29 = 16 = 12x+y (1)\)
Tỉ lệ phần trăm về khối lượng của các nguyên tố trong metan: ![]() \(\frac{m_C}{m_H} = \frac{12x}{y} = \frac{75}{25} = 3 (2)\)
\(\frac{m_C}{m_H} = \frac{12x}{y} = \frac{75}{25} = 3 (2)\)
Từ (1) và (2): x = 1; y = 4. Vậy công thức phân tử của metan là: ![]() \(CH_4\)
\(CH_4\)
Công thức cấu tạo của metan là:
Khí biogas được dùng để nấu nướng trong thực tiễn.
B. Hoạt động hình thành kiến thức
1. Cấu tạo phân tử
Quan sát mô hình phân tử metan dưới đây, so sánh với công thức cấu tạo đã viết ở hoạt động khởi động, viết công thức cấu tạo của metan và cho biết phân tử này chứa loại liên kết gì? Tại sao gọi metan là hidrocacbon no?
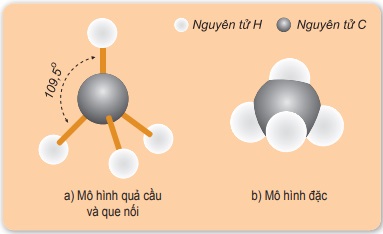
Trả lời:
Công thức cấu tạo viết ở phần hoạt động khởi động và công thức được được ra có sự khác nhau: Các hidro trong hình 33.2 không nằm trên cùng 1 mặt phẳng
Phân tử này chứa các liên kết đơn.
Gọi metan là hidrocacbon no vì: các nguyên tử của các nguyên tố trong metan liên kết với nhau bằng liên kết đơn.
2. Tính chất vật lý, hóa học
Quan sát thí nghiệm thử tính chất hóa học của metan, từ đó rút ra các kết luận về tính chất vật lý, hóa học của metan, viết PTHH của phản ứng xảy ra
Thí nghiệm: sgk trang 11
Trả lời:
| Thí nghiệm | Hiện tượng - Giải thích |
| Tác dụng với oxi |
Hiện tượng: Khí metan cháy cho ngọn lửa màu xanh. Giái thích: Do khí metan tác dụng được với khí oxi gây ra phản ứng cháy theo PTHH:
|
| Tác dụng với clo |
Hiện tượng: Quỳ tím chuyển màu đỏ Giải thích: Metan tác dụng được với nước clo theo PTHH:
|
3. Trạng thái tự nhiên và ứng dụng
Đọc thông tin dưới đây và trả lời câu hỏi
Thông tin: Sgk trang 11
Câu hỏi: Hãy cho biết, trong tự nhiên, metan có ở những nguồn nào, ứng dụng của metan là gì?
Trả lời:
Trong tự nhiên, metan có ở các mỏ khí, mỏ dầu, mỏ than, bùn ao, khí biogas, ...
Ứng dụng của metan: Dùng làm nhiên liệu, sản xuất hidro, bột than ...
C. Hoạt động luyện tập
Câu 1: Trang 12 khoa học tự nhiên 9 tập 2
Nhận định nào dưới đây không đúng về metan?
A. Metan có phản ứng thế với clo khi chiếu ánh sáng
B. Ứng dụng chủ yếu của metan là dùng làm nhiên liệu
C. Metan là chất khí, không màu nặng hơn không khí, ít tan trong nước
D. Đốt cháy hoàn toàn 1 thể tích khí metan sinh ra một thể tích ![]() \(CO_2\) và 2 thể tích hơi nước
\(CO_2\) và 2 thể tích hơi nước
Câu 2: Trang 12 khoa học tự nhiên 9 tập 2
Khi đốt 100 lít khí thiên nhiên chứa 96% ![]() \(CH_4,2\%N_2,2\%CO_2\) (về số mol). Thể tích khí
\(CH_4,2\%N_2,2\%CO_2\) (về số mol). Thể tích khí ![]() \(CO_2\) thải vào không khí là:
\(CO_2\) thải vào không khí là:
A. 94 lít
B. 96 lít
C. 98 lít
D. 100 lít
Ta có, tỉ lệ về số mol cũng bằng tỉ lệ về thể tích. Do đó, thể tích của các khí trong hỗn hợp ban đầu là:
![]() \(V_{CH_4}=96\%\times100=96(lít)\)
\(V_{CH_4}=96\%\times100=96(lít)\)
![]() \(V_{N_2}=2\%\times100=2(lít)\)
\(V_{N_2}=2\%\times100=2(lít)\)
![]() \(V_{CO_2}=2\%\times100=2(lít)\)
\(V_{CO_2}=2\%\times100=2(lít)\)
Trong hỗn hợp khí trên, chỉ có khí metan tham gia phản ứng cháy.
Phương trình phản ứng cháy của metan:
![]() \(CH_4+2O_2\rightarrow CO_2+2H_2\)
\(CH_4+2O_2\rightarrow CO_2+2H_2\)
Từ phương trình phản ứng, suy ra cứ 1 thể tích khí metan tạo ra một thể tích khí ![]() \(CO_2\)
\(CO_2\)
96 lít metan tạo ra 96 lít ![]() \(CO_2\).
\(CO_2\).
Vậy, thể tích ![]() \(CO_2\) thải vào không khí là:
\(CO_2\) thải vào không khí là: ![]() \(V_{CO_2} = V_{CO_2\; do\; pu\; cháy} + V_{CO_2\; có\; sẵn} = 96 + 2 = 98 (lít)\)
\(V_{CO_2} = V_{CO_2\; do\; pu\; cháy} + V_{CO_2\; có\; sẵn} = 96 + 2 = 98 (lít)\)
Đáp án: C
Câu 3: Trang 12 khoa học tự nhiên 9 tập 2
Trong những khí sau: metan, hidro, clo, oxi.
a) Những cặp khí nào tác dụng được với nhau ở điều kiện thích hợp?
b) Hai khí nào khi trộn với nhau có thể tạo ra hỗn hợp nổ?
a) Những cặp khí tác dụng được với nhau ở điều kiện thích hợp: metan và clo, metan và oxi, hidro và clo, hidro và oxi
b) Hai khí khi trộn với nhau có thể tạo ra hỗn hợp nổ: hidro và oxi, metan và oxi
Câu 4: Trang 12 khoa học tự nhiên 9 tập 2
Bằng phương pháp hóa học, hãy trình bày cách:
a) Nhận biết các khí sau đây: ![]() \(CO_2; \; CH_4;\; N_2;\; SO_2\)
\(CO_2; \; CH_4;\; N_2;\; SO_2\)
b) Tinh chế khí metan có lẫn khí: ![]() \(H_2S,\; SO_2\)
\(H_2S,\; SO_2\)
a)
Bước 1: Dùng cánh hoa hồng cho vào trong bình chứa mỗi khí, bình nào làm mất màu cánh hoa hồng là ![]() \(SO_2\)
\(SO_2\)
Bước 2: Sục các khí còn lại vào dung dịch nước vôi trong, bình nào làm nước vôi trong vẩn đục là ![]() \(CO_2\)
\(CO_2\)
Bước 3: Đốt hai khí còn lại, khí nào cháy với ngọn lửa màu xanh là ![]() \(CH_4\), còn lại là
\(CH_4\), còn lại là ![]() \(N_2\)(không có phản ứng cháy)
\(N_2\)(không có phản ứng cháy)
b) Dẫn hỗn hợp khí qua dung dịch nước vôi trong dư, ![]() \(SO_2;\; H_2S\) tạo thành kết tủa bị giữ lại.
\(SO_2;\; H_2S\) tạo thành kết tủa bị giữ lại.
PTHH:
![]() \(SO_2 + Ca(OH)_2 \rightarrow CaSO_3 + H_2O\)
\(SO_2 + Ca(OH)_2 \rightarrow CaSO_3 + H_2O\)
![]() \(H_2S + Ca(OH)_2 \rightarrow CaS + 2H_2O\)
\(H_2S + Ca(OH)_2 \rightarrow CaS + 2H_2O\)
Câu 5: Trang 12 khoa học tự nhiên 9 tập 2
Đốt cháy một lượng hỗn hợp X gồm metan và propan ![]() \((C_3H_8)\) ta thu được khí
\((C_3H_8)\) ta thu được khí ![]() \(CO_2\) và hơi nước theo tỉ lệ thể tích 3:5 (đo ở cùng điều kiện). Tính thành phần phần trăm theo thể tích của metan trong X.
\(CO_2\) và hơi nước theo tỉ lệ thể tích 3:5 (đo ở cùng điều kiện). Tính thành phần phần trăm theo thể tích của metan trong X.
Giả sư, trong hỗn hợp X có x (mol) metan và y (mol) propan.
PTHH:
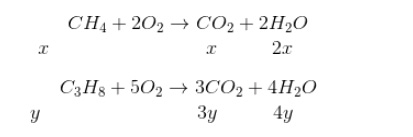
Tỉ lệ về số mol chính là tỉ lệ về thể tích, suy ra:  \(\frac{V_{CH_4}}{V_{C_3H_8}} = \frac{x}{y}\)
\(\frac{V_{CH_4}}{V_{C_3H_8}} = \frac{x}{y}\)
Theo bài ra: ![]() \(\frac{V_{CO_2}}{V_{H_2O}} = \frac{3}{5} = \frac{x + 3y}{2x + 4y} \Rightarrow \frac{x}{y} = 3\)
\(\frac{V_{CO_2}}{V_{H_2O}} = \frac{3}{5} = \frac{x + 3y}{2x + 4y} \Rightarrow \frac{x}{y} = 3\)
 \(\Rightarrow \frac{V_{CH_4}}{V_{C_3H_8}} = \frac{x}{y} = 3\)
\(\Rightarrow \frac{V_{CH_4}}{V_{C_3H_8}} = \frac{x}{y} = 3\)
Vậy, metan chiếm ![]() \(\%V_{CH_4} = \frac{3}{3+1} \times 100\% = 75\%\) theo thể tích trong hỗn hợp X
\(\%V_{CH_4} = \frac{3}{3+1} \times 100\% = 75\%\) theo thể tích trong hỗn hợp X
Câu 6: Trang 12 khoa học tự nhiên 9 tập 2
Nhiệt lượng tỏa ra khi đốt cháy hoàn toàn 1 mol khí ![]() \(CH_4\) là
\(CH_4\) là ![]() \(890kJ\). Để đun sôi 1 lít nước từ
\(890kJ\). Để đun sôi 1 lít nước từ ![]() \(20^{\circ}C\) cần 33,6 kJ và nhiệt thất thoát là 10%. Tính thể tích khí biogas (chứa 60% metan) cần dùng để đun sôi 2 lít nước như trên.
\(20^{\circ}C\) cần 33,6 kJ và nhiệt thất thoát là 10%. Tính thể tích khí biogas (chứa 60% metan) cần dùng để đun sôi 2 lít nước như trên.
Nhiệt lượng thất thoát là 10% nên hiệu suất là 90%
Nhiệt lượng thực tế cần để đun sôi 1 lít nước là: ![]() \(33,6 : 90% \approx 37,33 kJ\)
\(33,6 : 90% \approx 37,33 kJ\)
Nhiệt lượng thực tế cần để đun sôi 2 lít nước là: ![]() \(37,3\times 2 \approx 74,66 kJ\)
\(37,3\times 2 \approx 74,66 kJ\)
1 mol khí ![]() \(CH_4\) sinh ra 890 kJ. Vậy 74,66 kJ được tạo thành từ số mol
\(CH_4\) sinh ra 890 kJ. Vậy 74,66 kJ được tạo thành từ số mol ![]() \(CH_4\) là:
\(CH_4\) là: ![]() \(n=\frac{74,6}{890}\approx0,084mol\)
\(n=\frac{74,6}{890}\approx0,084mol\)
Thể tích khí metan cần dùng là: ![]() \(V_{metan} \approx 22,4\times 0,084 \approx 1,8816 (lít)\)
\(V_{metan} \approx 22,4\times 0,084 \approx 1,8816 (lít)\)
Thể tích khí biogas cần dùng là: ![]() \(V_{biogas} \approx 1,8816:60% \approx 3,136 (lít)\)
\(V_{biogas} \approx 1,8816:60% \approx 3,136 (lít)\)
E. Hoạt động tìm tòi, mở rộng
Trong hóa học hữu cơ, các chất có cấu tạo tương tự nhau và thành phần phân tử hơn kém nhau một hay nhiều nhóm ![]() \(−CH_2\) được gọi là đồng đẳng. Metan và các đồng đẳng của nó có nhiều ứng dụng trong công nghiệp và trong đời sống. Khí gas dùng trong bếp gas ở các hộ gia đình là hỗn hợp các khí đồng đẳng của metan. Tìm hiểu thông tin và trả lời câu hỏi.
\(−CH_2\) được gọi là đồng đẳng. Metan và các đồng đẳng của nó có nhiều ứng dụng trong công nghiệp và trong đời sống. Khí gas dùng trong bếp gas ở các hộ gia đình là hỗn hợp các khí đồng đẳng của metan. Tìm hiểu thông tin và trả lời câu hỏi.
Câu hỏi:
1. Em có biết thành phần chính của gas trong bình gas sử dụng để đun nấu là khí nào? Tại sao metan và các khí trong bình gas để đun nấu đều là chất không mùi mà khi bật bếp gas (lúc gas chưa cháy) thường thấy có mùi rất khó chịu? Mùi khó chịu đó là chất gì? Tại sao người ta phải cho chất đó vào khí gas cũng như khí thiên nhiên khi sử dụng chúng làm nhiên liệu?
2. Trong trường hợp bị rò rỉ khí gas chúng ta nên xử lí như thế nào?
3. Trên một số phương tiện thông tin đại chúng có đề cập đến vấn đề san gas từ các bình gas gia đình sang các bình gas mini. Đây là việc làm gây nguy hiểm cho người sử dụng. Vậy thành phần các khí trong bình gas gia đình và bình gas mini có gì khác nhau? Tại sao việc làm đó lại gây nguy hại cho người sử dụng
1.
- Thành phần chính của gas là propan
 \((C_3H_8)\) và butan
\((C_3H_8)\) và butan  \((C_4H_{10})\)
\((C_4H_{10})\) - Khi bật bếp gas thường có mùi vì người ta thêm một số chất phụ gia có mùi để cảnh báo khi gas bị rò rỉ.
- Phụ gia tạo mùi là các hợp chất mercaptan chứa lưu huỳnh vào để người sử dụng dễ phát hiện.
- Người ta thêm các chất đó để người sử dụng có thể dễ nhận biết khí gas khi bị rò rỉ, giảm thiểu thiệt hại.
2.
- Khi ngửi thấy mùi gas trong nhà (phát hiện có rò gas), tuyệt đối không động đến bất kỳ thiết bị nào có thể phát sinh tia lửa điện, không bật tắt công tắt đèn, quạt, đóng cắt mạch điện, kể cả điện thoại di động.
- Lập tức khoá van bình.
- Sử dụng các phương tiện thông gió thủ công, ví dụ quạt nan hoặc mảnh bìa cactong để quạt tản khí đi. Nếu quạt máy đang chạy thì vẫn để nguyên.
- Mở hết các cửa ở phía trên bếp (không phải là các cửa ngang bếp) để tạo đối lưu lên trên, khi nào gần hết mùi mới được mở hết các cửa nhà.
3. Do áp lực của bình gas gia đình và bình gas mini là khác nhau, nên hàm lượng propan và butan trong hai loại khí gas này là khác nhau do đó việc san gas từ bình gas gia đình sang bình gas mini không đảm bảo an toàn.
D. Hoạt động vận dụng
Hiện nay nhiều nơi sử dụng mô hình hầm biogas để thu lấy nhiên liệu dùng để đun nấu, chạy máy phát điện nhỏ, ... phục vụ cuộc sống. Bằng kiến thức hóa học, hãy giải thích tại sao có thể sử dụng khí biogas như vậy.
Tìm hiểu thêm về thành phần khí biogas, quá trình hình thành biogas, nguyên liệu có thể sử dụng để tạo khí biogas và chia sẻ, và đánh giá lợi ích của mô hình này với người thân trong gia đình em.
Thành phần chính của khí biogas là metan, metan cháy tỏa nhiều nhiệt nên khí biogas được dùng làm nhiên liệu.
Giải bài 33: Metan - Sách hướng dẫn học Khoa học Tự nhiên 9 tập 2 trang 9. Sách này nằm trong bộ VNEN của chương trình mới. Trên đây VnDoc hướng dẫn trả lời và giải đáp các câu hỏi trong bài học. Cách làm chi tiết, dễ hiểu, Hi vọng các bạn học sinh nắm tốt kiến thức bài học. Mời các bạn cùng tham khảo
............................................
Như vậy VnDoc đã giới thiệu các bạn tài liệu Khoa học tự nhiên 9 bài 33: Metan. Các bạn học sinh còn có thể tham khảo các đề thi học kì 1 lớp 9, đề thi học kì 2 lớp 9 các môn Toán, Văn, Anh, Lý, Địa, Sinh mà chúng tôi đã sưu tầm và chọn lọc. Với đề thi lớp 9 này giúp các bạn rèn luyện thêm kỹ năng giải đề và làm bài tốt hơn. Chúc các bạn ôn thi tốt
