Hóa học 8 Bài 33: Điều chế khí hiđro - Phản ứng thế
Hóa học 8 Bài 33 Điều chế khí hiđro - Phản ứng thế được VnDoc biên soạn là nội dung trọng tâm Hóa 8 bài 33, giúp các em biết điểu chế khí hidro trong phòng thí nghiệm, và điều chế trong công nghiệp, cung cấp cho em thêm định nghĩa về phản ứng thế. Giúp các em nắm chắc được nội dung bài.
Điều chế hiđro
Hy vọng với tài liệu này giúp các bạn học sinh học tốt hơn cũng như giúp ích cho quý thầy cô trong quá trình soạn giảng Hóa 8 bài 33 của mình. Mời các bạn tham khảo.
I. Tóm tắt lý thuyết hóa 8 bài 33
1. Điều chế khí hiđro trong phòng thí nghiệm.
Để điều chế khí H2 trong phòng thí nghiệm người ta có thể thay bằng dung dịch axit HCl bằng H2SO4 loãng thay kim loại Zn bằng Fe, Al,…
Phường trình hóa học:
Zn + 2HCl → ZnCl2 + H2
Fe + HCl → FeCl2 + H2
Kết luận:
Để nhận biết khí H2 sử dụng que đóm đang cháy, H2 cháy trong không khí cho ngọn lửa màu xanh.
Khí H2 ít tan trong nước và nhẹ hơn không khí, nên ta có thể thu H2 theo 2 cách: đẩy nước và đẩy không khí.
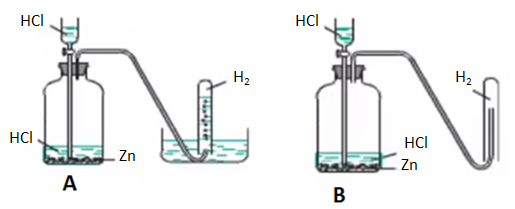
Hình A: Điều chế khí hiđro bằng cách đẩy nước
Hình B: Điều chế khí hiđro bằng cách đẩy không khí
2. Điều chế khí hidro trong công nghiệp
- Phương pháp điện phân nước
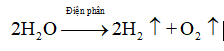
- Dùng than khử oxi của H2O ở nhiệt độ cao:
C + H2O ![]() \(\overset{t^{\circ } }{\rightarrow}\) H2 + CO
\(\overset{t^{\circ } }{\rightarrow}\) H2 + CO
Điều chế từ khí tự nhiên, khí mỏ dầu.
3. Phản ứng thế.
Định nghĩa: Phản ứng thế là phản ứng hóa học giữa đơn chất và hợp chất, trong đó nguyên tử của đơn chất thay thế nguyên tử của một nguyên tố khác trong hợp chất.
Xét phương trình phản ứng:
Zn + 2HCl → ZnCl2 + H2
(đơn chất) (hợp chất) (hợp chất) (đơn chất)
Nhận xét: Nguyên tử Zn đã thay thế nguyên tử H trong hợp chất HCl
Ví dụ:
Fe + H2SO4 (loãng) → FeSO4 + H2
2Al + 6HCl → 2AlCl3 + 3H2
II. Bài tập vận dụng mở rộng
Câu 1: Hiện tượng khi cho viên kẽm (Zn) vào dung dịch axit clohiđric (HCl) là
A. có kết tủa trắng.
B. có thoát khí màu nâu đỏ.
C. dung dịch có màu xanh lam.
D. viên kẽm tan dần, có khí không màu thoát ra.
Lời giải:
Hiện tượng khi cho viên kẽm (Zn) vào dung dịch axit clohiđric (HCl) là : viên kẽm tan dần, có khí không màu thoát ra.
PTHH: Zn + 2HCl → ZnCl2 + H2
Đáp án cần chọn là: D
Câu 2: Phản ứng nào dưới đây có thể tạo được khí hiđro?
A. Cu + HCl
B. CaO + H2O
C. Fe + H2SO4
D. CuO + HCl
Lời giải:
Phản ứng tạo được khí hiđro là: Fe + H2SO4 → FeSO4 + H2
Đáp án cần chọn là: C
Câu 3: Sau phản ứng Zn và HCl trong phòng thí nghiệm, đưa que đóm đang cháy vào ống dẫn khí, khí thoát ra cháy được trong không khí với ngọn lửa màu gì?
A. Đỏ
B. Xanh nhạt
C. Cam
D. Tím
Lời giải:
Phản ứng Zn và HCl trong phòng thí nghiệm:
PTHH: Zn + 2HCl → ZnCl2 + H2
Khí thoát ra là H2, cháy được trong không khí với ngọn lửa màu xanh nhạt.
Đáp án cần chọn là: B
Câu 4: Có mấy phương pháp thu khí hiđro?
A. 1
B. 2
C. 3
D. 4
Lời giải:
Có 2 phương pháp thu khí hiđro là phương pháp đẩy nước và phương pháp đẩy không khí.
Đáp án cần chọn là: B
Câu 5: Dung dịch axit được dùng để điều chế hiđro trong phòng thí nghiệm là:
A. H2SO4 đặc
B. HNO3 loãng
C. H2SO4 loãng
D. A và B đều đúng
Lời giải:
Dung dịch axit được dùng để điều chế hiđro trong phòng thí nghiệm là: dung dịch H2SO4 loãng
Đáp án cần chọn là: C
Câu 6: Điều chế hiđro trong công nghiệp bằng cách
A. từ thiên nhiên – khí dầu mỏ.
B. điện phân nước.
C. từ nước và than.
D. cả 3 cách trên.
Lời giải:
Điều chế hiđro trong công nghiệp bằng cách :
* Phương pháp điện phân nước.
2H2O →2H2↑ + O2↑
* Dùng than khử oxi của H2O ở nhiệt độ cao: C + H2O → CO + H2
* Điều chế từ khí tự nhiên, khí mỏ dầu.
Đáp án cần chọn là: D
Câu 7: Điều chế hiđro trong công nghiệp, người ta dùng:
A. Zn + HCl
B. Fe + H2SO4
C. Điện phân nước
D. Khí dầu hỏa
Lời giải:
Điều chế hiđro trong công nghiệp, người ta dùng phương pháp điện phân nước
Đáp án cần chọn là: C
Câu 8: Cho Al tác dụng tác dụng với H2SO4 loãng tạo ra mấy sản phẩm?
A. 2
B. 1
C. 3
D. 4
Lời giải:
Cho Al tác dụng tác dụng với H2SO4 loãng xảy ra phản ứng:
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
=> phản ứng tạo ra 2 sản phẩm
Đáp án cần chọn là: A
Câu 9: Đâu là phản ứng thế trong các phản ứng sau?
A. Fe + 2HCl → FeCl2 + H2
B. NaOH + HCl → NaCl + H2O
C. Cu + 2FeCl3 → CuCl2 + 2FeCl2
D. CuO + 2HCl → CuCl2 + H2O
Lời giải:
Phản ứng thế là: Fe + 2HCl → FeCl2 + H2
Đáp án cần chọn là: A
Câu 10: Phản ứng nào dưới đây là phản ứng thế?
A. 2KClO3→ 2KCl + 3O2.
B. SO3 + H2O → H2SO4.
C. Fe2O3 + 6HCl → 2FeCl3 + 3H2O.
D. Fe3O4 + 4H2→ 3Fe + 4H2O.
Lời giải:
Phản ứng thế là phản ứng hóa học trong đó nguyên tử của nguyên tố này thay thế nguyên tử của nguyên tố khác trong hợp chất
Đáp án A: phản ứng phân hủy
Đáp án B: phản ứng hóa hợp
Đáp án C: phản ứng trao đổi
Đáp án D: phản ứng thế
Đáp án cần chọn là: D
Câu 11: Chọn đáp án đúng:
A. Phản ứng giữa FeO và HCl là phản ứng oxi hóa – khử.
B. Phản ứng giữa Fe và HCl là phản ứng thế.
C. CaCO3to→→to CaO + CO2 là phản ứng khử.
D. Khí H2 nặng hơn không khí.
Lời giải:
A sai vì không xảy ra cả sự oxi hóa và sự khử
B đúng vì Fe thế chỗ của nguyên tử H
PTHH: Fe + 2HCl → FeCl2 + H2
C sai vì đây là phản ứng phân hủy, không phải phản ứng khử.
D sai vì khí H2 nhẹ hơn không khí
Đáp án cần chọn là: B
Câu 12: Cho 6,5 gam Zn phản ứng với axit clohiđric (HCl) thấy có khí bay lên với thể tích là
A. 2,24 lít.
B. 0,224 lít.
C. 22,4 lít.
D. 4,48 lít.
Lời giải:
Số mol Zn là: nZn= 6,5/65= 0,1mol
PTHH: Zn + 2HCl → ZnCl2 + H2
Tỉ lệ PT: 1mol 1mol
P/ứng: 0,1mol → 0,1mol
=> thể tích khí bay lên là: VH2=0,1.22,4=2,24 lít
Đáp án cần chọn là: A
Câu 13: Cho một thanh sắt nặng 5,6 gam vào bình đựng dung dịch axit clohiđric loãng, dư thu được dung dịch A và khí bay lên. Cô cạn dung dịch A được m gam chất rắn. Hỏi dung dịch A là gì và tìm m
A. FeCl2; m = 12,7 gam
B. FeCl2 ; m = 17,2 gam
C. FeCl3; m = 55,3 gam
D. Không xác định được
Lời giải:
Số mol Fe phản ứng là: nFe= 6,5/65=0,1 mol
PTHH: Fe + 2HCl → FeCl2 + H2
Tỉ lệ PT: 1mol → 1mol
P/ứng: 0,1mol → 0,1mol
Cô cạn dung dịch A thu được chất rắn => chất rắn là FeCl2
=> Khối lượng FeCl2 thu được là: mFeCl2=0,1.127=12,7gam
Đáp án cần chọn là: A
Câu 14: Tính khối lượng của Al khi cho phản ứng với axit sunfuric (H2SO4) thấy có 1,68 lít khí thoát ra.
A. 2,025 gam
B. 5,24 gam
C. 6,075 gam
D. 1,35 gam
Lời giải:
Số mol khí H2 là: nH2 =1,68/22,4 = 0,075mol
PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Tỉ lệ PT: 2mol 3mol
P/ứng: 0,05mol ← 0,075mol
=> Khối lượng Al đã phản ứng là: mAl = 0,05.27 = 1,35 gam
Đáp án cần chọn là: D
Câu 15: Cho các phản ứng hoá học sau: (coi điều kiện có đủ)
(1): ZnO + 2HCl -> ZnCl2 + H2O.
(2): 2Cu + O2 -> 2CuO.
(3): Fe + 2HCl -> FeCl2 + H2.
(4): 2KMnO4 -> K2MnO4 + MnO2 + O2.
(5): 2Na + 2H2O -> 2NaOH + H2.
(6): Na2O + H2O -> 2NaOH.
Số phản ứng thế là:
A. 1
B. 2
C. 3
D. 4
Lời giải:
(3) và (5) là phản ứng thế
Đáp án cần chọn là: B
Câu 16: Cho một lượng dư bột sắt Fe phản ứng với dung dịch axit clohiđric HCl, sau khi phản ứng xảy ra thu được các sản phẩm là:
A. Fe dư, FeCl2, H2.
B. FeCl2, H2.
C. Fe dư, FeCl2.
D. FeCl2.
Lời giải:
Fe dư + 2HCl → FeCl2 + H2↑
=> Sản phẩm gồm: FeCl2, H2 và Fe dư
Đáp án cần chọn là: A
Chú ý
Có dư Fe sau phản ứng
Câu 17: Trong phòng thí nghiệm có các kim loại Zn (A) và Mg (B), các dung dịch H2SO4 loãng (C) và HCl (D). Muốn điều chế được 1,12 lít khí H2 (ở đktc) từ một
kim loại và một dung dịch axit nhưng lượng sử dụng ít nhất thì dùng:
A. B và C.
B. B và D.
C. A và C.
D. A và D.
Lời giải:
nH2(ĐKTC) = 1,12 /22,4 = 0,05 (mol)
Điều chế cùng một lượng H2 từ một kim loại và một dung dịch axit => ta chọn dùng Mg và HCl
Đáp án cần chọn là: B
.......................
Mời các bạn tham khảo thêm một số tài liệu liên quan:
Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Chuyên đề Toán 8, Chuyên đề Vật Lý 8, Chuyên đề Hóa 8, Tài liệu học tập lớp 8 mà VnDoc tổng hợp và đăng tải.
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu học tập THCS miễn phí trên Facebook: Tài liệu học tập lớp 8. Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu mới nhất.
