Hóa học 8 Bài 5: Nguyên tố hóa học
Hóa học 8 Bài 5: Nguyên tố hóa học là toàn bộ nội dung cơ bản của Bài 5 trong chương trình Hóa học lớp 8. Từ những khái niệm căn bản giúp đưa các bạn học sinh đến gần hơn với môn Hóa học. Hy vọng đây sẽ là tài liệu hay giúp cho việc dạy và học của quý thầy cô trong việc soạn hóa 8 bài 5 và các em học sinh trở nên dễ dàng và hiệu quả hơn.
>> Mời các bạn tham khảo đề thi giữa học kì 1 hóa 8 năm 2023 tại:
- Đề thi giữa kì 1 Hóa 8 năm 2023 Đề 1
- Đề thi giữa kì 1 Hóa 8 năm 2023 Đề 3
- 10 đề thi giữa học kì 1 lớp 8 môn Hóa năm 2022 - 2023 Có đáp án
Hóa 8 bài 5: Nguyên tố hóa học
A. Tóm tắt lý thuyết Hóa 8 bài 5
I. Khái niệm nguyên tố hóa học
1. Định nghĩa
Nguyên tố hóa học là tập hợp những nguyên tử cùng loại, có cùng số proton trong hạt nhân
- Số proton là số đặc trưng của một nguyên tố hóa học.
- Các nguyên tử cùng 1 nguyên tố đều có tính chất hóa học như nhau.
2. Kí hiệu hóa học.
Mỗi nguyên tố hóa học học được biểu diễn ngắn gọn bằng một kí hiệu hóa học
Ví dụ:
Kí hiệu hóa học của nguyên tố Hidro: H
Kí hiệu hóa học của nguyên tố Canxi: Ca
Kí hiệu hóa học của nguyên tố Magie: Mg
Kí hiệu hóa học của nguyên tố Sắt: Fe
(Xem đầy đủ kí hiệu các nguyên tố hóa học SGK/42)
- Quy ước mỗi kí hiệu nguyên tố còn chỉ 1 nguyên tử nguyên tố đó
Ví dụ: muốn chỉ 2 nguyên tử hidro: 2H
Muốn chỉ 3 nguyên tử N: 3N
II. Nguyên tử khối
- Nguyên tử khối (NTK) tính bằng gam cho biết độ nặng nhẹ khác nhau giữa các nguyên tử và là đại lượng đặc trưng cho mỗi nguyên tố.
- Khối lượng của 1 nguyên tố C = 1,9926.10-23
- Quy ước lấy 1/12 khối lượng của nguyên tử Cacbon làm đơn vị khối lượng cho nguyên tử, gọi là đơn vị cacbon. Viết tắt đvC
- Cách tính nguyên tử khối: Nguyên tử khối là con số so sánh khối lượng của nguyên tử với 1/12 khối lượng nguyên tử cacbon.
1đvC = ![]() \(\frac{1}{{12}}\) khối lượng nguyên tử C
\(\frac{1}{{12}}\) khối lượng nguyên tử C
NTK A = Khối lượng nguyên tử A tính bằng gam/Khối lượng của 1đvC tính ra gam
Ví dụ:
NTK của oxi =  \(\frac{{2,{{6568.10}^{ - 23}}}}{{0,{{16605.10}^{ - 23}}}} = 16\)
\(\frac{{2,{{6568.10}^{ - 23}}}}{{0,{{16605.10}^{ - 23}}}} = 16\)
( ![]() \(\frac{1}{{12}}\) nguyên tử C có khối lượng =
\(\frac{1}{{12}}\) nguyên tử C có khối lượng = ![]() \(\frac{{1,{{9926.10}^{ - 23}}}}{{12}} = 0,{16605.10^{ - 23}}\) hoặc 1,66.10-24g)
\(\frac{{1,{{9926.10}^{ - 23}}}}{{12}} = 0,{16605.10^{ - 23}}\) hoặc 1,66.10-24g)
Ví dụ:
C = 12 đvC
Mg = 24 đvC
Fe = 56 đvC
O = 16 đvC
Ca = 40 đvC
III. Có bao nhiêu nguyên tố hóa học?
- Ngày nay, khoa học đã biết được 110 nguyên tố có trong tự nhiên (kể cả Mặt Trời, Trái Đất,…)
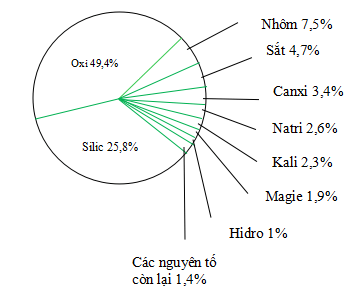
Hình 1. Tỉ lệ (%) về thành phần khối lượng các nguyên tố trong vỏ Trái Đất
- 92 nguyên tố có trong tự nhiên:
Các nguyên tố tự nhiên có trong vỏ Trái Đất rất không đồng đều
Oxi là nguyên tố phổ biến chiếm: 49,4%
Bảng nguyên tố hóa học 8
|
Số proton |
Tên Nguyên tố |
Ký hiệu hoá học |
Nguyên tử khối |
Hoá trị |
|
1 |
Hiđro |
H |
1 |
I |
|
2 |
Heli |
He |
4 |
|
|
3 |
Liti |
Li |
7 |
I |
|
4 |
Beri |
Be |
9 |
II |
|
5 |
Bo |
B |
11 |
III |
|
6 |
Cacbon |
C |
12 |
IV, II |
|
7 |
Nitơ |
N |
14 |
II, III, IV… |
|
8 |
Oxi |
O |
16 |
II |
|
9 |
Flo |
F |
19 |
I |
|
10 |
Neon |
Ne |
20 |
|
|
11 |
Natri |
Na |
23 |
I |
|
12 |
Magie |
Mg |
24 |
II |
|
13 |
Nhôm |
Al |
27 |
III |
|
14 |
Silic |
Si |
28 |
IV |
|
15 |
Photpho |
P |
31 |
III, V |
|
16 |
Lưu huỳnh |
S |
32 |
II, IV, VI |
|
17 |
Clo |
Cl |
35,5 |
I,… |
|
18 |
Argon |
Ar |
39,9 |
|
|
19 |
Kali |
K |
39 |
I |
|
20 |
Canxi |
Ca |
40 |
II |
|
24 |
Crom |
Cr |
52 |
II, III |
|
25 |
Mangan |
Mn |
55 |
II, IV, VII… |
|
26 |
Sắt |
Fe |
56 |
II, III |
|
29 |
Đồng |
Cu |
64 |
I, II |
|
30 |
Kẽm |
Zn |
65 |
II |
|
35 |
Brom |
Br |
80 |
I… |
|
47 |
Bạc |
Ag |
108 |
I |
|
56 |
Bari |
Ba |
137 |
II |
|
80 |
Thuỷ ngân |
Hg |
201 |
I, II |
|
82 |
Chì |
Pb |
207 |
II, IV |
Chú thích:
- Nguyên tố phi kim: chữ màu xanh
- Nguyên tố kim loại: chữ màu đen
- Nguyên tố khí hiếm: chữ màu đỏ
Một số nhóm nguyên tử
|
Tên nhóm |
Hoá trị |
Gốc axit |
Khối lượng gốc axit |
Axit tương ứng |
Khối lượng axit |
Tính axit |
|
Hiđroxit(*) (OH); Nitrat (NO3); Clorua (Cl) |
I |
NO3 |
62 |
HNO3 |
63 |
Mạnh |
|
Sunfat (SO4); Cacbonat (CO3) |
II |
SO4 |
96 |
H2SO4 |
98 |
Mạnh |
|
Photphat (PO4) |
III |
Cl |
35,5 |
HCl |
36,5 |
Mạnh |
|
(*): Tên này dùng trong các hợp chất với kim loại. |
PO4 |
95 |
H3PO4 |
98 |
Trung bình |
|
|
CO3 |
60 |
H2CO3 |
62 |
Rất yếu (không tồn tại) |
||
>> Bài tiếp theo: Hóa học 8 Bài 6: Đơn chất và Hợp chất - Phân tử
IV. Luyện tập
Luyện tập củng cố nội dung bài học ngay tại:
B. Bài tập Hóa 8 bài 5
Câu 1. Trong số các kim loại, nguyên tử của kim loại nào là nặng nhất? Nó nặng gấp bao nhiêu lần kim loại nhẹ nhất? (Chỉ xét các kim loại có trong bảng 1, SGK/42)
Câu 2. Phân biệt sự khác nhau giữa 2 khái niệm nguyên tố và nguyên tử
Câu 3. Cách biểu diễn các nguyên tố hóa dưới đây cho biết ý nghĩa gì: 2C, 3Cu, 5Fe, 2H, O.
Câu 4. Kí hiệu hóa học chỉ ra điều gì? Viết kí hiệu hóa học biểu diễn các nguyên tố lưu huỳnh, sắt, nhôm, magie, kẽm, nito, natri, canxi.
Câu 5. Biết nguyên tử cacbon có khối lượng bằng 1,9926.10-23 gam. Khối lượng tính bằng gam của nguyên tử Mg bằng bao nhiêu?
Hướng dẫn giải bài tập
Câu 1.
Kim loại nặng nhất trong bảng 1 SKG/42 là Chì kí hiệu là Pb có nguyên tử khối là 207, kim loại nhẹ nhất là liti có nguyên tử khối là 7
Kim loại chì nặng hơn kim loại liti: 207/7 ≈29,57 lần
Câu 2.
Nguyên tử là hạt vô cùng nhỏ và trung hòa về điện
Nguyên tố là những nguyên tử cùng loại, có cùng số proton trong hạt nhân
Câu 3.
2C : 2 nguyên tử cacbon
3Cu: 3 nguyên tử đồng
5Fe: 5 nguyên tử sắt
2H: 2 nguyên tử hidro
O: 1 nguyên tử oxi
Câu 4.
Kí hiệu hóa học chỉ ra: tên nguyên tố, một nguyên tử và nguyên tử khối của nguyên tố đó
Lưu huỳnh: S, sắt: Fe, nhôm: Al, magie: Mg, kẽm: Zn, nito: N, natri: Na, canxi: Ca.
Câu 5.
1đvC có khối lượng = ![]() \(\frac{{1,{{9926.10}^{ - 23}}}}{{12}} = 0,{16605.10^{ - 23}}\)g
\(\frac{{1,{{9926.10}^{ - 23}}}}{{12}} = 0,{16605.10^{ - 23}}\)g
Khối lượng bằng gam của Mg ![]() \(0,{16605.10^{ - 23}} \times 24 = 3,{9852.10^{ - 23}}g\)
\(0,{16605.10^{ - 23}} \times 24 = 3,{9852.10^{ - 23}}g\)
C. Giải bài tập Hóa 8 bài 5 SGK
Để giúp các bạn học sinh có thể hoàn thành tốt các dạng bài tập sách giáo khoa cũng như biết cách vận dụng kiến thức đã học của bài áp dụng vào các dạng bài tập, từ đó rèn luyện kĩ năng thao tác giải bài tập. VnDoc đã biên soạn hướng dẫn giải bài tập hóa 8 sách giáo khoa bài 5 tại
D. Giải sách bài tập hóa 8 bài 5
Ngoài các dạng câu hỏi bài tập sách giáo khoa hóa 8 bài 5, để giúp các bạn học sinh nâng cao củng cố nâng cao kiến thức bài học. Cũng như rèn luyện các thao tác kĩ năng làm bài tập. Các bạn học sinh cần bổ sung làm thêm các câu hỏi bài tập sách bài tập.
Để hỗ trợ bạn đọc trong quá trình học tập cũng như làm bài tập. VnDoc biên soạn hướng dẫn giải chi tiết bài tập SBT hóa 8 bài 5 tại:
E. Trắc nghiệm hóa 8 bài 5
Câu 1: Có bao nhiêu nguyên tố hóa học:
A. Trên 110 nguyên tố
B. Đúng 110 nguyên tố
C. 111 nguyên tố
D. 100 nguyên tố
Câu 2: Kí hiệu của nguyên tố Xeci là
A. Cs
B. Sn
C. Ca
D. B
Câu 3: Khối lượng nguyên tử
A. 1, 9926.10-24 kg
B. 1,9924.10-27g
C. 1,9925.10-25 kg
D. 1,9926.10-27 kg
Câu 4: Nguyên tử của nguyên tố X có nguyên tử khối gấp 7 lần của nguyên tử nguyên tố hidro, đó là nguyên tử nguyên tố nào. Cho biết số p và số e
A. Liti, số p = số e = 3
B. Be, số p = số e = 4
C. Liti, số p = số e = 7
D. Natri, số p = số e = 11
Câu 5: Cho nguyên tố O có nguyên tử khối là 16, Mg là 24. Nguyên tử nào nặng hơn
A. Mg nặng hơn O
B. Mg nhẹ hơn O
C. O bằng Mg
D. Tất cả đáp án trên
Câu 6: Cho nguyên tử của nguyên tố C có 11 proton. Chọn đáp án sai
A. Đấy là nguyên tố Natri
B. Số e là 16 e
C. Nguyên tử khối là 22
D. Số thứ tự trong bảng tuần hoàn là 11
Câu 7: Cho nguyên tử khối của Bari là 137. Tính khối lượng thực nguyên tố trên.
A. mBa = 2,2742.1022 kg
B. mBa = 2,234.10-24 g
C. mBa = 1,345.10-23 kg
D. mBa = 2,7298.10-21g
Câu 8: Chọn đáp án sai
A. Số p là số đặc trưng của nguyên tố hóa học
B. Nguyên tố hóa học là tập hợp những nguyên tố cùng loại, có cùng số p trong hạt nhân
C. 1 đvC = 1/12 mC
D. Oxi là nguyên tố chiếm gần nửa khối lượng vỏ trái đất
Hướng dẫn: nguyên tố hóa học là tập hợp những nguyên tử cùng loại, có cùng số p trong hạt nhân
Câu 9: Cho số khối của nguyên tử nguyên tố X là 39. Biết rằng tổng số hạt nguyên tử là 58. Xác định nguyên tố đó và cho biết số notron
A. Kali, số n = 19
B. Kali, số n = 20
C. Ca, số n = 19
D. Ca, số n = 20
Câu 10: Cho điện tích hạt nhân của X là 15+. Biết rằng số hạt mang điện nhiều hơn không mang điện là 14. Xác định nguyên tố và số khối
A. Nguyên tố P và A = 30
B. Nguyên tố Si và A = 29
C. Nguyên tố P và A = 31
D. Nguyên tố Cl và A = 35,5
Câu 11: 7Cl có ý nghĩa gì?
A. 7 chất Clo
B. 7 nguyên tố Clo
C. 7 nguyên tử Clo
D. 7 phân tử Clo
Câu 12: So sánh nguyên tử canxi (Ca) và nguyên tử sắt (Fe) ta thấy:
A. Nguyên tử Ca nặng hơn nguyên tử Fe 1,4 lần
B. Nguyên tử Fe nặng hơn nguyên tử Ca 1,4 lần
C. Nguyên tử Ca nặng hơn nguyên tử Fe 0,7 lần
D. Nguyên tử Ca nhẹ hơn nguyên tử Fe 0,7 lần
Mời các bạn tải chi tiết câu hỏi trắc nghiệm cũng như đáp án câu hỏi trắc nghiệm Hóa 8 bài 5 tại:
..........................................
Mời các bạn tham khảo thêm một số tài liệu liên quan:
- Giải Hóa 8 Bài 7: Bài thực hành 2
- Bản tường trình hóa học 8 bài thực hành 2
- Giải Hóa 8 Bài 8: Bài luyện tập 1
- Bài tập trắc nghiệm hóa học 8 chương 1 có đáp án
VnDoc giới thiệu tới các bạn Hóa học 8 Bài 5: Nguyên tố Hóa học được VnDoc biên soạn tóm tắt các ý chính trong hóa 8 bài 5 giúp các bạn học sinh dễ dàng soạn bài cũng như nắm chắc kiến thức trọng tâm bài học từ đó vân dụng giải các dạng câu hỏi bài tập.
Trên đây VnDoc đã đưa tới các bạn Hóa học 8 Bài 5: Nguyên tố hóa học. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Chuyên đề Toán 8, Chuyên đề Vật Lý 8, Chuyên đề Hóa 8, Tài liệu học tập lớp 8 mà VnDoc tổng hợp và đăng tải.
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu học tập THCS miễn phí trên Facebook: Tài liệu học tập lớp 8. Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu mới nhất.
