Hóa học 8 Bài 13: Phản ứng hóa học
Hóa học 8 Bài 13: Phản ứng hóa học được VnDoc biên soạn là nội dung bài Hóa 8 bài 13 trong Chương 2, ở bài này sẽ giúp các bạn biết chất có thể biến đổi thành chất khác hay không, quá trình đó được gọi là gì, khi nào thì xảy ra, dựa vào đâu mà biết được.... Bên cạnh đó tài liệu đưa vào các dạng bài tập nhằm củng cố nâng cao kiến thức cho các bạn học sinh.
Phản ứng hóa học
Hy vọng với nội dung lý thuyết hóa 8 bài 13, bạn đọc có thể ghi nhớ kiến thức một cách dễ dàng nhất, từ đó vận dụng giải các dạng câu hỏi bài tập liên quan đến nội dung bài. Mời các bạn tham khảo.
>> Bài trước đó: Hóa học 8 Bài 12: Sự biến đổi chất
I. Tóm tắt nội dung kiến thức
1. Định nghĩa Phản ứng hóa học
Phản ứng hóa học là quá trình biến đổi chất này thành chất khác
- Chất ban đầu bị biến đổi trong phản ứng gọi là chất phản ứng (hay chất tham gia)
- Chất mới sinh ra là sản phẩm.
Phản ứng hóa học được viết theo phương trình chữ như sau:
Tên các chất phản ứng → Tên các sản phẩm
Ví dụ: Khí hidro + oxi → nước
Đọc là: Khí hidro tác dụng với oxi tạo ra nước
Canxi oxit + nước → canxihidroxit
Đọc là: canxi oxit tác dụng với nước sinh ra canxi hidroxit
Trong quá trình phản ứng, lượng chất phản ứng giảm dần, lượng sản phẩm tăng dần.
2. Diễn biến của phản ứng hóa học
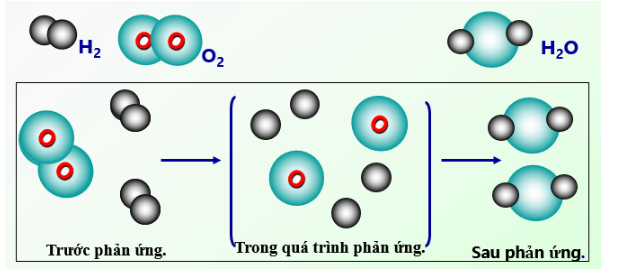
Sơ đồ tượng trưng cho phản ứng hóa học giữa khí hidro và khí oxi tạo thành nước
Quan sát sơ đồ cho ta biết:
- Trước phản ứng: 2 nguyên từ H liên kết với nhau, 2 nguyên tử oxi liên kết với nhau
- Sau phản ứng: 2 nguyên tử H liên kết với 1 nguyên tử O
- Trong quá trình phản ứng: 4 nguyên tử H, 2 nguyên tử O => vẫn giữ nguyên
- Số phân tử trước phản ứng là: một phân tử oxi với 1 phân tử hidro, sau phản ứng số phân tử là 2 phân tử nước.
Kết luận: “Trong phản ứng hóa học chỉ có liên kết giữa các nguyên tử thay đổi làm cho phân tử này biến đổi thành phân tử khác”.
Chú ý: Nếu có đơn chất kim loại tham gia phản ứng thì sau phản ứng nguyên tử kim loại phải liên kết với nguyên tố khác.
3. Khi nào phản ứng hóa học xảy ra?
- Muốn phản ứng hóa học được xảy ra: Các chất tham gia phản ứng phải tiếp xúc với nhau.
Ví dụ: Ta pha nước đường, sử dụng đường cát sẽ dễ tan hơn sử dụng đường phèn. Vì đường cát có diện tích tiếp xúc nhiều hơn đường phèn.
- Một số phản ứng hóa học muốn xảy ra được cần phải đun nóng đến nhiệt độ thích hợp.
- Muốn phản ứng xảy ra cần có mặt chất xúc tác đối với một số phản ứng hóa học.
4. Làm thế nào để nhận biết có phản ứng hóa học xảy ra?
- Dựa vào dấu hiệu có chất mới xuất hiện, có tính chất khác với chất phản ứng.
Ví dụ: Cho vôi sống tác dụng với nước, phản ứng sinh ra nước vôi trong làm quỳ tím chuyển sang màu đỏ.
- Dựa vào màu sắc, trạng thái, tính tan,…
Ví dụ: Khi sục khí cacbonic (CO2) vào dung dịch nước vôi trong ta quan sát được dung dịch bị vẩn đục.
>> Bài tiếp theo tại: Hóa học 8 Bài 14: Bài thực hành số 3
II. Bài tập mở rộng nâng cao
1. Phần câu hỏi tự luận
Câu 1. Ghi lại phương trình bằng chữ của phản ứng hóa học trong các hiện tượng mô tả sau:
a) Cho một mẩu natri vào nước, tu được sản phẩm natri hidroxit NaOH và khí hidro.
b) Cho dung dịch sắt (II) clorua FeCl2 tác dụng với dung dịch bạc nitrat AgNO3, thu được bạc clorua kết tủa màu trắng và dung dịch sắt (II) nitrat.
Hướng dẫn giải bài tập
a) Natri + nước → natri hidroxit + hidro
b) Sắt (II) clorua + bạc nitrat → bạc clorua + sắt (II) nitrat
Câu 2. Viết phương trình hóa học sau: Đốt chát mẩu sắt trong bình đựng khí oxi, tạo ra oxit sắt từ. Xác định chất tham gia và sản phẩm tạo thành?
Hướng dẫn giải bài tập
Sắt + khí oxi → sắt từ oxit
Chất tham gia: sắt và khí oxi
Chất tạo thành: sắt từ oxit
Câu 3. a) Theo em, muốn phản ứng hóa học xảy ra phải có điều kiện gì?
b) Em hãy nêu những yếu tố ảnh hưởng đến tốc độ phản ứng hóa học?
Hướng dẫn giải bài tập
a) Muốn phản ứng hóa học xảy ra:
Những chất tham gia phản ứng phải tiếp xúc với nhau.
Có nhiệt độ thích hợp, có trường hợp cần chất xúc tác.
b) Những yếu tố ảnh hưởng đến tốc độ phản ứng là:
Nhiệt độ của các chất phản ứng: tốc độ phản ứng hóa học tăng khi tăng nhiệt độ và ngược lại.
Thí dụ: Phản ứng phân hủy đá vôi cần đun nóng ở nhiệt độ cao
Độ đậm đặc của dung dịch chất phản ứng: tốc độ phản ứng hóa học tăng nếu độ đậm đặc của dung dịch tăng. Ngược lại
Khi cho một mẩu kẽm vào dung dịch HCl đặc, phản ứng xảy ra nhanh hơn, khi cho mẩu kem tác dụng với dung dịch HCl loãng.
Kích thước của các chất rắn phản ứng: kích thước của các chất rắn càng nhỏ (tức là diện tích tiếp xúc càng lớn) thì tốc độ phản ứng hóa học càng tăng. Ngược lại.
Thí dụ: Phản ứng giữa bột sắt và bột lưu huỳnh xảy ra khi các chất tham gia đều ở dạng bột min làm tăng diện tích tiếp xúc thúc đẩy phản ứng hóa học.
Câu 4. Ghi lại bằng chữ của phương trình phản ứng xảy ra trong hiện tượng mô tả dưới đây?
Cho axit nitric loãng tác dụng với với đinh sắt tạo muối nitrat và khí nito (II) oxit không màu, khí này tiếp xúc với không khí trở thành khí nito (IV) oxit màu nâu đỏ
Hướng dẫn giải bài tập
Kẽm + axit nitric → Muối nitrat + khí nito (IV) oxit
Câu 5. Ghi lại bằng chữ của phương trình phản ứng xảy ra trong hiện tượng mô tả dưới đây?
Lưu huỳnh cháy trong không khí với ngọn lửa nhỏ, màu xanh nhạt. Đưa lưu huỳnh đang cháy vào bình oxi nó cháy mãnh liệt hơn nhiều tạo thành khói màu trắng (chủ yếu lưu huỳnh đioxit (khí sunfuro SO2)
Hướng dẫn giải bài tập
Phương trình hóa học bằng chữ: Lưu huỳnh + oxi → lưu huỳnh đioxit
Phương trình hóa học: S + O2 → SO2
Câu 6. Dấu hiệu để nhận biết xảy ra phản ứng hóa học
Hướng dẫn giải bài tập
Dựa vào dấu hiệu có chất mới xuất hiện, có tính chất khác với chất phản ứng.
Dựa vào màu sắc, trạng thái, tính tan,…
Thí dụ:
Phản ứng cho axit sunfuric đặc tác dụng với đường tạo thành than và nước có sự biến đổi màu từ trắng của đường sang màu đen của than.
Phản ứng giữa bạc nitrat và natri clorua cho sản phẩm là chất rắn màu trắng không tan bạc clorua
Phản ứng giữa (II) sunfua và axit clohidric giải phóng sản phẩm khí hidro sunfua có mùi trứng thối đặc trưng.
Cây nên khi đốt cháy trong không khí đã có phản ứng giữa parafin (thành phần chính của nến) với oxi không khí.
Câu 7. Ghi lại bằng phương trình chữ của phản ứng xảy ra trong thí nghiệm được mô tả dưới đây.
Cho một lá đồng Cu vào bình đựng dung dịch axit nitric HNO3 loãng tạo thành dung dịch muối đồng nitrat có màu xanh đặc trưng và khí nito (II) oxit không màu. Khí này tiếp xúc với khí oix trong không khí tạo thành khí nito (IV) oxit có màu nâu đỏ.
Hướng dẫn giải bài tập
Phương trình phản ứng bằng chữ của phản ứng xảy ra là:
Đồng + axit nitric → đồng nitrat + nito (II) oxit + nước
Nito (II) oxit + oxi → nito (IV) oxit
2. Phần câu hỏi trắc nghiệm Hóa 8 bài 13
Câu 1: Dấu hiệu của phản ứng hóa học
A. Thay đổi màu sắc
B. Tạo chất bay hơi
C. Tạo chất kết tủa
D. Tỏa nhiệt hoặc phát sáng
E. Tất cả đáp án
Câu 2: Trong các quá trình sau, quá trình nào có phản ứng hóa học
(1) Đốt cháy than trong không khí
(2) Làm bay hơi nước muối biển trong quá trình sản xuất muối
(3) Nung vôi
(4) Tôi vôi
(5) I-ot thăng hoa
A.(1), (2), (3)
B. (2), (3), (4), (5)
C. (1), (3), (5)
D. Tất cả đáp án
Câu 3: Phản ứng hóa học là
A. Quá trình kết hợp các đơn chất thành hợp chất
B. Quá trình biến đổi chất này thành chất khác
C. Sự trao đổi của 2 hay nhiều chất ban đầu để tạo chất mới
D. Là quá trình phân hủy chất ban đầu thành nhiều chất
Câu 4: Cho phản ứng giữa khí nito và khí hidro trong điều kiện nhiệt độ thích hợp sinh ra khí amoniac. Chọn đáp án đúng
A. Tỉ lệ giữa khí nitơ và hidro là 1:3
B. Tỉ lệ giữa khí hidrô và nitơ là 1:2
C. Tỉ lệ của nitơ và amoniac là 1:2
D. Không có đáp án đúng
Câu 5: Chọn đáp án đúng
Thả một mảnh sắt vào dung dịch axit clohydric thấy sinh ra khí
A. Khí đó là khí clo
B. Khí cần tìm là khí hidro
C. Thấy có nhiều hơn một khí
D. Không xác định
Câu 6: Chọn đáp án sai
A. Hidro + oxi → nước
B. Canxi cacbonat→ canxi oxit + khí cacbonic
C. Natri + clo → natri clorua
D. Đồng + nước → đồng hidroxit
Câu 7: Khẳng định đúng
Trong 1 phản ứng hóa học, các chất phản ứng và sản phẩm phải chứa
A. Số nguyên tử trong mỗi chất
B. Số nguyên tử mỗi nguyên tố
C. Số nguyên tố tạo ra chất
D. Số phân tử của mỗi chất
Câu 8: Cho kim loại natri (Na) vào khí clo (Cl2). Sản phẩm tạo thành là
A. Sinh ra khí clo
B. Sản phẩm là NaCl2
C. Sinh ra nước muối NaCl
D. Na2Cl
Câu 9: Chọn câu trả lời đúng
A. Sắt + lưu huỳnh thành sắt (II) sunfua
B. Sắt + Clo thành sắt(II) clorua
C. Sắt + lưu huỳnh thành sắt (III) sunfat
D. Sắt + axit clohidric thành sắt (III) clorua
Câu 10: Trong các trường hợp sau, trường hợp không là phương trình hóa học
A. Rượu để trong chai không kín bị cạn dần
B. Sắt cho tác dụng với oxi tạo ra khí SO2
C. Natri cháy trong không khí thành Na2O
D. Tất cả đáp án
Câu 11: Cho phản ứng: Sắt phản ứng với oxi tạo ra oxit sắt từ.
Phương trình hóa học của phản ứng trên là:
A. 2Fe + O2 → 2FeO
B. Fe + O2 → FeO2
C. 4Fe + 3O2 → 2Fe2O3
D. 3Fe + 2O2 → Fe3O4
Câu 12: Khí nitơ tác dụng với khi hidro tạo thành khí amoniac NH3. Phương trình hóa học của phản ứng trên là:
A. N + 3H → NH3
B. N2 + 6H → 2NH3
C. N2 + 3H2 → 2NH3
D. N2 + H2 → NH3
Câu 13: Phát biểu nào sau đây không đúng về phản ứng hóa học?
A. Phản ứng hóa học xảy ra sự thay đổi liên kết giữa các nguyên tử
B. Khi phản ứng hóa học xảy ra, lượng chất tham gia tăng dần theo thời gian phản ứng.
C. Một số phản ứng hóa học cần xúc tác để phản ứng xảy ra nhanh hơn.
D. Chất kết tủa hoặc chất khí bay lên là dấu hiệu thể hiện phản ứng hóa học xảy ra.
Câu 14: Cho sắt vào trong bình đựng khí clo thu được sắt (III) clorua. Tổng hệ số tất cả các chất tham gia phản ứng là:
A. 3
B. 5
C. 7
D. 8
Câu 15: Cho phương trình hóa học
MgO + 2HNO3 → ? + H2O
Công thức hóa học còn thiếu trong dấu ? để hoàn thành phương trình hóa học là:
A. Mg(NO3)2
B. MgNO3
C. Mg(OH)2
D. Mg
Để xem toàn bộ câu hỏi trắc nghiệm cũng như đáp án hướng dẫn giải chi tiết tại: Trắc nghiệm Hóa học 8 bài 13
III. Giải bài tập SGK Hóa 8 bài 13
Để nâng cao rèn luyện, cũng như củng cố lại bài học, sau mỗi bài học sẽ có các dạng bài tập cơ bản giúp các bạn luyện tập. VnDoc đã biên soạn hướng dẫn giải chi tiết các dạng bài tập trong sách giáo khoa tại:
IV. Giải SBT Hóa 8 bài 13
Ngoài các dạng câu hỏi bài tập sách giáo khoa hóa 8 bài 13, để củng cố nâng cao kiến thức bài học cũng như rèn luyện các thao tác kĩ năng làm bài tập. Các bạn học sinh cần bổ sung làm thêm các câu hỏi bài tập sách bài tập. Để hỗ trợ bạn đọc trong quá trình học tập cũng như làm bài tập. VnDoc đã hướng dẫn các ban học sinh giải các dạng bài tập trong Sách bài tập Hóa 8 bài 13 tại Hóa 8 bài 13 tại:
...........................
VnDoc giới thiệu tới các bạn Hóa học 8 Bài 13: Phản ứng hóa học được VnDoc biên soạn. Ở bài 13 hóa 8 này các bạn phải nắm được định nghĩa phản ứng hóa học cũng như điều kiện cách nhận biết một phản ứng hóa học.
Mời các bạn tham khảo một số tài liệu liên quan:
- Hóa học 8 Bài 14: Bài thực hành số 3
- Hóa học 8 Bài 15: Định luật bảo toàn khối lượng
- Giải Hóa 8 Bài 15: Định luật bảo toàn khối lượng
- Bản tường trình hóa học 8 bài thực hành 3
- Trắc nghiệm Hóa học 8 bài 13
Trên đây VnDoc đã gửi tới bạn đọc tài liệu Hóa học 8 Bài 13: Phản ứng hóa học. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Chuyên đề Toán 8, Chuyên đề Vật Lý 8, Chuyên đề Hóa 8, Tài liệu học tập lớp 8 mà VnDoc tổng hợp và đăng tải.
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu học tập THCS miễn phí trên Facebook: Tài liệu học tập lớp 8. Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu mới nhất.
