Hóa học 10 bài 32: Hidro sunfua - Lưu huỳnh (IV) oxit - Lưu huỳnh (VI) oxit
Chuyên đề Hóa học lớp 10: Hidro sunfua - Lưu huỳnh (IV) oxit - Lưu huỳnh (VI) oxit được VnDoc sưu tầm và giới thiệu tới các bạn học sinh cùng quý thầy cô tham khảo. Nội dung tài liệu sẽ giúp các bạn học sinh học tốt môn Hóa học lớp 10 hiệu quả hơn. Mời các bạn tham khảo.
Lý thuyết: Hidro sunfua - Lưu huỳnh (IV) oxit - Lưu huỳnh (VI) oxit
A/ Lý thuyết Hóa học 10 bài 32
1/ Hidro sunfua (H2S)
a/ Tính axit yếu
Hiđro sunfua tan trong nước tạo thành dung dịch axit rất yếu (yếu hơn axit cacbonic), có tên là axit sunfuhiđric (H2S).
Axit sunfuhiđric tác dụng với kiềm tạo nên 2 loại muối: muối trung hòa, như Na2S chứa ion S2- và muối axit như NaHS chứa ion HS−.
b/ Tính khử mạnh
Là chất khử mạnh vì trong H2S lưu huỳnh có số oxi hoá thấp nhất (-2), tác dụng hầu hết các chất ôxihóa tạo sản phẩm ứng với số oxh cao hơn.
Trong hợp chất H2S, nguyên tố lưu huỳnh có số oxi hóa thấp nhất là −2. Khi tham gia phản ứng hóa học, tùy huộc vào bản chất và nồng độ của chất oxi hóa, nhiệt độ,...mà nguyên tố lưu huỳnh có số oxi hóa −2 (S−2) có thể bị oxi hóa thành lưu huỳnh tự do (S0), hoặc lưu huỳnh có số oxi hóa +4 (S+4), hoặc lưu huỳnh có số oxi hóa +6 (S+6). Vì vậy, hiđro sunfua có tính khử mạnh.
Tác dụng với oxi có thể tạo S hoặc SO2 tùy lượng ôxi và cách tiến hành phản ứng.
2H2S + 3O2 ![]() 2H2O + 2 SO2 (dư oxi)
2H2O + 2 SO2 (dư oxi)
2H2S + O2 ![]() 2H2O + 2S
2H2O + 2S
Ở nhiệt độ cao, khí H2S cháy trong không khí với ngọn lửa xanh nhạt, H2S bị oxi hóa thành SO2:
2H2S + 3O2 ![]() 2H2O + 2SO2
2H2O + 2SO2
Tác dụng với clo có thể tạo S hay H2SO4 tùy điều kiện phản ứng
H2S+4Cl2 + 4H2O → 8HCl + H2SO4
H2S +Cl2 → 2 HCl + S (khí clo gặp khí H2S)
Dung dịch H2S có tính axit yếu 2 nấc: Khi tác dụng dung dịch kiềm có thể tạo muối axit hoặc muối trung hòa
H2S + NaOH → NaHS + H2O
H2S + NaOH → Na2S + H2O
*Tính chất của muối sunfua
- Muối sunfua của các kim loại nhóm IA, IIA (trừ Be) như Na2S, K2S tan trong nước và tác dụng với các dung dịch axit HCl, H2SO4 loãng sinh ra khí H2S:
Na2S+2HCl → 2NaCl+H2S↑
- Muối sunfua của một số kim loại nặng như PbS, CuS... không tan trong nước, không tác dụng với dung dịch HCl, H2SO4 loãng.
- Muối sunfua của những kim loại còn lại như ZnS, FeS,... không tan trong nước, nhưng tác dụng với dung dịch HCl, H2SO4 loãng sinh ra khí H2S:
ZnS+2H2SO4 → ZnSO4+H2S↑
- Một số muối sunfua có màu đặc trưng: CdS màu vàng, CuS, FeS, Ag2S,...màu đen.
2/ Lưu huỳnh (IV) oxit
Công thức hóa học SO2 ngoài ra có các tên gọi khác là lƣu huỳnh dioxit hay khí sunfurơ, hoặc anhidrit sunfurơ.
Với số oxi hoá trung gian: +4 (SO2). Khi SO2vừa là chất khử, vừa là chất oxi hóa và là 1 oxit axit.
SO2 là chất khử ( S+4 -2e → S+6)
Khi gặp chất oxi hóa mạnh như O2 , Cl2 , Br2 : khí SO2 đóng vai trò là chất khử.
2 SO2 +O2 → 2SO2
SO2 + Cl2 + 2H2O → 2HCl + H2SO4
5SO2+ 2KMnO4 + 2H2O → K2SO4 + 2MnSO4 + 2 H2SO4
SO2 là chất oxi hoá (S+4 + 4e → So). Khi tác dụng chất khử mạnh:
SO2 + 2H2S → 2H2O + 3S
SO2 + Mg → MgO + S
Ngoài ra SO2 là một oxit axit:
SO2 + NaOH → NaHSO3
SO2 + 2 NaOH → Na2SO3 + H2O
Nếu 1 < nNaOH : nSO2 <2 sản phẩm tạo 2 muối: x mol
NaHSO3 và y mol Na2SO3.
3/ Lưu huỳnh (VI) oxit
SO3: lưu huỳnh trioxit, là 1 oxit axit
Tác dụng với H2O tạo axit sunfuric: SO3 + H2O → H2SO4
SO3 tan vô hạn trong H2SO4 tạo oleum H2SO4.nSO3
Tác dụng với bazo tạo muối
SO3 + 2NaOH → Na2SO4 + H2O
B/ Trắc nghiệm Hóa học 10 bài 32
Câu 1: Phương pháp nào sau đây dùng để điều chế kí sunfuro trong phòng thí nghiệm?
A. Đốt lưu huỳnh trong không khí
B. Cho dung dịch K2SO3 tác dụng với H2SO4 đặc
C. Cho tinh thể K2SO3 tác dụng với H2SO4 đặc
D. Đốt cháy khí H2S trong không khí
Câu 2: Phương trình nào sau đây thể hiện tính khử của SO2?
A. SO2 + NaOH→NaHSO3
B. SO2+ Br2+ 2H2O → H2SO4
C. SO2 + CaO → CaCO3
D. SO2 + 2KOH → K2SO3 + H2O
Câu 3: Phản ứng nào sau đây được dùng để điều chế SO2 trong công nghiệp?
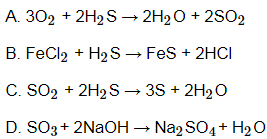
Câu 4: Một mẫu khí thải (H2S, NO2, SO2, CO2) được sục vào dung dịch CuSO4, thấy xuất hiện kết tủa màu đen. Hiện tượng này do chất nào có trong khí thải gây ra?
A. H2S
B. NO2
C. SO2
D. CO2
Câu 5: Thuốc thử nào sau đây dùng để phân biệt khí H2S với khí CO2?
A. Dung dịch HCl
B. Dung dịch Pb(NO3)2
C. Dung dịch K2SO4
D. Dung dịch NaCl
Câu 6: Khí N2 có lẫn tạp chất là H2S và SO2. Có thể dùng dung dịch nào sau đây để loại bỏ H2S và SO2 ra khỏi hỗn hợp?
A. NaCl
B. Pb(NO3)2
C. Ba(OH)2
D. H2SO4
Câu 7: Cho V lít khí SO2 tác dụng với 1lit dung dịch NaOH 0,2M thì thu được 11,5g muối. Giá trị của V là
A. 2,24l
B. 1,87l
C. 4,48l
D. 1,12l
Câu 8: Cho khí H2S lội qua dung dịch CuSO4 thấy có kết tủa màu xám đen xuất hiện, chứng tỏ
A. Có phản ứng oxi hóa- khử xảy ra
B. Có kết tủa CuS tạo thành, không tan trong axit mạnh
C. Axit sunfuric mạnh hơn axit sunfuahidric
D. Axit sunfuahidric mạnh hơn axit sunfuaric
Câu 9: Sục khí H2S vào dung dịch FeCl3, hiện tượng quan sát được
A. Dung dịch trong suốt
B. Kết tủa trắng
C. Khí màu vàng thoát ra
D. Dung dịch mất màu vàng, có hiện tượng vẩn đục
Câu 10: Trường hợp nào sau đây không xảy ra phản ứng hóa học?
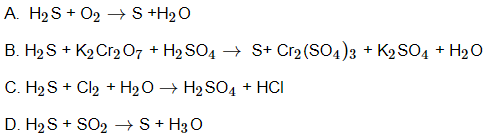
Câu 11: Hòa tan 0,4g SO3 vào a gam dung dịch H2SO4 10% thu được dung dịch H2SO4. Giá trị của a là
A. 19,6
B. 12,65
C. 13,6
D. Kết quả khác
Câu 12: Để oxi hóa cùng một số mol H2S theo các phản ứng dưới đây (chưa cân bằng) thì trường hợp nào khối lượng chất oxi hóa cần dùng là lớn nhất?
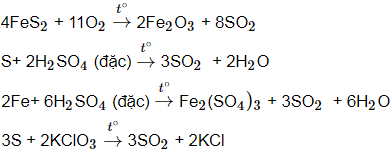
Câu 13: Khí H2S là khí rất độc, để thu được khí H2S thoát ra khi làm thí nghiệm người ta đã dùng:
A. Dung dịch NaCl
B. Nước cất
C. Dung dịch axit HCl
D. Dung dịch NaOH
Câu 14: Chất khí X tan trong nước tạo tành dung dịch làm màu quỳ tím chuyển sang đỏ và có thể được dùng làm chất tẩy màu. Khí X là
A. NH3
B. O3
C. SO2
D. H2S
Câu 15: Dãy chất nào trong các dãy sau đây gồm các chất đều thể hiện tính oxi hóa khi phản ứng với SO2?
A. H2S, O2, nước brom
B. O2, nước brom, dung dịch KMnO4
C. Dung dịch NaOH, O2, dung dịch KMnO4
D. Dung dịch BaCl2, CaO, nước brom
Câu 16: Đốt cháy hoàn toàn 8,96 lít H2S (đktc) rồi cho sản phẩm khí sinh ra vào 80ml dung dịch NaOH 25% (d- 1,28g/ml). Số mol muối tạo thành là
A. Na2SO3 0,24mol và NaHSO3 0,16 mol
B. Na2SO3 0,4 mol
C. Na2SO3 0,16 mol và NaHSO3 0,24 mol
D. NaHSO3 0,08 mol
Câu 17: Thổi SO2 vào 500ml dung dịch Br2 đến khi vừa mất màu hoàn toàn, thu được dung dịch X. Để trung hòa dung dịch X cần 250ml dung dịch NaOH 0,2M. Nồng độ dung dịch Br2 là
A. 0,025M
B. 0,01M
C. 0,02M
D. 0,005M
Câu 18: Phát biểu nào sau đây sai?
A. Ở nhiệt độ thường, H2S là chất khí không màu, có mùi trứng thối, rất độc.
B. Ở nhiệt độ thường, SO2 là chất khí không màu, mùi hắc, tan nhiều trong nước.
C. Ở nhiệt độ thường, SO3 là chất khí không màu, tan vô hạn trong nước.
D. Trong công nghiệp, SO3 là chất khí không màu, tan vô hạn trong nước.
Câu 19: Khí SO2 (sinh ra từ việc đốt các nhiên liệu hóa thạch, quặng sunfua) là một trong những chất gây ô nhiễm môi trường, do SO2 trong không khí sinh ra
A. Mưa axit
B. Hiện tượng nhà kính
C. Lỗ thủng tầng ozon
D. Nước thải gây ung thư
Câu 20: Thể tích khí SO2 (đktc) làm mất màu vừa hết 100ml dung dịch KMnO4 1M là
A. 0,896l
B. 5,6l
C. 2,24l
D. 11,2l
Câu 21: Để nhận biết SO2 và SO3 người ta dùng thuốc thử:
A. Nước Clo
B. Nước vôi trong
C. Dung dịch Brom
D. Tất cả đều không được
Câu 22: Hấp thụ 4,48 lít SO2 (đktc) vào 150 ml dung dịch NaOH 2M, thu được dung dịch chứa m gam muối. Giá trị của m là
A. 18,9
B. 25,2
C. 20,8
D. 23,0
Câu 23: Nung m gam hỗn hợp X gồm FeS và FeS2 trong một bình kín chứa không khí (gồm 20% thể tích O2 và 80% thể tích N2) đến khi các phản ứng xảy ra hoàn toàn, thu được một chất rắn duy nhất và hỗn hợp khí Y có thành phần thể tích: 84,8% N2, 14% SO2, còn lại là O2. Thành phần phần trăm khối lượng của FeS trong hỗn hợp X là
A. 42,31%
B. 59,46%
C. 19,64%
D. 26,83%
Đáp án
| 1C | 2B | 3A | 4A | 5B | 6C | 7A | 8D | 9D | 10B |
| 11A | 12C | 13D | 14C | 15B | 16A | 17C | 18A | 19A | 20B |
| 21C | 22D | 23C |
------------------------------------------
Trong phần chuyên đề trên đây chúng ta có thể hiểu biết thêm về Hidro sunfua - Lưu huỳnh (IV) oxit - Lưu huỳnh (VI) oxit gồm các khái niệm về tính chất vật lý, các phản ứng hóa học, ứng dụng vào thực tế và cách điều chế hidro sunfua...
Như vậy VnDoc đã giới thiệu các bạn tài liệu Lý thuyết Hóa học lớp 10 bài 32: Hidro sunfua - Lưu huỳnh (IV) oxit - Lưu huỳnh (VI) oxit. Mời các bạn tham khảo thêm tài liệu: Trắc nghiệm Sinh học 10, Giải bài tập Sinh học lớp 10, Giải Vở BT Sinh Học 10, Giải bài tập Sinh học 10 ngắn nhất, Tài liệu học tập lớp 10.
Để tiện trao đổi, chia sẻ kinh nghiệm về giảng dạy và học tập các môn học lớp 10, VnDoc mời các thầy cô giáo, các bậc phụ huynh và các bạn học sinh truy cập nhóm riêng dành cho lớp 10 sau: Nhóm Tài liệu học tập lớp 10. Rất mong nhận được sự ủng hộ của các thầy cô và các bạn.
