Tính khử của CO
Chuyên đề Hóa học lớp 11: Tính khử của CO được VnDoc sưu tầm và giới thiệu tới các bạn học sinh cùng quý thầy cô tham khảo. Nội dung tài liệu sẽ giúp các bạn học sinh học tốt môn Hóa học lớp 11 hiệu quả hơn. Mời các bạn tham khảo.
Lý thuyết: Tính khử của Co
I. Phương pháp giải
- CO khử được các oxit kim loại đứng sau Zn trong dãy hoạt động hóa học.
M2On + nCO → 2M + nCO2↑
- Sử dụng định luật bảo toàn nguyên tố C để giải toán kết hợp với định luật bảo toàn khối lượng.
moxit KL + mCO = mKl + mCO2
=> nO (oxit) = nCO = nCO2 và moxit Kl = mKL + mO
Chú ý: Đốt cháy Cacbon bởi oxi: Có 2 trường hợp
+) Nếu thừa oxi: C + O2 → Hỗn hợp khí sau phản ứng gồm CO2 và O2 (dư).
+) Nếu thiếu oxi: C + O2 → Hỗn hợp khí sau phản ứng gồm CO2 và CO dư.
II. Ví dụ
Bài 1: Dẫn một luồng khí CO dư qua ống sứ đựng Fe3O4 và CuO nung nóng đến khi phản ứng hoàn toàn thu được 2,32 gam hỗn hợp kim loại. Khí thoát ra khỏi bình được dẫn qua dung dịch nước vôi trong dư thu được 5 gam kết tủa. Tính tổng khối lượng 2 oxit trong hỗn hợp đầu.
Trả lời
Phương trình phản ứng:
4CO + Fe3O4 to→ 4CO2↑ + 3Fe
CO + CuO to→ CO2↑ + Cu
CO2 + Ca(OH)2 → CaCO3↓ + H2O
nCO2 = nCaCO3 = 5/100 = 0,05 mol
Áp dụng định luật bảo toàn nguên tố C ta có: nCO = nCO2 = 0,05 mol
Áp dụng định luật bảo toàn khối lượng ta có: moxit kl + mCO = mkl + mCO2
=> moxit kl = 2,32 + 0,05.44 – 0,05,28 = 3,12 gam
Bài 2: Khử hoàn toàn 32,20 gam hỗn hợp gồm CuO, Fe2O3 và ZnO bằng CO ở nhiệt độ cao thu được 25,00 gam hỗn hợp X gồm 3 kim loại. Cho X tác dụng vừa đủ với dung dịch HNO3 thì thu được V lít khí NO duy nhất (đktc) và dung dịch chứa m gam muối (không chứa NH4NO3). Tính thể tích khí NO thoát ra và m gam muối thu được
Trả lời
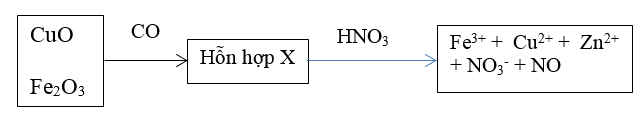 Ta có: nCO = nCO2 = x mol
Ta có: nCO = nCO2 = x mol
Áp dụng định luật bảo toàn khối lượng: moxit kl + mCO = mkl + mCO2
⇔ 32,2 + 28x = 25 + 44x => x = 0,45 mol
Trong quá trình phản ứng chỉ có sự thay đỏi số oxi hóa của C và N.
Phương trình cho nhận e: C+2 - 2e → C+4; N+5 + 3e → N+2
Áp dụng bảo toàn e cho toàn quá trình ta có: 0,45.2 = 3.nNO => nNO = 0,3 mol
Vậy thể tích khí NO thu được là V = 0,3.22,4 = 6,72 lít
nNO3- tạo muối = 3nNO = 0,3.3 = 0,9 mol
Khối lượng muối thu được là m = mkl + mNO3- = 25 + 0,9.62 = 80,8 gam.
Trên đây VnDoc đã giới thiệu tới các bạn lý thuyết Hóa học 11: Tính khử của CO. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Chuyên đề Hóa học 11, Giải bài tập Hóa học lớp 11, Giải bài tập Vật Lí 11, Tài liệu học tập lớp 11 mà VnDoc tổng hợp và đăng tải.
