Bản tường trình Hóa học 8 bài thực hành 4
Hóa học 8 bài thực hành 4 Điều chế - Thu khí oxi và thử tính chất của oxi
Bản tường trình Hóa học 8 bài thực hành 4 được VnDoc biên soạn, trình bày rõ ràng giúp các bạn học sinh nắm được các thao tác làm thí nghiệm bài thực hành. Từ đó đưa ra các nhận xét, giải thích cho câu hỏi bài thực hành. Dưới đây VnDoc trình bày rõ ràng bản tường trình Hóa 8 bài thực hành 4. Mời các bạn tham khảo nhé.
Mời các bạn tham khảo một số tài liệu mới nhất:
- Bản tường trình hóa học 8 bài thực hành 6
- Bản tường trình Hóa học 8 bài thực hành 5
- Đề thi giữa học kì 2 môn Hóa học lớp 8 năm học 2021 - 2022 Đề 1
- Đề thi giữa học kì 2 môn Hóa học lớp 8 năm học 2021 - 2022 Đề 2
A. Báo cáo bản thực hành 4 hóa 8
Họ và tên: ............................................................................... Lớp ........................
Phần I: Phần đánh giá
| Nhận xét | Điểm | ||||
|
Thao tác TN (3đ) |
Kết quả TN (2đ) |
Nội dung tường trình (3đ) |
Chuẩn bị dụng cụ, vệ sinh (2đ) |
Tổng số (10 đ) |
|
Phần II. Phần thực hành
1. Chuẩn bị dung cụ
Chuẩn bị hóa chất: kali penmanganat (thuốc tím), lưu huỳnh
Chuẩn bị dụng cụ: que đóm, ống nghiệm, giá ống nghiệm, kẹp gỗ, đèn cồn, ống dẫn khí, bình thủy tinh có nút, bông, muỗng sắt ....
2. Tiến hành thí nghiệm
Thí nghiệm 1: Điều chế và thu khí oxi
Cách tiến hành:
Lắp dụng cụ như hình vẽ.
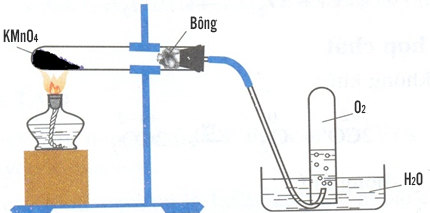
Cho một lượng nhỏ (bằng hạt ngô) KMnO4 vào đáy ống nghiệm. Đặt một ít bồng gần miệng ống nghiệm.
Dùng nút cao su có ống dẫn khí xuyên qua đậy kín ống nghiệm. Đặt ống nghiệm vào giá đỡ hoặc kẹp gỗ sao cho đáy ống nghiệm cao hơn miệng ống nghiệm chút ít.
Nhánh dài của ống dẫn khí sâu gần sát đáy ống nghiệm (hoặc lọ thu).
Dùng đèn cồn đun nóng cả ống nghiệm chứa KMnO4, sau đó tập trung đốt nóng phần có hóa chất. Kali pemanganat bị phân hủy tạo ra khí oxi. Nhận ra khí trong ống nghiệm (2) bằng que đóm còn hồng.
Sau khi kiểm tra độ kín của các nút, đốt nóng ống nghiệm chứa KMnO4. Khí oxi sinh ra sẽ đẩy không khí hoặc đẩy nước và chứa trong ống nghiệm thu. Dùng nút cao su đậy kín ống nghiệm đã chứa đẩy bình oxi để dùng cho thí nghiệm sau.
Hiện tượng:
Chất rắn trong ống nghiệm chuyển dần thành màu đen, tàn đóm đỏ bùng cháy.
Phương trình hóa học
Khi nung KMnO4 ta điều chế được khí oxi theo phản ứng:
2KMnO4 ![]() \(\overset{t^{\circ } }{\rightarrow}\) K2MnO4 + MnO2 + O2
\(\overset{t^{\circ } }{\rightarrow}\) K2MnO4 + MnO2 + O2
Giải thích:
Khi đun nóng kalipemaganat bị phân hủy tạo ra khí oxi.
Vì khí oxi duy trì sự cháy nên làm cho tàn đóm đỏ bùng cháy.
Chất rắn màu đen là MnO2
Thí nghiệm 2: Đốt cháy lưu huỳnh trong không khí và trong khí oxi
Cách tiến hành:
Chuẩn bị dụng cụ như hình 4.1. Cho vào muỗng sắt một lượng nhỏ (bằng hạt đậu xanh) lưu huỳnh S bột.
Đưa muỗng sắt có chứa lưu huỳnh vào ngọn lửa đèn cồn cho lưu huỳnh cháy trong không khí, sau đó đưa lưu huỳnh đang cháy vào lọ (hoặc ống nghiệm) chứa đầy khí oxi.
Hiện tượng:
Trong không khí lưu huỳnh cháy với ngọn lửa nhỏ màu xanh nhạt.
Trong khí oxi lưu huỳnh cháy mãnh liệt hơn.
Tạo ra chất khí mùi hắc là lưu huỳnh đioxit (SO2)
Phương trình hóa học:
S + O2 ![]() \(\overset{t^{\circ } }{\rightarrow}\) SO2
\(\overset{t^{\circ } }{\rightarrow}\) SO2
Giải thích: Vì trong lọ đựng oxi sự tiếp xúc của các phân tử lưu huỳnh với các phân tử oxi nhiều hơn trong không khí nên sự cháy xảy ra mãnh liệt hơn.
Kết luận: Ở nhiệt độ cao oxi dễ dàng phản ứng với phi kim tạo ra oxit axit.
...........................................
B. Nhắc lại nội dung kiến thức liên quan
I. Tính chất của oxi
Oxi là một đơn chất phi kim hoạt động mạnh, đặc biệt là ở nhiệt độ cao, dễ dàng tham gia phản ứng hóa học với nhiều phi kim, nhiều kim loại và hợp chất.
1. Tác dụng với phi kim
S + O2 ![]() \(\overset{t^{o} }{\rightarrow}\) SO2
\(\overset{t^{o} }{\rightarrow}\) SO2
4P + 5O2 ![]() \(\overset{t^{o} }{\rightarrow}\) 2P2O5
\(\overset{t^{o} }{\rightarrow}\) 2P2O5
2. Tác dụng với kim loại
3Fe + O2 ![]() \(\overset{t^{o} }{\rightarrow}\) Fe3O4
\(\overset{t^{o} }{\rightarrow}\) Fe3O4
3. Tác dụng với hợp chất
CH4 + 2O2 ![]() \(\overset{t^{o} }{\rightarrow}\) CO2 + H2O
\(\overset{t^{o} }{\rightarrow}\) CO2 + H2O
II. Điều chế và thu khí oxi
Trong phòng thí nghiệm, oxi được điều chế bằng cách đun nóng những hợp chất giàu oxi và kém bền với nhiệt như KMnO4 và KClO3.
2KClO3 ![]() \(\overset{t^{o} }{\rightarrow}\) 2KCl + 3O2
\(\overset{t^{o} }{\rightarrow}\) 2KCl + 3O2
2KMnO4 ![]() \(\overset{t^{o} }{\rightarrow}\) K2MnO4 + MnO2 + O2
\(\overset{t^{o} }{\rightarrow}\) K2MnO4 + MnO2 + O2
Khí oxi thu dược bằng cách đẩy không khí hay đẩy nước.
C. Chú ý trong quá trình thực hành thí nghiệm Điều chế - Thu khí oxi và thử tính chất của oxi
Trên đây VnDoc đã gửi tới bạn đọc chi tiết nội dung Bản tường trình hóa học 9 bài 14. Nội dung bài thực hành hóa học 8 bài 30 gồm 2 thí nghiệm:
- Thí nghiệm 1: Điều chế và thu khí oxi
- Thí nghiệm 2: Đốt cháy lưu huỳnh trong không khí và trong khí oxi
Để có thể hoàn thành tốt bài thực hành thí nghiệm trên lớp một cách tốt nhất, cũng như biết cách viết báo cáo sau khi thực hành một cách chính xác bạn đọc cần:
Nắm được các nội quy của phòng thí nghiệm, cũng như cách sử dụng, dụng cụ thí nghiệm hóa chất, tránh gây đổ vỡ, mất an toàn. Tuyệt đối tuân theo sự hướng dẫn của giáo viên bộ môn.
Trong quá trình thực hành để thu được kết quả tốt nhất các bạn học sinh cần chú ý:
+ Tập trung quan sát giáo viên bộ môn hướng dẫn
+ Chú ý các thao tác cầm kẹp gỗ, sử dụng giá ống nghiệm, hay cách lấy hóa chất, ....
+ Chuẩn bị đọc bài thật kĩ, trước khi đến lớp.
Mời các bạn tham khảo thêm một số tài liệu:
- Giải Hóa 8 Bài 29: Bài luyện tập 5 Oxi - không khí
- Hóa học 8 Bài 27: Điều chế khí oxi - Phản ứng phân hủy
- Giải Hóa 8 bài 27: Điều chế khí oxi – Phản ứng phân hủy
Trên đây, VnDoc đã gửi tới các bạn Bản tường trình Hóa học 8 bài thực hành 4. Hy vọng đây là tài liệu tham khảo hữu ích giúp các bạn học sinh dễ dàng thực hiện Bản tường trình Hóa học 8 bài thực hành 4.
Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Chuyên đề Toán 8, Chuyên đề Vật Lý 8, Chuyên đề Hóa 8, Tài liệu học tập lớp 8 mà VnDoc tổng hợp và đăng tải.
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu học tập THCS miễn phí trên Facebook: Tài liệu học tập lớp 8. Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu mới nhất.
