Trắc nghiệm Hóa học 8 bài 24
Trắc nghiệm Hóa học 8 có đáp án
Trắc nghiệm Hóa học 8 bài 24 nhằm hỗ trợ quá trình giảng dạy và học tập của quý thầy cô cùng các em đạt kết quả cao, VnDoc biên soạn với nội dung tổng hợp, đa dạng các bài tập Hóa 8 khác nhau trong chương trình học lớp 8.
Bài tập Hóa học 8 bài 24: Tính chất của oxi
Câu 1: Khí oxi nặng hơn không khí bao nhiêu lần
A. 1,1 lần
B. 0,55 lần
C. 0,90625 lần
D. 1,8125 lần
Câu 2: Đốt cháy 3,1g photpho trong bình chứa oxi tạo ra điphotpho pentaoxit. Tính khối lượng oxit thu được
A. 1,3945 g
B. 14,2 g
C. 1,42 g
D. 7,1 g
Câu 3: Cháy mạnh, sáng chói, không có khói là hiện tượng của phản ứng
A. C+O2 → CO2
B. 3Fe+2O2 → Fe3O4
C. 2Cu+O2 → 2CuO
D. 2Zn+O2 → 2ZnO
Câu 4: Cháy trong oxi với lửa nhỏ có màu xanh nhạt, cháy trong không khí mãnh liệt hơn là hiện tượng của phản ứng
A. 2S + 3O2 → 2SO3
B. S + O2 → SO2
C. P + O2 → P2O5
D. P + O2 →P2O5
Câu 5: Cháy mạnh trong oxi với ngọn lửa sáng chói, tạo ra khói trắng dày đặc bám vào thành lọ dưới dạng bột hòa tan được nước là phản ứng
A. 4P + 5O2 → 2P2O5
B. P + O2 → P2O3
C. S + O2 →SO2
D. 2Zn + O2 → 2ZnO
Câu 6: Cho 0,56g Fe tác dụng với 16g oxi tạo ra oxit sắt từ. Tính khối lượng oxit sắt từ và cho biết chất còn dư sau phản ứng
A. Oxi dư và m = 0,67 g
B. Fe dư và m = 0,774 g
C. Oxi dư và m = 0,773 g
D. Fe dư và m = 0,67 g
Câu 7: Tính chất nào sau đây oxi không có
A. Oxi là chất khí
B. Trong các hợp chất, oxi có hóa trị 2
C. Tan nhiều trong nước
D. Nặng hơn không khí
Câu 8: Chọn đáp án đúng
A. Oxi không có khả năng kết hợp với chất hemoglobin trong máu
B. Khí oxi là một đơn chất kim loại rất hoạt động
C. Oxi nặng hơn không khí
D. Oxi có 3 hóa trị
Câu 9: Chọn đáp án đúng
A. CH4 + O2 → 2CO2 + H2O
B. 2C2H2 +5O2→ 4CO2 + 2H2O
C. Ba + O2 → BaO
D. 2KClO3 → 2KCl + O2
Câu 10: Tính thể tích khí oxi phản ứng khi đốt cháy 3,6g C
A. 0,672 l
B. 67,2 l
C. 6,72 l
D. 0,0672 l
Câu 11: Trong 16g khí oxi có bao nhiêu nguyên mol nguyên tử oxi và bao nhiêu mol phân tử oxi?
A. 1 mol nguyên tử oxi và 1 mol phân tử oxi
B. 1 mol nguyên tử oxi và 0,5 mol phân tử oxi
C. 0,5 mol nguyên tử oxi và 1 mol phân tử oxi
D. 0,5 mol nguyên tử oxi và 0,5 mol phân tử oxi
Câu 12: Tỉ khối hơi của oxi với nitơ là:
A. 1,12
B. 1,13
C. 1,14
D. 1,15
Câu 13: Người ta thu khí oxi bằng cách đẩy nước là nhờ dựa vào tính chất.
A. Khí oxi tan trong nước
B. Khí oxi ít tan trong nước
C. Khí oxi khó hóa lỏng
D. Khí oxi nhẹ hơn nước
Câu 14: Cho 0,56g Fe tác dụng với 16 g oxi tạo ra oxit sắt từ. Tính khối lượng oxit sắt từ và cho biết chất còn dư sau phản ứng
A. Oxi dư và m = 0,67 g
B. Fe dư và m = 0,774 g
C. Oxi dư và m = 0,773 g
D. Fe dư và m = 0,67 g
Câu 15: Đâu là tính chất của oxi
A. Không màu, không mùi, ít tan trong nước
B. Không màu, không mùi, tan nhiều trong nước
C. Không màu, có mùi hắc, ít tan trong nước
D. Màu trắng, không mùi, tan nhiều trong nước
Câu 16: Khi đốt cháy mẫu dây sắt trong bình đựng khí oxi, dây sắt cháy mạnh, sáng chói, tạo ra:
A. Các hạt nhỏ nóng chảy màu nâu đỏ là sắt (III) oxit.
B. Các hạt nhỏ nóng chảy màu đỏ là oxit sắt từ.
C. Các hạt nhỏ nóng chảy màu xám là sắt (III) oxit.
D. Các hạt nhỏ nóng chảy màu nâu đen là sắt từ oxit.
Câu 17: Người ta điều chế oxi trong phòng thí nghiệm bằng cách nào sau đây?
A. Chưng cất phân đoạn không khí lỏng.
B. Điện phân nước.
C. Điện phân dung dịch NaOH.
D. Nhiệt phân KClO3 với xúc tác MnO2.
Câu 18: Đốt cháy 6,2 gam P trong bình chứa 6,72 lít khí oxi (đktc) tạo thành P2O5.
a, Chất nào còn dư,chất nào hết?
A. P còn dư, O2 phản ứng hết.
B. P hết, O2 dư.
C. Cả 2 chất vừa đủ.
D. Tất cả đều sai.
Câu 19: Tính số gam kali clorat cầm thiết để điều chế được 48 gam khí oxi?
A. 183,75 gam
B. 122,5 gam
C. 147 gam
D. 196 gam.
Câu 20: Đốt cháy m1 gam kẽm bằng khí oxi vừa đủ, thu được 12,15 gam ZnO. Hòa tan toàn bộ lượng ZnO ở trên vào dung dịch chứa m2 gam HCl vừa đủ thu được sản phẩm là ZnCl2 và nước. Tính m1 + m2
A. 20,7 gam.
B. 10,95 gam.
C. 9,75 gam.
D. 10,35 gam
Đáp án Câu hỏi trắc nghiệm Hóa học 8
| 1.A | 2.D | 3.B | 4.A | 5.A |
| 6.C | 7.C | 8.C | 9.B | 10.C |
| 11.B | 12.C | 13.B | 14.C | 15.A |
| 16. B | 17.D | 18.B | 19.B | 20.A |
Hướng dẫn:
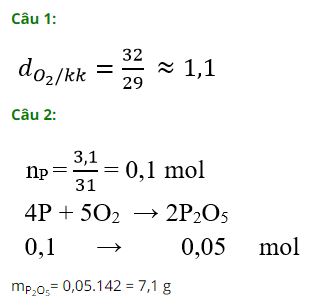

Câu 10: C + O2 → CO2
nC = 3,6/12 = 0,3 mol
nhìn vào phương trình thấy số mol của C bằng số mol oxi phản ứng
⇒ VO2 = 0,3.22,4 = 6,72 l
