KHCO3 là chất gì?
KHCO3 là chất gì? được VnDoc sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy môn Hóa học lớp 8. Hi vọng rằng đây sẽ là những tài liệu hữu ích trong công tác giảng dạy và học tập của quý thầy cô và các bạn học sinh.
Lưu ý: Nếu bạn muốn Tải bài viết này về máy tính hoặc điện thoại, vui lòng kéo xuống cuối bài viết.
KHCO3 là chất gì?
Câu hỏi: KHCO3 là chất gì?
Trả lời:
Kali hiđrocacbonat (công thức phân tử: KHCO3), còn gọi là kali bicacbonat) là một hợp chất muối mặn, không màu, không mùi, có tính bazo.
I. Kali hiđrocacbonat là gì?
Kali hiđrocacbonat (công thức phân tử: KHCO3), còn gọi là kali bicacbonat là một hợp chất muối mặn, không màu, không mùi, có tính bazo.
Công thức hóa học: KHCO3
II. Cấu tạo
- Là muối của kim loại K kết hợp với gốc axit yếu HCO3.
- Công thức cấu tạo:
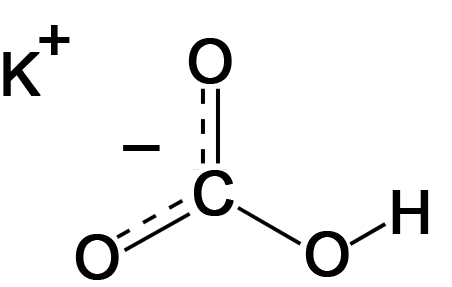
III. Tính chất vật lí
- Là chất ở dạng tinh thể đơn tà màu trắng (tinh thể gồm: ion K+ và ion HCO3-).
- Những ion HCO3- liên kết với nhau bằng liên kết hiđro tạo thành mạch dài.
- Tan nhiều trong nước; độ tan tăng theo nhiệt độ.
IV. Tính chất hóa học
- Muối cacbonat tan tác dụng được với dung dịch bazơ tạo thành bazơ mới và muối mới
KHCO3 + Ba(OH)2 → KOH + BaCO3
- KHCO3 bền ở nhiệt độ thường, đun nóng bị phân hủy tạo muối trung hòa K2CO3:
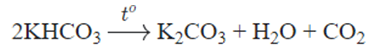
- Ngay trong dung dịch và ở nhiệt độ thường nó cũng bị phân hủy chậm tạo khí CO2; nếu đun nóng thì phân hủy sẽ mãnh liệt hơn.
- Tan trong nước thủy phân cho môi trường kiềm yếu → nhận biết được bằng quỳ tím chuyển xanh và metyl da cam chuyển vàng nhưng không nhận biết được bằng phenolphthalein:
KHCO3 + H2O ⇄ K2CO3 + KOH
- Tác dụng với dung dịch kiềm (NaOH, KOH…) → phản ứng trung hòa.
KHCO3 + KOH → K2CO3 + H2O
2KHCO3 + Ca(OH)2 → K2CO3 + CaCO3 + H2O
KHCO3 + Ca(OH)2 → KOH + CaCO3 + H2O
- Phản ứng của 2 muối axit với nhau: (muối axit mạnh sẽ đóng vai trò là axit; muối axit yếu sẽ đóng vai trò là bazơ)
KHSO4 + KHCO3 → K2SO4 + CO2 + H2O
- Tác dụng với axit: (muối của axit yếu phản ứng với axit mạnh tạo ra muối mới + axit yếu hơn)
HCl + KHCO3 → KCl + CO2 + H2O
H2SO4 + 2KHCO3 → K2SO4 + 2CO2 + 2H2O
- Tác dụng với muối:
KHCO3 + AlCl3 + H2O → KCl + CO2 + Al(OH)3
KHCO3 + FeCl3 + H2O → Fe(OH)3 + KCl + CO2
- Tác dụng với oxit axit:
KHCO3 + SO2 → KHSO3 + CO2
V. Điều chế
Phương trình điều chế KHCO3
K2CO3 + Ba(HCO3)2 ⟶ BaCO3 + 2KHCO3
KCl + NH4HCO3 ⟶ NH4Cl + KHCO3
H2O + K2CO3 + CO2 ⟶ 2KHCO3
VI. Ứng dụng
- Sử dụng làm men trong làm bánh,; chất trong bình chữa cháy; dùng làm thuốc thử và chất đệm mạnh trong dược phẩm.
- Sử dụng làm chất phụ gia trong sản xuất rượu vang và điều chỉnh độ pH của rượu.
- Dùng làm thuốc diệt nấm mốc, vảy tảo trong canh tác hữu cơ.
- Dùng để trung hòa đất nhiều axit.
VII. Nhận biết
- Thuốc thử: dung dịch chứa ion Ca2+ hoặc chứa ion Ba2+ như: BaCl2; Ca(OH)2…
- Hiện tượng: thấy xuất hiện kết tủa trắng là CaCO3 (với thuốc thử chứa ion Ca2+) hoặc BaCO3 (với thuốc thử chứa ion Ba2+).
- PTHH minh họa:
2KHCO3 + Ca(OH)2 → K2CO3 + CaCO3 + H2O
-------------------------------------------
Như vậy VnDoc đã giới thiệu các bạn tài liệu KHCO3 là chất gì? Mời các bạn tham khảo thêm tài liệu: Chuyên đề Hóa học 8, Giải bài tập Hóa học 8, Giải SBT Hóa 8, Trắc nghiệm Hóa học 8, Tài liệu học tập lớp 8
