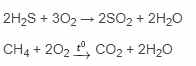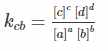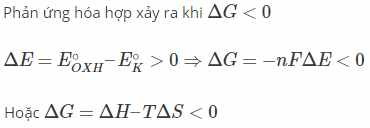Phản ứng hóa hợp là gì?
Chúng tôi xin giới thiệu bài Phản ứng hóa hợp là gì? được VnDoc sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy môn Hóa học lớp 8. Hi vọng rằng đây sẽ là những tài liệu hữu ích trong công tác giảng dạy và học tập của quý thầy cô và các bạn học sinh.
Lưu ý: Nếu bạn muốn Tải bài viết này về máy tính hoặc điện thoại, vui lòng kéo xuống cuối bài viết.
Phản ứng hóa hợp là gì?
Câu hỏi: Phản ứng hóa hợp là gì?
Trả lời:
Phản ứng hóa hợp là phản ứng hóa học trong đó có một chất mới được tạo thành từ hai hay nhiều chất ban đầu.
Ví dụ: 2Na+Cl2 → 2NaCl
4Fe+3O2 → 2Fe2O3
Ví dụ phản ứng không phải là phản ứng hóa hợp (do có hai chất mới được tạo thành).
1. Phản ứng hóa hợp là gì?
Phản ứng hóa hợp là một phản ứng hóa học trong đó chỉ có một chất mới (Sản phẩm) được tạo thành tự hai hay nhiệt chất ban đầu.
Ví dụ phản ứng hóa hợp.
C + O2 → CO2
N2 + H2 → NH3
P + O2 → P2O5
Zn + O2 → ZnO
Ca + O2 → CaO
Nhận xét: Những phản ứng trên đều là phản ứng hóa học và các em có thể quan sát được ngay vế chất tham gia có 2 chất và vế sản phẩm đều có 1 chất duy nhất tạo thành mà thôi. Do đó, chúng ta gọi những phản ứng trên là phản ứng hóa hợp.
Nói một cách khác phản ứng hóa hợp là một phản ứng hóa học và hợp nhất các chất lại với nhau.
Lưu ý: Trong phản ứng hóa học khi xét về vấn đề nhiệt độ có 3 phản ứng dưới đây:
- Phản ứng tỏa nhiệt.
- Phản ứng đẳng nhiệt.
- Phản ứng hấp thụ nhiệt.
Trong những kiểu phản ứng trên chúng ta sẽ thường gặp nhiều nhất phản ứng tỏa nhiệt. Có một số ví dụ như khi cho kim loại Natri, Kali, Ba, Ca... tác dụng với oxi ở nhiệt độ thường và sẽ tỏa nhiệt. Nhưng đối với các phản ứng của các kim loại Mg, Fe, Cu... khi tác dụng với oxi thì cần thêm nhiệt độ để kích thích phản ứng xảy ra. Tuy nhiên, khi xảy ra phản ứng thì chúng lại tỏa nhiệt mạnh nên ta vẫn gọi đó là những phản ứng tỏa nhiệt.
2. Cách xác định phản ứng hóa hợp.
Để xác định đâu là một phản ứng hóa hợp chúng ta chỉ cần quan tâm tới vế sản phẩm. Khi vế sản phẩm có 1 chất duy nhất được tạo thành thì ta gọi đó là một phản ứng hóa hợp. Một cách tổng quát giúp các em nhìn rõ hơn như sau:
A + B + C → AxByCz
3. Đặc điểm phản ứng hóa hợp
Phản ứng hóa hợp có thể có sự thay đổi số oxi hóa hoặc không thay đổi số oxi hóa tùy vào bản chất chất tham gia.
Phản ứng kết thúc khi:
- Một trong các chất tham gia phản ứng hết
- Cân bằng hóa học được thiết lập:
4. Điều kiện xảy ra phản ứng hóa hợp
Điều kiện
Môi trường
Chất xúc tác: một số phản ứng hóa hợp muốn xảy ra hoặc xảy ra nhanh thì cần phải có chất xúc tác:
Ví dụ: 2Al + 3I2 → H2O → 2AlI3
Nồng độ: hàm lượng, nồng độ các chất càng lớn thì pư xảy ra càng nhanh.
5. Phân loại phản ứng hóa hợp
Phản ứng hóa hợp có sự thay đổi số oxi hóa
- Đơn chất + Đơn chất → Hợp chất
- Kim loại điển hình + Phi kim điển hình → Hợp chất ion
4Al + 3O2 → 2Al2O3
- Phi kim + Phi kim → Hợp chất cộng hóa trị
S+O2→SO2
- Đơn chất + Hợp chất → Hợp chất cộng hóa trị
H2 + C2H4 → C2H6
- Hợp chất + Hợp chất → Hợp chất cộng hóa trị
C2H4 + H2O → C2H5OH
Phản ứng hóa hợp không có sự thay đổi số oxi hóa
- Oxit bazơ + Oxit axit → Muối
CaO + CO2 → CaCO3
- Oxit bazơ + Nước → Bazơ
Na2O + H2O→2NaOH
- Oxit axit + Nước → Axit
SO3+H2O → H2SO4
- Oxit axit + Bazơ → Muối axit
SO2 + KOH → KHSO3
- Amoniac + Axit → Muối amoni
NH3 + H2SO4 → (NH4)2SO4
- Phản ứng tạo phức chất
Al2O3 + 2NaOH + 3H2O → 2Na[Al(OH)4]
6. Một số phản ứng hóa hợp trong tự nhiên
Phản ứng quang hợp
- Quang hợp vốn là quá trình trong đó năng lượng ánh sáng Mặt Trời được diệp lục trong lục lạp hấp thụ để tạo ra cacbonhiđrat và ôxi từ khí cacbonic và nước.
- Quang hợp là một quá trình oxi hóa khử trong đó H2O bị oxi hóa và CO2 bị khử.
- Phương trình tổng quát về quang hợp: 6CO2 + 12H2O → C6H12O6 + 6O2
Phản ứng ăn mòn đá vôi
Đá dùng trong xây dựng ít bị phá hoại do tải trọng thiết kế mà thường bị phá hoại do ăn mòn. Sự phá hoại do một số nguyên nhân chính như sau :
- Môi trường nước chứa hàm lượng khí cacbonic lớn (hơn 35mg/l) sẽ xảy ra phản ứng hóa học:
CaCO3 + H2O + CO2 → Ca(HCO3)2, Ca(HCO3)2 là hợp chất dễ tan nên dần dần đá bị ăn mòn.
- Môi trường nước có chứa các loại axit cũng xảy ra phản ứng hóa học
CaCO3 + 2HCl → CaCl2 + CO2 + H2O.
Các dạng ăn mòn trên thường xảy ra đối với các loại đá cacbonat.
- Đá có chứa nhiều thành phần khoáng vật khác nhau thì đá cũng có thể bị phá hoại nhanh hơn do sự giãn nở nhiệt không đều.
- Các loại bụi bẩn nguồn gốc vô cơ và hữu cơ từ các chất thải công nghiệp hoặc đời sống tích tụ trên bề mặt hoặc trong các lỗ rỗng của đá là môi trường để cho vi khuẩn phát triển và phá hoại đá bằng chính axit của chúng tiết ra.
Phản ứng tạo gỉ sắt
- Trong không khí ẩm, sắt bị ăn mòn theo phản ứng: 4Fe + 3O2 + 2nH2O → 2Fe2O3.nH2O
- Phản ứng này tạo thành gỉ sắt có màu nâu đỏ
- Gỉ sắt này có cấu trúc mềm và xốp, do đó chúng dễ dàng hấp thụ nước và sắt bên trong tiếp tục bị ăn mòn và nhanh chóng vị rã nát.
-------------------------------------------
Như vậy VnDoc đã giới thiệu các bạn tài liệu Phản ứng hóa hợp là gì? Mời các bạn tham khảo thêm tài liệu: Chuyên đề Hóa học 8, Giải bài tập Hóa học 8, Giải SBT Hóa 8, Trắc nghiệm Hóa học 8, Tài liệu học tập lớp 8