Thể tích mol của chất khí là gì?
Thể tích mol của chất khí là gì? được chúng tôi sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy môn Hóa học lớp 8. Hi vọng rằng đây sẽ là những tài liệu hữu ích trong công tác giảng dạy và học tập của quý thầy cô và các bạn học sinh.
Lưu ý: Nếu bạn muốn Tải bài viết này về máy tính hoặc điện thoại, vui lòng kéo xuống cuối bài viết.
Thể tích mol của chất khí là gì?
Câu hỏi: Thể tích mol của chất khí là gì?
Trả lời:
- Thể tích mol của chất khí là thể tích chiếm bởi N phân tử của chất khí đó.
- Một mol của bất kì chất khí nào trong cùng điều kiện về nhiệt độ và áp suất đều chiếm những thể tích bằng nhau.
Ví dụ:
Thể tích của 1 mol khí hiđro bằng thể tích 1 mol khí oxi bằng thể tích 1 mol khí nitơ (nếu các khí ở cùng một điều kiện).
- Nếu ở nhiệt độ 0oC và áp suất là 1 atm gọi là điều kiện tiêu tiêu chuẩn (đktc) thì 1 mol chất khí có thể tích là 22,4 lít.
- Nếu ở nhiệt độ 20oC và áp suất 1 atm thì 1 mol chất khí có thể tích là 24 lít.
I. Mol là gì?
- Mol là lượng chất chứa 6,02.10 nguyên tử hoặc phân tử chất đó.
- Con số 6,02.10 được gọi là số Avogađro và được kí hiệu là N.
*Ví dụ: 1 mol nguyên tử vàng là một lượng vàng có chứa N nguyên tử Au 1 mol nguyên tử bạc là một lượng bạc có chứa N nguyên tử Ag. 1 mol phân tử nước là một lượng nước có chứa N phân tử H O.
→ Nhận xét: Nếu biết số mol ta có thể tính được số phân tử hoặc số nguyên tử.
*Ví dụ: Hãy tính số nguyên tử Cu có trong 2 mol Cu. Ta thấy: Cứ 1 mol Cu có 6,02.10 nguyên tử Cu ⇒ 2 mol Cu có: 2.6,02.10 nguyên tử Cu.
Lưu ý: Phân biệt ý nghĩa của 2 cách viết sau
- 1 mol H nghĩa là chỉ 1 mol nguyên tử Hidro
- 1 mol H2 nghĩa là chỉ 1 mol phân tử Hidro
II. Thể tích mol của chất khí có công thức như thế nào?
Thể tích mol của chất khí định nghĩa là gì?
Thể tích mol phân tử của một chất khí chính là thể tích của 1 mol phân tử của chất khí đó. Hay nói đơn giản là, thể tích mol của chất khí là thể tích chiếm bởi NA phân tử chất đó.
Một mol của bất kỳ chất khí nào, trong cùng đặt trong cùng điều kiện nhiệt độ áp suất đều chiếm thể tích bằng nhau. Quy ước ở t = 0°C và P = 1 atm (điều kiện tiêu chuẩn ) thì 1 mol khí bất kì nào cũng có thể tích là 22,4 lít.
Ta có ví dụ sau: Ta ví dụ sau 1 mol khí H2 hoặc 1 mol khí O2 hay bất kì khí nào thì đều chiếm thể tích 22,4 lít.
Công thức tính mol chất khí xét ở điều kiện tiêu chuẩn (đktc)
Để tính số mol chất khí (đktc) thông qua thể tích ta có công thức:
Trong đó:
+ n: số mol chất khí (mol)
+ V: thể tích chất khí ở điều kiện tiêu chuẩn (lít)
Đối với các chất khí ở điều kiện tự nhiên ( không ở điều kiện tiêu chuẩn), thì công thức này không còn áp dụng để tính toán nữa. Ta sử dụng công thức sau để tính số mol chất khí không trong điều kiện tiêu chuẩn:
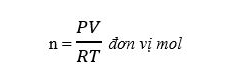
Trong đó:
+ P là Áp suất (atm)
+ V là thể tích chất khí (lít)
+ R = 0.082
+ T = 273 + t độ C.
III. Bài tập vận dụng
Bài 1: Hãy tính thể tích của 8g khí oxi ở đktc?
Hướng dẫn giải:
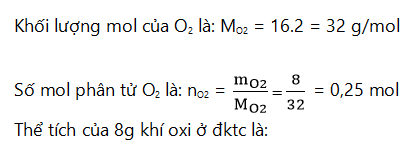
VO2 = nO2 . 22,4 = 0,25.22,4 = 5,6 lít.
Bài 2: Tính khối lượng của 8,96 lít khí CO2 ở đktc?
Hướng dẫn giải:
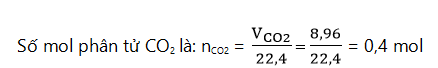
Khối lượng mol của CO2 là: MCO2 = 12 +16.2 = 44 g/mol
Khối lượng của 8,96 lít khí CO2 ở đktc là:
mCO2 = nCO2.MCO2 = 0,4.44 = 17,6 gam.
Bài 3: Một hỗn hợp khí X gồm 0,25 mol khí SO2 và 0,15 mol khí CO2
a) Tính thể tích của hỗn hợp khí X (đktc).
b) Tính khối lượng của hỗn hợp khí X.
Hướng dẫn giải:
a) Thể tích của hỗn hợp khí X (đktc) là:
VX = nX.22,4 = (0,25 + 0,15).22,4 = 8,96 lít
b) MCO2= 32+2.16 = 64 g/mol
Khối lượng của 0,25 mol khí SO2 là: mCO2 = nCO2.MCO2 = 0,25.64 = 16g.
MCO2 = 12+2.16 = 44 g/mol
Khối lượng của 0,15 mol khí CO2 là: mCO2 = nCO2.MCO2 = 0,15.44 = 6,6g.
Khối lượng của hỗn hợp khí X là: mX = mCO2 + mCO2 = 16 +6,6 = 22,6g.
-------------------------------------------