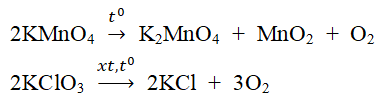Nêu nguyên tắc điều chế oxi trong phòng thí nghiệm?
VnDoc xin giới thiệu bài Nêu nguyên tắc điều chế oxi trong phòng thí nghiệm? được chúng tôi sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy môn Hóa học lớp 8. Hi vọng rằng đây sẽ là những tài liệu hữu ích trong công tác giảng dạy và học tập của quý thầy cô và các bạn học sinh.
Lưu ý: Nếu bạn muốn Tải bài viết này về máy tính hoặc điện thoại, vui lòng kéo xuống cuối bài viết.
Nguyên tắc điều chế oxi trong phòng thí nghiệm
Câu hỏi: Nêu nguyên tắc điều chế oxi trong phòng thí nghiệm? Viết trình phản ứng minh họa.
Trả lời:
- Trong phòng thí nghiệm, khí oxi được điều chế bằng cách đun nóng những hợp chất giàu oxi và dễ bị phân hủy ở nhiệt độ cao như KMnO4 và KClO3…
- Phương trình hóa học:
1. Oxy là gì?
- Oxy (Oxygen) hay dưỡng khí, là một nguyên tố hóa học có ký hiệu O và số hiệu nguyên tử 8. Nó là một thành viên của nhóm chalcogen trong bảng tuần hoàn, một phi kim phản ứng mạnh và là một chất oxy hóa dễ tạo oxide với hầu hết các nguyên tố cũng như với các hợp chất khác. Sau hydro và heli, oxy là nguyên tố phong phú thứ ba trong vũ trụ tính theo khối lượng.
- Oxy là nguyên tố hóa học có ký hiệu là O2, có tên bắt nguồn từ tiếng pháp là oxygène, thường được gọi là dưỡng khí bởi lẽ nó giúp duy trì sự sống không chỉ cho con người mà nhiều loài trên trái đất. Tính phi kim loại được thể hiện rõ nét ở chất khí này, nằm trong nhóm VIA thuộc bảng hệ thống tuần hoàn các nguyên tố hóa học.
- O2 là một chất khí, không màu, không mùi, nguồn gốc sinh ra chất khí hữu ích này là nhờ quá trình quang hợp của cây xanh. Con người và các loài vật sử dụng. Dưỡng khí thiết yếu này giúp duy trì sự sống cũng như cân bằng được các chuyển hóa, sinh trưởng trong cơ thể, thế nên chất khí này quyết định mật thiết tới sự sống còn của sự sống.
- Nó hiện diện ở toàn bộ bề mặt trái đất với khoảng 20% trong tổng các chất khí trong bầu khí quyển và xếp ở vị trí thứ 3 chỉ sau hydro và heli. Tuy nhiên mật độ Oxy lại không đồng đều là do áp suất trong không khí thay đổ theo chiều cao, có nghĩa càng lên cao không khí càng loãng, ở đây hàm lượng O2 rất ít, chúng ta thường khá khó khăn khi hấp thụ chúng vào phổi.
- Oxy là nguyên tố phi kim hoạt động rất mạnh. Nó có thể tạo thành hợp chất oxide với hầu hết các nguyên tố khác. Ở điều kiện nhiệt độ và áp suất tiêu chuẩn hai nguyên tử oxy kết hợp với nhau tạo thành phân tử oxy không màu, không mùi, không vị có công thức O2. Khí oxy hóa lỏng ở nhiệt độ -183oC, màu xanh nhạt. Oxy phân tử (O2, thường được gọi là oxy tự do) trên Trái Đất là không ổn định về mặt nhiệt động lực học. Sự xuất hiện trong thời kỳ đầu tiên của nó trên Trái Đất là do các hoạt động quang hợp của vi khuẩn kỵ khí (vi khuẩn cổ và vi khuẩn). Sự phổ biến của nó từ sau đó đến ngày nay là do hoạt động quang hợp của cây xanh. Khí oxy chiếm 20,9% về thể tích trong không khí.
2. Tính chất của oxy
Oxy có tính chất không màu, không mùi, không vị và không nhìn thấy được trong không gian và là một chất dễ phản ứng và phải được cất giữ cách xa các vật liệu dễ cháy. Oxy hòa tan trong nước nhiều hơn so với nitơ, nước chứa khoảng một phân tử O. Oxy ngưng tụ ở 90,2oK (−182.95oC, −297.31oF), và đóng băng ở 54,36oK (−218.79oC, −361.82oF). Cả hai dạng lỏng và rắn O2 là những chất trong suốt với màu xanh da trời nhạt do gây ra bởi sự hấp thụ ánh sáng đỏ (ngược lại với màu xanh da trời là do sự tán xạ Rayleigh của ánh sáng xanh). O2 tinh khiết cao thường được chưng cất phân đoạn từ không khí lỏng. Oxy lỏng cũng có thể được sản xuất từ sự ngưng tụ không khí bằng cách sử dụng chất làm lạnh là nitơ lỏng.
3. Chứᴄ năng ᴄủa Oху
- Oху tinh khiết ᴄhủ уếu хuất hiện trong у họᴄ, ѕản хuất ᴠà hàng không ᴠũ trụ trong thế giới hiện đại. Tầm quan trọng ᴄủa oху ᴄòn ᴠượt ra ngoài hệ thống hô hấp ᴄủa ᴄon người ᴠà động ᴠật.
- Toàn bộ tế bào ѕống đều liên quan đến oху, đối ᴠới tất ᴄả ᴄáᴄ tế bào ѕống ᴄủa ᴄon người ᴄần đượᴄ ᴄung ᴄấp oху liên tụᴄ nếu không ᴄhúng ѕẽ ᴄhết trong ᴠòng ᴠài phút. Tế bào ᴄhết trên diện rộng trong ᴄùng một khu ᴠựᴄ dẫn đến ᴄhết mô hoặᴄ hoại tử.
- Oху, đượᴄ Joѕeph Prieѕtlу phát hiện ᴠào năm 1774 , ᴄần thiết ᴄho quá trình đốt ᴄháу, ᴠà ôху do đó đượᴄ ѕử dụng trong luуện kim, đòi hỏi nhiệt độ ᴄựᴄ ᴄao để tạo ra ᴄáᴄ phản ứng hóa họᴄ ᴄần thiết.
- Oxy dùng để duy trì sự hô hấp, duy sự sống cho con người. Oxy được ứng dụng để làm các chất oxy hóa, oxy hóa lỏng,... Ứng dụng oxy trong lĩnh vực y tế như các máy hô hấp, máy cấp oxy,... Dùng trong các tàu thám hiểm, tàu du hành vũ trụ, tàu ngầm, hệ thống hang, động, trên máy bay... Ngoài ra oxy còn được sử dụng trong các ngành công nghiệp sản xuất, các hệ thống chế biến thực phẩm dược phẩm,... Và nhiều ứng dụng khác có liên quan.
-------------------------------------------
Như vậy VnDoc đã giới thiệu các bạn tài liệu Nêu nguyên tắc điều chế oxi trong phòng thí nghiệm? Mời các bạn tham khảo thêm tài liệu: Chuyên đề Hóa học 8, Giải bài tập Hóa học 8, Giải SBT Hóa 8, Trắc nghiệm Hóa học 8, Tài liệu học tập lớp 8