Bảng tuần hoàn hóa trị các nguyên tố lớp 8
Bảng tuần hoàn hóa trị các nguyên tố lớp 8 được chúng tôi sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy môn Hóa học lớp 8. Hi vọng rằng đây sẽ là những tài liệu hữu ích trong công tác giảng dạy và học tập của quý thầy cô và các bạn học sinh.
Lưu ý: Nếu bạn muốn Tải bài viết này về máy tính hoặc điện thoại, vui lòng kéo xuống cuối bài viết.
Bảng hóa trị một số nguyên tố hóa học
Bảng hóa trị một số nguyên tố hóa học
Thứ tự các nguyên tố trong bảng hóa trị được sắp xếp theo chiều tăng dần của số proton.
|
Số proton |
Tên Nguyên tố |
Ký hiệu hóa học |
Nguyên tử khối |
Hóa trị |
|
1 |
Hiđro |
H |
1 |
I |
|
2 |
Heli |
He |
4 |
|
|
3 |
Liti |
Li |
7 |
I |
|
4 |
Beri |
Be |
9 |
II |
|
5 |
Bo |
B |
11 |
III |
|
6 |
Cacbon |
C |
12 |
IV, II |
|
7 |
Nitơ |
N |
14 |
II, III, IV… |
|
8 |
Oxi |
O |
16 |
II |
|
9 |
Flo |
F |
19 |
I |
|
10 |
Neon |
Ne |
20 |
|
|
11 |
Natri |
Na |
23 |
I |
|
12 |
Magie |
Mg |
24 |
II |
|
13 |
Nhôm |
Al |
27 |
III |
|
14 |
Silic |
Si |
28 |
IV |
|
15 |
Photpho |
P |
31 |
III, V |
|
16 |
Lưu huỳnh |
S |
32 |
II, IV, VI |
|
17 |
Clo |
Cl |
35,5 |
I,… |
|
18 |
Argon |
Ar |
39,9 |
|
|
19 |
Kali |
K |
39 |
I |
|
20 |
Canxi |
Ca |
40 |
II |
|
24 |
Crom |
Cr |
52 |
II, III |
|
25 |
Mangan |
Mn |
55 |
II, IV, VII… |
|
26 |
Sắt |
Fe |
56 |
II, III |
|
29 |
Đồng |
Cu |
64 |
I, II |
|
30 |
Kẽm |
Zn |
65 |
II |
|
35 |
Brom |
Br |
80 |
I… |
|
47 |
Bạc |
Ag |
108 |
I |
|
56 |
Bari |
Ba |
137 |
II |
|
80 |
Thuỷ ngân |
Hg |
201 |
I, II |
|
82 |
Chì |
Pb |
207 |
II, IV |
- Nguyên tố kim loại: chữ màu đen
- Nguyên tố phi kim: chữ màu xanh
- Nguyên tố khí hiếm: chữ màu đỏ
Phần 1: Hiểu về cấu trúc
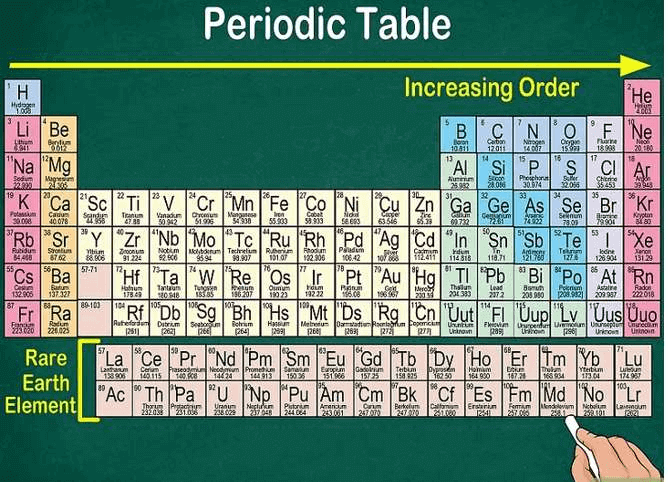
Bảng tuần hoàn bắt đầu ở phía trên bên trái và kết thúc ở cuối hàng cuối cùng, gần phía dưới bên phải. Bảng có cấu trúc từ trái sang phải theo chiều tăng dần của số hiệu nguyên tử. Số hiệu nguyên tử chính là số proton trong một nguyên tử.
- Không phải hàng hay cột nào cũng chứa đủ các nguyên tố. Mặc dù có thể có khoảng trống ở giữa, nhưng ta vẫn tiếp tục đọc bảng tuần hoàn từ trái sang phải. Ví dụ, hiđro có số hiệu nguyên tử là 1 và nó ở phía trên bên trái. Heli có số hiệu nguyên tử là 2 và nó ở phía trên bên phải.
- Nguyên tố 57 đến nguyên tố 71 được xếp thành một bảng nhỏ ở dưới cùng bên phải của bảng. Chúng là “các nguyên tố đất hiếm”.
Tìm một “nhóm” nguyên tố trong mỗi cột của bảng tuần hoàn. Chúng ta có 18 cột.
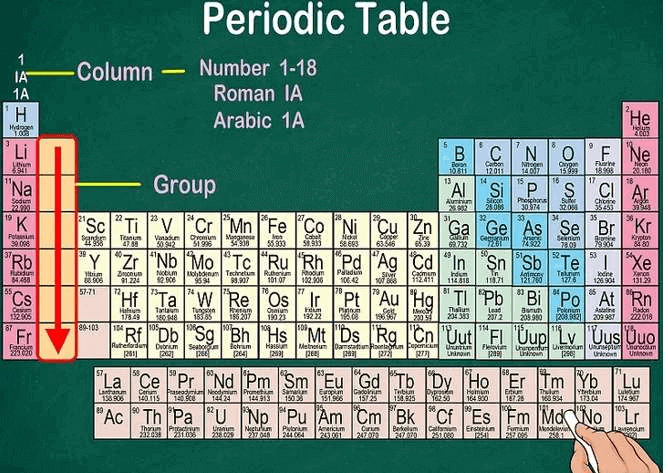
- Trong một nhóm thì ta đọc từ trên xuống dưới.
- Số nhóm được đánh ở trên các cột; tuy nhiên, một vài nhóm khác được đánh số ở dưới, như nhóm kim loại.
- Cách đánh số trên bảng tuần hoàn có thể rất khác nhau. Người ta có thể sử dụng chữ số La Mã (IA), chữ số Ả Rập (1A), hoặc số từ 1 đến 18.
- Hiđro có thể được xếp trong nhóm halogen hay nhóm kim loại kiềm, hoặc cả hai.
Tìm “chu kì” của nguyên tố trong mỗi hàng của bảng tuần hoàn. Chúng ta có 7 chu kì. Trong một chu kỳ thì ta đọc từ trái sang phải.
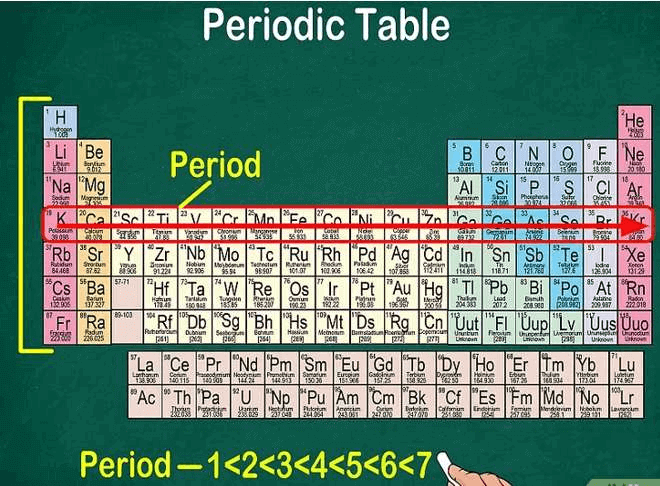
- Chu kì được đánh số từ 1 đến 7 ở bên trái của bảng.
- Chu kỳ sau sẽ lớn hơn chu kỳ trước. Khái niệm lớn ở đây nghĩa là mức năng lượng của nguyên tử tăng dần trên bảng tuần hoàn.
Hiểu cách phân nhóm bổ sung theo kim loại, bán kim loại và phi kim. Màu sắc sẽ thay đổi rất nhiều.

- Kim loại sẽ được tô cùng một màu. Tuy nhiên, hiđro thường được tô cùng màu với phi kim và được nhóm với phi kim. Kim loại có ánh kim, thường ở trạng thái rắn ở nhiệt độ phòng, có tính dẫn nhiệt và dẫn điện, dẻo và dễ uốn.
- Phi kim được tô cùng một màu. Chúng là các nguyên tố từ C-6 đến Rn-86, bao gồm H-1 (Hiđro). Phi kim không có ánh kim, không dẫn nhiệt hoặc dẫn điện và không có tính dẻo. Chúng thường ở trạng thái khí ở nhiệt độ phòng và có thể ở trạng thái rắn, khí hoặc lỏng.
- Bán kim loại/á kim thường được tô màu tím hoặc xanh lá cây, là sự kết hợp của 2 màu khác. Đường chéo trải dài từ nguyên tố B-5 đến At-85 là đường ranh giới. Chúng có một số tính chất của kim loại và một số tính chất của phi kim.
Lưu ý rằng các nguyên tố đôi khi cũng được sắp xếp thành từng họ. Đó là họ kim loại kiềm (1A), kim loại kiềm thổ (2A), halogen (7A), khí hiếm (8A) và cacbon (4A).
Họ nguyên tố được đánh theo chữ số La Mã, Ả Rập hay số tiêu chuẩn.
Phần 2: Đọc ký hiệu hóa học và tên nguyên tố
Đọc ký hiệu hóa học trước. Đó là sự kết hợp của 1 đến 2 chữ cái được sử dụng thống nhất trong các ngôn ngữ.
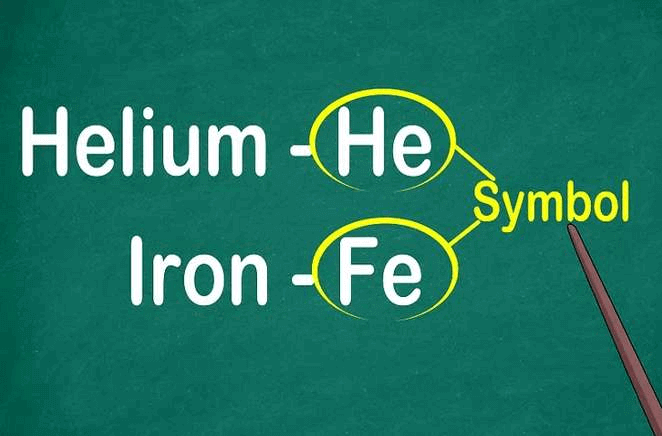
- Ký hiệu hóa học bắt nguồn từ tên Latinh của nguyên tố đó hoặc tên thông thường được phổ biến rộng rãi.
- Trong nhiều trường hợp, ký hiệu hóa học bắt nguồn từ tên tiếng Anh, như trường hợp heli là “He”. Tuy nhiên, đây không phải là quy tắc thống nhất trong hóa học. Ví dụ, sắt (iron) là “Fe”. Vì lý do này, bạn phải ghi nhớ cả ký hiệu hóa học/tên để nhận biết nhanh nguyên tố.
Tìm tên thông thường của nguyên tố. Tên nguyên tố nằm ở dưới ký hiệu hóa học. Nó sẽ thay đổi phụ thuộc vào ngôn ngữ của bảng tuần hoàn.
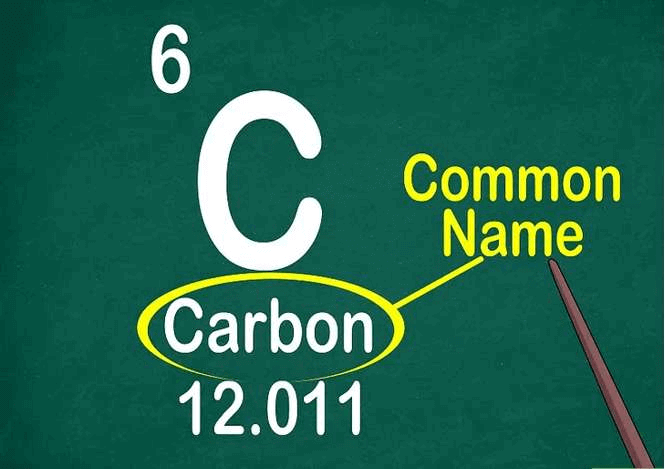
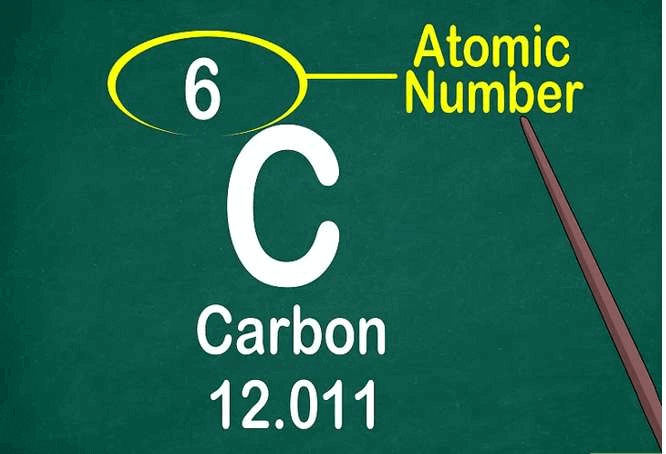
Phần 3: Đọc số hiệu nguyên tử
Đọc bảng tuần hoàn theo số hiệu nguyên tử nằm ở giữa bên trên hoặc ở trên bên trái của mỗi ô nguyên tố. Như đã nói, số hiệu nguyên tử được sắp xếp tăng dần từ góc trái bên trên sang góc phải bên dưới. Biết được số hiệu nguyên tử là cách nhanh nhất để tìm thêm thông tin về nguyên tố.
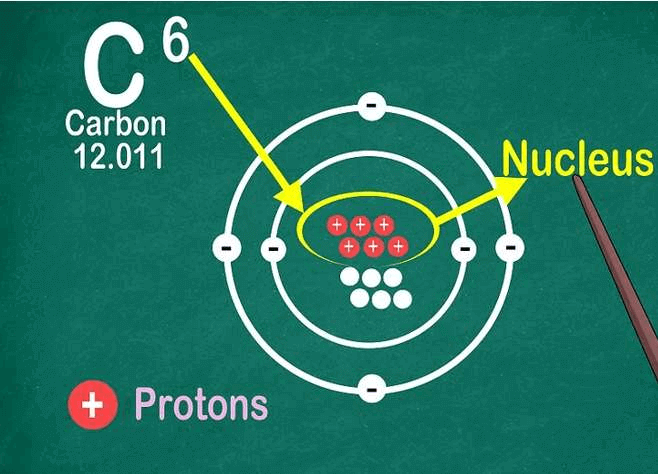
Số hiệu nguyên tử chính là số proton trong hạt nhân nguyên tử của nguyên tố.
Việc thêm hoặc bớt proton sẽ tạo ra nguyên tố khác.
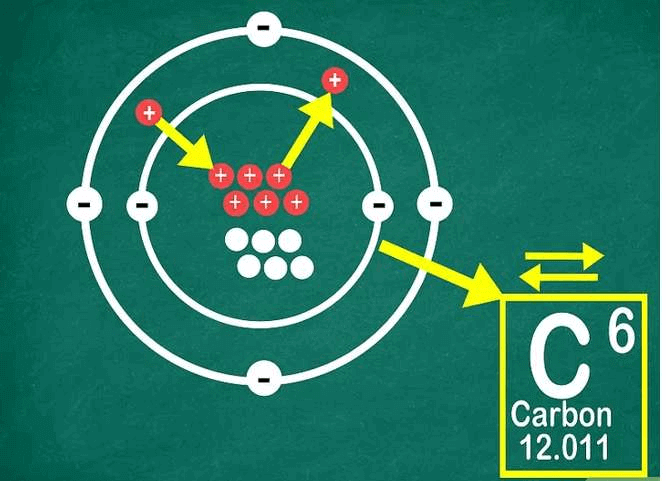
Tìm ra số proton trong nguyên tử cũng như tìm được số electron trong nguyên tử đó. Nguyên tử có số electron và số proton bằng nhau.
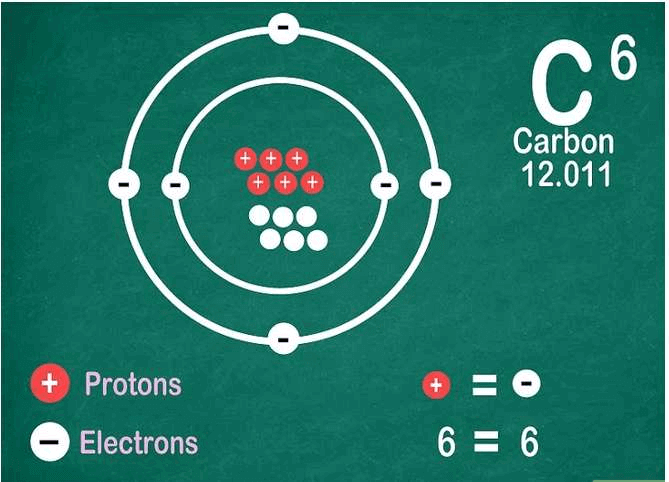
- Lưu ý rằng có một ngoại lệ trong quy tắc này. Nếu nguyên tử mất hoặc nhận electron, nó trở thành một ion tích điện.
- Nếu có dấu cộng bên cạnh ký hiệu hóa học của nguyên tố thì đó là điện tích dương. Nếu là dấu trừ thì đó là điện tích âm.
- Nếu không có dấu cộng hoặc dấu trừ và bài toán hóa học không liên quan đến ion thì bạn có thể xem số proton bằng với số electron.
Phần 4: Đọc trọng lượng nguyên tử
Tìm trọng lượng nguyên tử. Đây là con số bên dưới tên nguyên tố.

Mặc dù dường như trọng lượng nguyên tử tăng dần từ góc trái bên trên sang góc phải bên dưới, nhưng điều này không phải lúc nào cũng đúng.
Trọng lượng nguyên tử của hầu hết các nguyên tố đều được ghi dưới dạng thập phân. Trọng lượng nguyên tử là tổng trọng lượng của các hạt trong hạt nhân nguyên tử; tuy nhiên, đây là nguyên tử khối trung bình của các đồng vị.
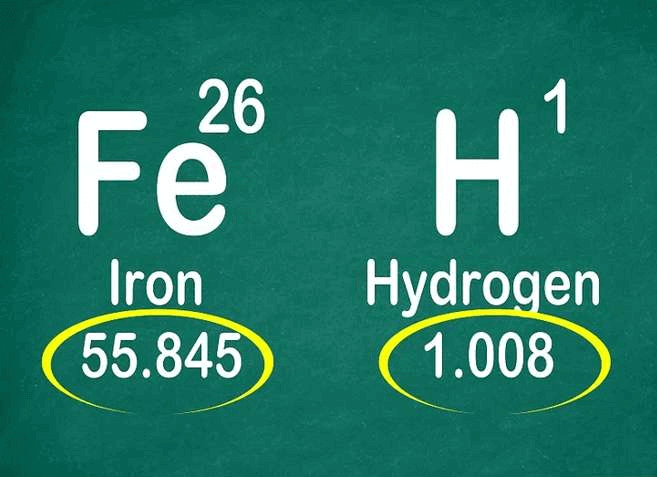
Dùng trọng lượng nguyên tử để tìm số nơtron trong nguyên tử. Làm tròn trọng lượng nguyên tử đến số nguyên gần nhất sẽ được nguyên tử khối. Sau đó, bạn lấy nguyên tử khối trừ đi số proton để có số nơtron.
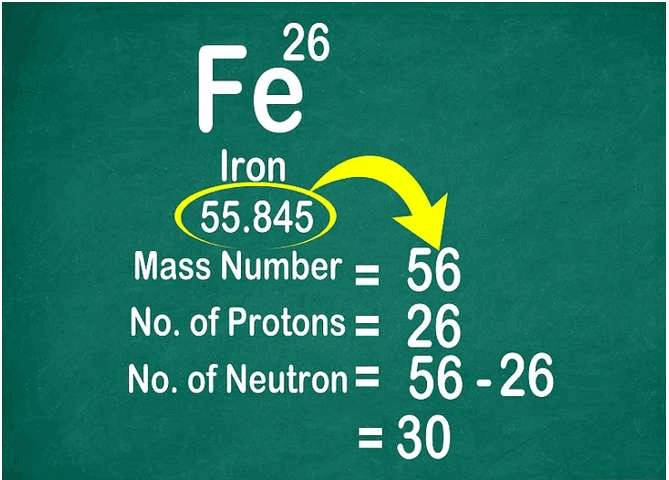
- Ví dụ, trọng lượng nguyên tử của sắt là 55,847, vì vậy nguyên tử khối là 56. Nguyên tử này có 26 proton. 56 (nguyên tử khối) trừ đi 26 (proton) bằng 30. Nghĩa là trong một nguyên tử sắt thường có 30 nơtron.
- Thay đổi số nơtron trong nguyên tử sẽ tạo thành các đồng vị, là các biến thể của nguyên tử có nguyên tử khối nặng hay nhẹ hơn.
-------------------------------------------
Như vậy VnDoc đã giới thiệu các bạn tài liệu Bảng tuần hoàn hóa trị các nguyên tố lớp 8 Mời các bạn tham khảo thêm tài liệu: Chuyên đề Hóa học 8, Giải bài tập Hóa học 8, Giải SBT Hóa 8, Trắc nghiệm Hóa học 8, Tài liệu học tập lớp 8
