Ankin là gì?
Ankin là gì? được VnDoc sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy môn Hóa học lớp 11. Hi vọng rằng đây sẽ là những tài liệu hữu ích trong công tác giảng dạy và học tập của quý thầy cô và các bạn học sinh.
Lưu ý: Nếu bạn muốn Tải bài viết này về máy tính hoặc điện thoại, vui lòng kéo xuống cuối bài viết.
Ankin là gì?
Câu hỏi: Ankin là gì?
Trả lời:
- Ankin là hiđrocacbon không no, mạch hở trong phân tử có chứa 1 liên kết ba CΞC còn lại là các liên kết đơn.
- Công thức tổng quát của ankin: CnH2n-2 (n ≥ 2).
I. Tên gọi của Ankin (danh pháp)
*Tên thường:
- Tên gốc hiđrocacbon gắn với C mang liên kết ba + axetilen
- Ví dụ: CH≡CH: axetilen; CH≡C-CH -CH: etylaxetilen; CH -C≡C-CH: đimetylaxetilen
*Tên thay thế:
- Số chỉ vị trí mạch nhánh + tên nhánh + tên mạch chính + số chỉ vị trí nối ba + in
- Ví dụ: CH≡CH: etin; CH≡C-CH: propin; CH≡C-CH -CH: but-1-in
II. Tính chất vật lý của ankin
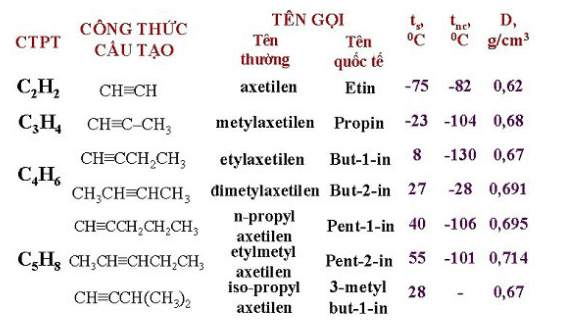
Các chất hữu cơ thuộc nhóm ankin có khối lượng riêng, nhiệt độ sôi và nhiệt độ nóng chảy tăng dần theo phân tử khối. Ankin từ C2-C4 là chất khí và từ C5-C16 là chất lỏng. Còn lại từ C17 trở lên là chất rắn. Các ankin đều nhẹ hơn nước và không tan trong nước, chỉ tan được trong 1 số dung môi hữu cơ.
III. Tính chất hóa học của ankin
1. Phản ứng cộng
Cộng H2
CnH2n-2 + H2 → CnH2n (Pd/PbCO3, to)
CnH2n-2 + 2H2 → CnH2n+2 (Ni, to)
Chú ý:
- Tuỳ thuộc vào xúc tác được sử dụng mà phản ứng cộng H2 vào ankin xảy ra theo các hướng khác nhau.
- Thường thì phản ứng cộng H2 vào ankin thường tạo ra hỗn hợp gồm nhiều sản phẩm.
- Số mol khí giảm = số mol H2 tham gia phản ứng. Chú ý bảo toàn khối lượng, bảo toàn H, bảo toàn C.
Cộng Br2
CnH2n-2 + Br2 → CnH2n-2Br2
CnH2n-2 + 2Br2 → CnH2n-2Br4
- Khối lượng dung dịch brom tăng chính là khối lượng ankin đã phản ứng.
Cộng HX
- Cộng H2O:
+ C2H2 → anđehit
CHΞCH + H2O → CH3 - CHO (H2SO4, HgSO4, 80oC)
+ Ankin khác → xeton
CHΞC-CH3 + H2O → CH3-CO-CH3 (H+)
- Cộng axit:
CHΞCH + HCl → CH2=CHCl (vinyl clorua) (Hg2Cl2 ở 150 đến 200oC)
CHΞCH + HCN → CH2=CH-CN (nitrin acrylic)
CHΞCH + CH3COOH → CH3COOCH=CH2 (vinylaxetat)
CHΞCH + C2H5OH → CH2=CH-O-CH3 (etylvinylete)
2. Phản ứng trùng hợp
- Đimel hóa
2CHΞCH → CHΞC-CH=CH2 (vinyl axetilen) (NH4Cl, Cu2Cl2, to)
- Trime hóa
3CHΞCH → C6H6 (C, 600oC)
- Trùng hợp (polime hóa)
nCHΞCH → (-CH=CH-)n (xt, to, p) (nhựa cupren)
3. Phản ứng oxi hóa
Phản ứng oxi hóa hoàn toàn
CnH2n-2 + (3n - 1)/2O2 → nCO2 + (n - 1)H2O
→ Đặc điểm của phản ứng đốt cháy ankin: nCO2 > nH2O và nCO2 - nH2O = nankin
Phản ứng oxi hóa không hoàn toàn
- Các ankin đều làm mất màu dung dịch thuốc tím ở nhiệt độ thường.
3C2H2 + 8KMnO4 + 2H2O → 3(COOK)2 + 2MnO2 + 2KOH
Nếu trong môi trường axit thì tạo thành CO2 sau đó CO2 phản ứng với KOH tạo thành muối.
- Với các ankin khác sẽ có sự đứt mạch tạo thành hỗn hợp 2 muối.
R1-CΞC-R2 + 2KMnO4 → R1COOK + R2COOK + 2MnO2
4. Phản ứng thế của ank-1-in
CHΞCH + Ag2O → CAgΞCAg↓ + H2O
2CHΞC-R + Ag2O → CAgΞC-R↓ (vàng) + H2O
Chú ý:
- Chỉ có C2H2 mới phản ứng với Ag2O theo tỉ lệ mol 1:1; các ank-1-in khác chỉ phản ứng theo tỉ lệ 2:1.
- Nếu có hỗn hợp ankin tham gia phản ứng với Ag2O mà tỉ lệ mol của (ankin: Ag2O) = k có giá trị:
+ k < 2 → có C2H2.
+ k > 2 → không có C2H2
+ k = 2 → hỗn hợp gồm 2 ank-1-in hoặc hỗn hợp C2H2 và ankin khác (không phải ank-1-in) có số mol bằng nhau.
- Từ kết tủa vàng thu được có thể khôi phục lại ankin ban đầu bằng cách cho tác dụng với HCl.
CAgΞC-R + HCl → CHΞC-R + AgCl
(phản ứng này dùng để tách ank-1-in khỏi hỗn hợp)
- Ngoài cách viết với Ag2O có thể viết phản ứng với dung dịch AgNO3/NH3 và phản ứng này được dùng để nhận biết ank-1-in.
IV. Điều chế ankin
Điều chế axetilen
Điều chế các ankin khác
- Tách HX khỏi dẫn xuất đihalogen
CH2Br-CH2Br + 2KOH → CH≡CH + 2KBr + 2H2O
- Phản ứng giữa axetilua với dẫn xuất halogen:
CH3I + AgC ≡ CAg + CH3I → CH3 - C ≡ C - CH3 + 2AgI
V. Ứng dụng của ankin
- Axetilen cháy trong oxi tạo ra ngọn lửa có nhiệt độ khoảng 3000oC nên được dùng trong đèn xì axetilen - oxi để hàn và cắt kim loại:
C2H2 + O2 → 2CO2 + H2O
- Sử dụng axetilen phải rất cẩn trọng vì khi nồng độ axetilen trong không khí từ 2,5% trở lên có thể gây cháy nổ.
- Axetilen và các ankin khác còn được dùng làm nguyên liệu để tổng hợp các hóa chất cơ bản khác như vinyl clorua, vinyl axetat, vinylaxetilen, anđehit axetic,...
-------------------------------------------
Như vậy VnDoc đã giới thiệu các bạn tài liệu Ankin là gì? Mời các bạn tham khảo thêm tài liệu: Giải bài tập Hóa học lớp 11, Giải SBT Hóa Học 11, Trắc nghiệm Hóa học 11, Tài liệu học tập lớp 11