Bảng tính tan của các muối
Bảng tính tan của các muối được VnDoc sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy môn Hóa học lớp 11. Hi vọng rằng đây sẽ là những tài liệu hữu ích trong công tác giảng dạy và học tập của quý thầy cô và các bạn học sinh.
Lưu ý: Nếu bạn muốn Tải bài viết này về máy tính hoặc điện thoại, vui lòng kéo xuống cuối bài viết.
Bảng tính tan của các muối
Bảng tính tan của các muối
|
Hợp chất |
Tính chất |
Trừ |
|
Axit (xem ở cột ion H+ và anion gốc axit tương ứng). |
Đều tan. |
H2SiO3 |
|
Bazo (xem ở hàng ion OH- và các cation tương ứng). |
Không tan. |
LiOH, NaOH, KOH, Ca(OH)2, Ba(OH)2, NH4OH. |
|
Muối liti Li+ Muối natri Na+ Muối kali K+ Muối amoni NH4+ |
Đều tan. |
|
|
Muối bạc Ag+ |
Không tan (thường gặp AgCl). |
AgNO3, CH3COOAg. |
|
Muối nitrat NO3- Muối axetat CH3COO- |
Đều tan. |
|
|
Muối clorua Cl- Muối bromua Br- Muối iotua I- |
Đều tan. |
AgCl: kết tủa trắng AgBr: kết tủa vàng nhạt AgI: kết tủa vàng PbCl2, PbBr2, PbI2. |
|
Muối sunfat SO42- |
Đều tan |
BaSO4, CaSO4, PbSO4: trắng Ag2SO4: ít tan |
|
Muối sunfit SO32- Muối cacbonnat CO32- |
Không tan |
Trừ muối với kim loại kiềm và NH4+ |
|
Muối sunfua S2- |
Không tan |
Trừ muối với kim loại kiềm, kiềm thổ và NH4+ |
|
Muối photphat PO43- |
Không tan |
Trừ muối với Na+, K+ và NH4+ |
Kiến thức mở rộng:
I. Chất tan và chất không tan
Ở trong nước có chất tan và chất không tan, có chất tan ít, có chất tan nhiều.
Tính tan của một số axit, bazo, muối
– Bảng tính tan của Axit: Hầu hết axit tan được trong nước, trừ axit silixic.
– Bảng tính tan của Bazo: phần lớn các bazo không tan trong nước, trừ một số như: KOH, NaOH,..
– Bảng tính tan của Muối:
- Những muối natri, kali đều tan.
- Những muối nitrat đều tan.
- Phần lớn các muối clorua, sunfat tan được. Nhưng phần lớn các muối cacbonat không tan.
II. Độ tan của một chất trong nước
1, Định nghĩa độ tan
- Độ tan là một đại lượng đặc trưng cho khả năng tan của một chất tại một điều kiện nhất định.
- Độ tan (S) của một chất trong nước là số gam chất đó hòa tan trong 100 g nước để tạo thành dung dịch bão hòa ở một nhiệt độ xác định.
Độ tan của một chất trong nước
- Nếu 100 gam nước hòa tan:
> 10 gam chất tan → chất dễ tan hay chất tan nhiều.
< 1 gam chất tan → chất tan ít.
< 0,01 gam chất tan → chất thực tế không tan.
2, Những yếu tố ảnh hưởng đến độ tan
– Độ tan của chất rắn trong nước phụ thuộc vào nhiệt độ, trong nhiều trường hợp, khi nhiệt độ tăng thì độ tan cũng tăng theo. Số ít trường hợp, nhiệt độ tăng độ tan lại giảm.
– Độ tan của chất khí trong nước phụ thuộc vào nhiệt độ và áp suất. Độ tan của chất khí trong nước sẽ tăng, nếu ta giảm nhiệt độ và tăng áp suất
III. Đặc tính tan trong nước của Axit, Bazơ và muối
Các hợp chất khác nhau có đặc tính tan khác nhau, tổng hợp chung có thể rút ra như sau:
- Axit: Hầu hết các axit đều tan trong nước, trừ Axit Silicic [SiOx(OH)4-2x]n như H2SiO3, H4SiO4,…
- Bazơ: Các bazơ hầu hết không thể tan trong nước trừ một số hợp chất như : KOH, NaOH…
- Muối: Muối kali, natri đều tan; muối nitrat đều tan; hầu hết muối clorua, sunfat đều tan được nhưng hầu như các muối cacbonat đều không tan.
IV. Bảng tính tan hóa học
Bảng tính tan cho ta biết, độ tan các chất trong nước: chất nào kết tủa, bay hơi, chất tan hay không tồn tại trong dung dịch. Từ đó ta có thể làm các bài nhận biết và các bài toán có kiến thức liên quan.
Nắm được bảng tính tan là nội dung quan trọng trong giải các bài toán hóa học. Ở nhiệt độ phòng, áp suất 1atm, ta có bảng tính tan hóa học như sau:
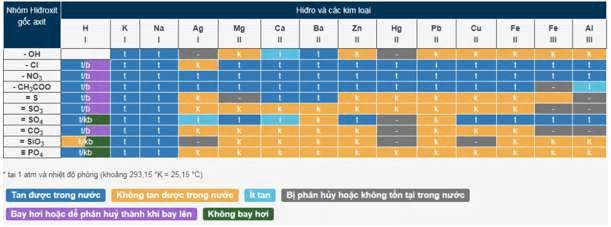
Trong đó:
- t – tan;
- k – không tan;
- b– bay hơi;
- i – tan ít;
- “-” là hợp chất không tồn tại trong nước.
V. Màu sắc của một số bazơ không tan hay gặp
|
Bazo |
Màu sắc |
|
Mg(OH)2 |
Trắng |
|
Cu(OH)2 |
Xanh lam |
|
Al(OH)3 |
Keo trắng |
|
Zn(OH)2 |
Trắng |
|
Pb(OH)2 |
Trắng |
|
Cr(OH)3 |
Lục xám |
|
Mn(OH)2 |
Hồng nhạt |
|
Fe(OH)2 |
Trắng xanh |
|
Fe(OH)3 |
Nâu đỏ |
-------------------------------------------
Như vậy VnDoc đã giới thiệu các bạn tài liệu Bảng tính tan của các muối. Mời các bạn tham khảo thêm tài liệu: Giải bài tập Hóa học lớp 11, Giải SBT Hóa Học 11, Trắc nghiệm Hóa học 11, Tài liệu học tập lớp 11

