Công thức phân tử của Phenol
Công thức phân tử của Phenol được chúng tôi sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy môn Hóa học lớp 11. Hi vọng rằng đây sẽ là những tài liệu hữu ích trong công tác giảng dạy và học tập của quý thầy cô và các bạn học sinh.
Lưu ý: Nếu bạn muốn Tải bài viết này về máy tính hoặc điện thoại, vui lòng kéo xuống cuối bài viết.
Công thức phân tử của Phenol
Câu hỏi: Công thức phân tử của Phenol là gì?
Trả lời:
Công thức phenol
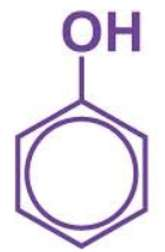
I. Định nghĩa
- Phenol là những hợp chất hữu cơ trong phân tử có nhóm -OH liên kết trực tiếp với nguyên tử C của vòng benzen.
Lưu ý: Cần phân biệt phenol và ancol thơm
- Phân loại: Dựa vào số nhóm -OH trong phân tử, phenol chia thành 2 loại: phenol đơn chức và đa chức.
II. Tính chất vật lý của phenol
Phenol ít tan trong nước lạnh, tan nhiều trong nước nóng nên dùng để tách bằng phương pháp chiết.Là chất rắn, độc, khi để lâu trong không khí bị chảy rữa do hút ẩm và chuyển thành màu hồng.
III. Tính chất hóa học
Có một nhóm -OH liên kết trực tiếp với cacbon của vòng Benzen. Đặc biệt hơn, trong phân tử phenol có hiệu ứng liên hợp mạnh do có oxi của nhóm -OH cũng ảnh hưởng đến tính chất vật lý cũng như tính chất hóa học của phenol.
Cụ thể, trong phân tử phenol có hiệu ứng liên hợp (+C), mây electron của cặp e không tham gia liên kết trong nguyên tử O bị dịch chuyển về phía nhân benzen: kết quả làm tăng độ phân cực của liên kết O - H. Nguyên tử H linh động, dễ tách ra làm phenol có tính axit. Mặt khác, do hiệu ứng liên hợp dương (+C) của nhóm OH làm mật độ e ở các vị trí ortho và para trên nhân benzen tăng lên, do đó phản ứng thế vào các vị trí này dễ hơn ở benzen. (phần này nâng cao phù hợp cho các bạn muốn hiểu sâu về cơ chế phản ứng của dãy đồng đẳng phenol)
Từ đây, Phenol có phản ứng thế nguyên tử H của nhóm -OH và có tính chất của vòng benzen.
Phản ứng thế nguyên tử H của nhóm -OH:
Tác dụng với kim loại kiềm:
C6H5OH + Na → C6H5ONa + 1/2H2
(Các muối ancolat là chất rắn, tan nhiều trong rượu tương ứng, bị thuỷ phân hoàn toàn)
→ Phản ứng này dùng để phân biệt phenol với anilin.
Tác dụng với dung dịch kiềm:
C6H5OH + NaOH → C6H5ONa + H2O
Chú ý:
- Vòng benzen đã làm tăng khả năng phản ứng của nguyên tử H thuộc nhóm -OH trong phân tử phenol so với trong phân tử ancol.
- Phản ứng này chứng tỏ H của phenol linh động hơn H của Ancol. Phenol thể hiện tính axit nhưng là axit rất yếu không làm đổi màu quỳ tím, yếu hơn cả axit cacbonic.
C6H5ONa + CO2 + H2O → C6H5OH + NaHCO3 (Phản ứng này được dùng để tái tạo phenol trong công nghiệp)
- Phản ứng này dùng để tách phenol khỏi hỗn hợp anilin và phenol sau đó thu hồi lại phenol nhờ phản ứng với các axit mạnh hơn:
C6H5ONa + HCl → C6H5OH + NaCl
Phản ứng thế nguyên tử H của vòng benzen:
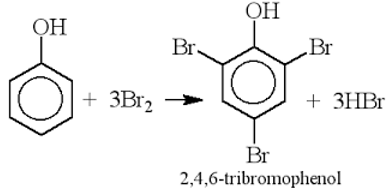
-Thí nghiệm: phenol tác dụng với dung dịch brom.
Hiện tượng: Có kết tủa trắng
Phương trình hóa học:
-Thí nghiệm: phenol tác dụng với HNO3 đặc có xúc tác H2SO4 đặc, đun nóng tạo 2, 4, 6 - trinitrophenol (axit picric).
Hiện tượng: Có kết tủa vàng.
Phương trình hóa học:
C6H5OH + 3HNO3 → C6H2(NO2)3OH + 3H2O
Nhận xét:
- Phản ứng này dùng để nhận biết phenol khi không có mặt của anilin.
- Chứng minh ảnh hưởng của nhóm -OH đến khả năng phản ứng của vòng benzen.
Chú ý: Ngoài phenol, tất cả những chất thuộc loại phenol mà còn nguyên tử H ở vị trí o, p so với nhóm -OH đều có thể tham gia vào 2 phản ứng thế brom và thế nitro.
Phản ứng tạo nhựa phenolfomanđehit:
Phenol + HCHO trong môi trường axit tạo sản phẩm là nhựa phenolfomandehit.
nC6H5OH + nHCHO → nH2O + (HOC6H2CH2)n
IV. Cách điều chế Phenol
Chúng ta đã tìm hiểu Phenol là gì. Ngay bây giờ sẽ là cách điều chế chất này. Phenol lần đầu tiên được chiết xuất với nguyên liệu là từ nhựa than đá. Cách thức như sau:
![]()
Ngày nay, chúng đã được sản xuất trên quy mô lớn (khoảng 7 tỷ kg/năm) với các nguyên liệu có nguồn gốc từ dầu mỏ
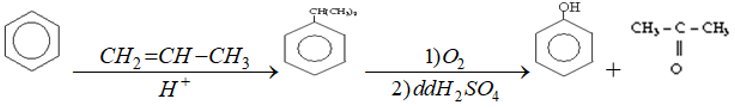
Chế biến Phenol trong công nghiệp điều chế đồng thời phenol và xeton như sau:
V. Ứng dụng của phenol
+ Phenol được dùng trong nhiều lĩnh vực khác nhau:
– Công nghiệp chất dẻo: phenol là nguyên liệu để điều chế nhựa phenol formaldehyde.
– Công nghiệp tơ hóa học: Từ phenol tổng hợp ra tơ polyamide.
– Nông dược: Từ phenol điều chế được chất diệt cỏ dại và kích thích tố thực vật 2,4 – D (là muối natri của axit 2,4 điclophenoxiaxetic).
– Phenol cũng là nguyên liệu để điều chế một số phẩm nhuộm, thuốc nổ (axit picric).
– Do có tính diệt khuẩn nên phenol được dùng để trực tiếp làm chất sát trùng, tẩy uế, hoặc để điều chế các chất diệt nấm mốc (ortho – và para – nitrophenol…)
-------------------------------------------
Như vậy VnDoc đã giới thiệu các bạn tài liệu Công thức phân tử của Phenol. Mời các bạn tham khảo thêm tài liệu: Giải bài tập Hóa học lớp 11, Giải SBT Hóa Học 11, Trắc nghiệm Hóa học 11, Tài liệu học tập lớp 11