Photpho trắng và photpho đỏ là
Photpho trắng và photpho đỏ là được chúng tôi sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy môn Hóa học lớp 11. Hi vọng rằng đây sẽ là những tài liệu hữu ích trong công tác giảng dạy và học tập của quý thầy cô và các bạn học sinh.
Lưu ý: Nếu bạn muốn Tải bài viết này về máy tính hoặc điện thoại, vui lòng kéo xuống cuối bài viết.
Photpho trắng và photpho đỏ
Trắc nghiệm: Photpho trắng và photpho đỏ là
- 2 chất khác nhau.
- 2 chất giống nhau.
- 2 dạng đồng phân của nhau.
- 2 dạng thù hình của nhau.
Trả lời:
Đáp án đúng: D. 2 dạng thù hình của nhau.
Photpho trắng và photpho đỏ là 2 dạng thù hình của nhau.
I. Đơn chất của photpho
Vì P có các số oxi hóa: -3, 0, +3, +5 nên P có thể thể hiện tính khử và tính oxi hóa.
Tính oxi hóa: P0→ P -3
Tác dụng với một số kim loại hoạt động, tạo ra photphua kim loại.
Ví dụ:
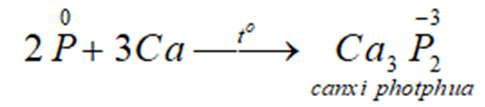
Tính khử: P 0 → P +3, P0 → P +5
- Tác dụng với oxi: Khi đốt nóng, photpho cháy trong không khí tạo ra các oxit của photpho:
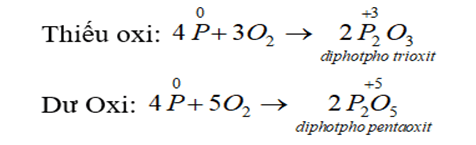
- Tác dụng với clo: Khi cho clo đi qua P nóng chảy, sẽ thu được các hợp chất photpho clorua:
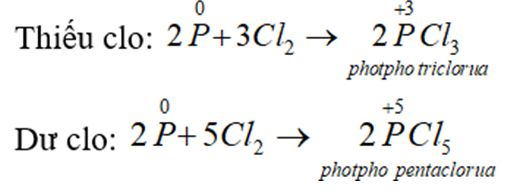
- Tác dụng với hợp chất:
6P + 5KClO3 → 3P2O5 + 5KCl
II. Axit photphoric (H3PO4)
- Là axit ba nấc, có độ mạnh trung bình.
- Có đầy đủ tính chất hóa học của một axit.
- Khi tác dụng với dung dịch kiềm, tùy theo lượng chất mà tạo ra các muối khác nhau.
III. Muối photphat
Khái niệm và tính chất vật lí
- Có 3 loại: PO43-, HPO42- và H2PO4-.
- Tất cả muối H2PO4- đều tan; muối PO43- và HPO42- chỉ có muối của kim loại kiềm và amoni tan được.
Tính chất hóa học
- Muối photphat có đầy đủ các tính chất hóa học của muối.
- Các muối photphat của kim loại kiềm dễ bị thủy phân trong dung dịch tạo môi trường bazơ:
Na3PO4 → 3Na+ + PO43-
PO43- + H2O → HPO42- + OH-
- Muối axit còn biểu hiện tính chất của axit.
NaH2PO4 + NaOH → Na2HPO4 + H2O
Điều chế
- Cho P2O5 hoặc H3PO4 tác dụng với dung dịch kiềm.
- Dùng phản ứng trao đổi ion.
Nhận biết
Nhận biết ion PO43- bằng dung dịch AgNO3:
3Ag+ + PO43- → Ag3PO4 (kết tủa vàng)
IV. Trắc nghiệm
Câu 1. Vị trí của P (z = 15) trong bảng tuần hoàn các nguyên tố hóa học là
- ô 15, chu kỳ 2, nhóm VA.
- ô 15, chu kỳ 3, nhóm VA.
- ô 15, chu kỳ 2, nhóm IIIA.
- ô 15, chu kỳ 3, nhóm IIIA.
Câu 2. Hai dạng thù hình phổ biến, quan trọng của photpho là
- Photpho trắng và photpho đen.
- Photpho trắng và photpho đỏ.
- Photpho đỏ và photpho đen.
- Photpho tinh thể và photpho vô định hình.
Câu 3. Số oxi hóa của P trong hợp chất là
- +1, +3, +5.
- -3, +1, +3, +5.
- -3, +1, +2, +3, +4, +5.
- –3, +3, +5.
Câu 4. Khi tham gia phản ứng hóa học, P thể hiện tính chất nào sau đây?
- Tính oxi hóa.
- Tính khử.
- Vừa có tính oxi hóa, vừa có tính khử.
- Tính kim loại.
Câu 5. Trong các nguồn sau, nguồn chứa nhiều photpho trong tự nhiên là
- Quặng apatit.
- Quặng xiđerit.
- Cơ thể người và động vật.
- Protein thực vật.
Câu 6. Thành phần chính của quặng photphorit là
- Ca(H2PO4)2.
- Ca3(PO4)2.
- NH4H2PO4.
- CaHPO4.
Câu 7. Công thức đúng của quặng apatit là
- Ca3(PO4)2.
- Ca(H2PO4)2.
- 3Ca3(PO4)2 .CaF2.
- CaSO4.
Câu 8. Cho P tác dụng với Ca, sản phẩm thu được là
- Ca3P2.
- Ca2P3.
- Ca3(PO4)2.
- CaP2.
Câu 9. Công thức của magie photphua là
- Mg3(PO4)2.
- MgP.
- Mg3P2.
- Mg2P3.
Câu 10. Đốt cháy P trong lượng dư khí oxi thu được sản phẩm là
- PO.
- P2O.
- P2O3.
- P2O5.
-------------------------------------------
Như vậy VnDoc đã giới thiệu các bạn tài liệu Photpho trắng và photpho đỏ là. Mời các bạn tham khảo thêm tài liệu: Giải bài tập Hóa học lớp 11, Giải SBT Hóa Học 11, Trắc nghiệm Hóa học 11, Tài liệu học tập lớp 11


