Các tính chất hóa học của nhôm
Các tính chất hóa học của nhôm được VnDoc sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy môn Hóa học lớp 9. Hi vọng rằng đây sẽ là những tài liệu hữu ích trong công tác giảng dạy và học tập của quý thầy cô và các bạn học sinh.
Lưu ý: Nếu bạn muốn Tải bài viết này về máy tính hoặc điện thoại, vui lòng kéo xuống cuối bài viết.
Tính chất hóa học của nhôm
Câu hỏi: Nêu các tính chất hóa học của nhôm?
- Nhôm có đầy đủ tính chất hóa học của kim loại như:
- Tác dụng với phi kim:
+ Al tác dụng với O2 tạo thành nhôm oxit.
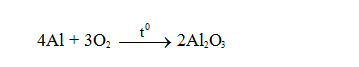
- Tác dụng với các phi kim khác: Nhôm tác dụng với một số phi kim tạo thành muối nhôm.
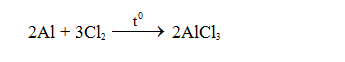
- Tác dụng với dung dịch axit:
- Nhôm tác dụng với một số dd axit (HCl, H2SO4 loãng …) tạo thành muối và giải phóng khí H2.
2Al + 6HCl → 2AlCl3 + 3H2 ↑
- Tác dụng với dung dịch muối: Nhôm tác dụng với dung dịch muối của những kim loại có hoạt động hóa học yếu hơn (trong dãy hoạt động hóa học của kim loại) tạo ra muối nhôm và kim loại mới.
2Al + 3CuSO4 → Al2(SO4)3 + 3Cu ↓
- Tác dụng với dung dịch kiềm: Ngoài những tính chất hóa học trên, nhôm còn tác dụng được với dung dịch kiềm như NaOH, KOH…
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2 ↑
1. Định nghĩa nhôm là gì?
- Nhôm (bắt nguồn từ tiếng Pháp: aluminium, phiên âm tiếng Việt: a-luy-mi-nhôm) là tên của một nguyên tố hóa học trong bảng tuần hoàn nguyên tố có ký hiệu Al và số nguyên tử bằng 13.
- Nhôm thuộc kim loại, có màu sắc trắng ánh bạc, mềm và nhẹ. Nhôm có độ phản chiếu cao cũng như có tính dẫn nhiệt và dẫn điện lớn. Nhôm là kim loại không độc và có tính chống mài mòn. Nhôm cũng là kim loại có nhiều thành phần nhất.
- Trong tự nhiên rất khó để tìm được nhôm nguyên chất, thông thường kim loại này được tìm thấy khi được kết hợp cùng oxygen cùng với những nguyên tố khác. Người ta vẫn thường gọi là hợp kim nhôm trong cuộc sống hàng ngày.
2. Tính chất vật lý của Nhôm
- Nhôm (Al) có nguyên tử khối bằng 27 đvC, có những tính chất vật lý sau:
+ Là kim loại mềm có tính dẻo, màu trắng bạc, có ánh kim mờ
+ Khối lượng riêng: 2,7 g/cm3
- Dẫn nhiệt, dẫn điện tốt (độ dẫn điện của Al bằng 2/3 độ dẫn điện của Cu)
- Nhiệt độ nóng chảy: 660°C
3. Tính chất hóa học
Tính khử mạnh: Al → Al3+ + 3e
Tác dụng với phi kim
- Với oxi: Ở to thường tạo lớp màng oxit bảo vệ. Nếu đốt bột nhôm thì sẽ phản ứng mạnh.
Ví dụ:
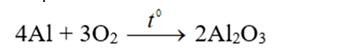
- Với phi kim khác:
+ Với Cl2, Br2 phản ứng ngay ở to thường tạo thành AlCl3, AlBr3 phản ứng bốc cháy.
Ví dụ:

+ Khi đun nóng, phản ứng được với I2, S. Khi đun nóng mạnh, phản ứng được với N2, C.
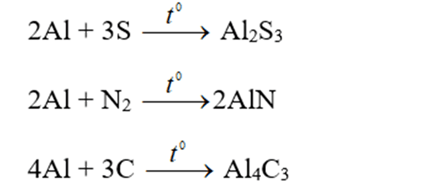
Tác dụng với axit
- Axit thường: khử dễ dàng ion H+ thành H2.
Al + 3HCl → AlCl3 + 3/2 H2
- Axit oxi hóa: Không tác dụng với axit H2SO4, HNO3 đặc nguội. Al tác dụng mạnh với axit HNO3 loãng, H2SO4 đặc, nóng.
Ví dụ:
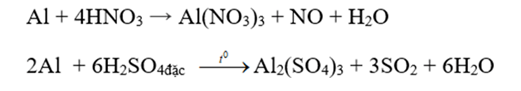
Tác dụng với oxit kim loại – Phản ứng nhiệt nhôm
Ở to cao, Al khử được nhiều ion kim loại trong oxit như (Fe2O3, Cr2O3, CuO …) thành kim loại tự do.
Ví dụ:
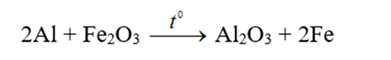
Phản ứng nhiệt nhôm
4. Tổng hợp các ứng dụng của nhôm trong cuộc sống
- Ưu điểm lớn nhất của Al chính là khả năng chống mài mòn rất tốt và độ bền cao nên Al không xảy ra phản ứng hóa học hay vật lý khi tiếp xúc nên nhôm được ứng dụng trong nhiều lĩnh vực trong cuộc sống như thực phẩm, dược phẩm, công nghiệp, gia dụng…
Ứng dụng trong y học
- Nhôm là kim loại nhưng hợp chất của Al là nhôm Oxit lại có tính chất thích hợp trở thành vật liệu sinh học. Với tính chất trơn nhẵn nhôm oxit được chế tác che chắn các bề mặt tiếp xúc của các bộ phận giả trên cơ thể (hông, vai, chân, tay..), rất an toàn không ảnh hưởng tới sức khỏe.
- Ngoài ra nhôm oxit còn được các hãng mỹ phẩm sản xuất kem che khuyết điểm, son, phấn má… nhờ đặc tính làm bóng và mịn da.
Ứng dụng trong công nghiệp
- Thật dễ dàng để bắt gặp những chiếc máy cắt, các chi tiết vận hành sản xuất được làm từ Al. Với tính chất sáng, không hoen rỉ Al đã dần trở thành những thành phần không thể thiếu được của mỗi nhà máy. Một số vật dụng được sản xuất từ Al như:
- Khung xe máy, khung xe ô tô
- Thùng xe tải, một số chi tiết khác
- Thanh tản nhiệt…
- Đặc biệt Al được ứng dụng trong sản xuất của ngành hàng không. Thân và cánh máy bay được làm từ Al – đây là ứng dụng dựa vào đặc tính khối lượng riêng của nhôm nhẹ và bền rất cần thiết để máy bay có thể giảm trọng lượng tối đa khi bay trên bầu trời.
Ứng dụng trong cuộc sống hàng ngày
- Có thể nói trong nhà chúng ta rất nhiều đồ gia dụng được làm từ Al . Khác với sắt dễ bị hoen rỉ nhôm vừa có khả năng chống rỉ lại rất bền đẹp đạt độ thẩm mỹ cao. Từ bàn tay tài hoa của những người thợ chế tác những thanh nhôm vô tri vô giác trở nên gần gũi và phổ biến hơn trong cuộc sống với hình dáng của những đồ gia dụng quen thuộc.
- Tủ quần áo, tủ kệ, tủ bếp…
- Thanh treo màn, mắc áo, mắc treo đồ…
- Chậu nhôm, mâm nhôm, thìa nhôm…
- Thang nhôm, bàn ghế, giường nhôm…
Ứng dụng trong ngành xây dựng
- Al được tôn vinh là “cạ cứng” của ngành xây dựng Việt Nam. Bởi lẽ rất nhiều nguyên liệu được làm từ chất liệu Al – từ giá thành đến tính chất của nhôm đều thích hợp ứng dụng trong sản xuất đại trà.
- Cửa sổ, cửa chính, cửa phụ, cửa nhà vệ sinh…
- Khung sườn nhôm, tủ kệ
- Mái hiên, mặt tiền, mặt dựng, vách ngăn…
Ứng dụng trong ngành chiếu sáng
- Thanh nhôm định hình LED, hay đèn làm từ chất liệu Al trở thành các khái niệm quen thuộc trong ngành chiếu sáng. Được làm từ chất liệu Al nên các thiết bị chiếu sáng sẽ giảm được giá thành đáng kể so với các dòng đèn làm từ đồng hay hợp kim. Đồng thời với khả năng chịu nhiệt tốt Al sẽ giúp bạn có được 1 sản phẩm thiếu sáng có tuổi thọ dài, hoạt động ổn định.
-------------------------------
Ngoài Các tính chất hóa học của nhôm đã được VnDoc giới thiệu, mời các bạn cùng tham khảo thêm Chuyên đề Hóa học lớp 9, Trắc nghiệm Hóa học 9, Lý thuyết môn Hóa học lớp 9 để hoàn thành tốt chương trình học THCS.
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu học tập THCS miễn phí trên Facebook: Tài liệu học tập lớp 9. Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu mới nhất.

