Trong phòng thí nghiệm Etilen được điều chế bằng cách
Chúng tôi xin giới thiệu bài Trong phòng thí nghiệm Etilen được điều chế bằng cách được VnDoc sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy môn Hóa học lớp 9. Hi vọng rằng đây sẽ là những tài liệu hữu ích trong công tác giảng dạy và học tập của quý thầy cô và các bạn học sinh.
Lưu ý: Nếu bạn muốn Tải bài viết này về máy tính hoặc điện thoại, vui lòng kéo xuống cuối bài viết.
Điều chế Etilen trong phòng thí nghiệm
Câu hỏi: Trong phòng thí nghiệm etilen được điều chế bằng cách
- tách H2 từ etan
- cộng H2 vào axetilen
- cracking propan
- đun nóng ancol etylen với H2SO4 đặc
Lời giải:
Đáp án đúng: D. đun nóng ancol etylen với H2SO4 đặc
Trong phòng thí nghiệm etilen được điều chế bằng cách đun nóng ancol etylen với H2SO4 đặc
Phương trình hóa học: C2H5OH -> C2H4 + H2O.
I. Khái niệm Etilen
Khí Etilen (tên IUPAC là ethene) là chất khí, là một loại hiđrocacbon có công thức hóa học là C2H4 hoặc CH2 = CH2. Được biết đến là một chất khí dễ cháy không màu với mùi ngọt của xạ hương hơi mờ nhạt.
Những đặc điểm nổi bật của khí Ethylene – C2H4 là gì
- Là một alkene đơn giản nhất, nó đứng đầu trong dãy alkene.
- Ethene là loại khí olefin đơn giản nhất.
- Là phân tử tín hiệu sinh học dạng khí đầu tiên được con người biết đến.
- Ethylene được thực vật tổng hợp trong các giai đoạn phát triển khác nhau và đáp ứng yêu cầu sinh học và phi sinh học theo mỗi giai đoạn.
- Khí Etylen ảnh hưởng đến a sự tăng trưởng, phát triển thực vật và phản ứng với dấu hiệu môi trường.
II. Tính chất vật lí
Etilen là chất khí, không màu, không mùi, nhẹ hơn không khí và ít tan trong nước.
III. Cấu tạo phân tử
Etilen có công thức cấu tạo:
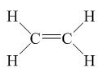
Viết gọn là: CH2=CH2
Trong phân tử etilen C2H4, có một liên kết đôi giữa hai nguyên tử cacbon.
Trong liên kết đôi có một liên kết kém bền. Liên kết này dễ đứt ra trong các phản ứng hóa học.
IV. Tính chất hóa học
Tác dụng với oxi: Khi đốt trong oxi, etilen cháy tạo thành khí CO2và H2O, tỏa nhiều nhiệt.
PTHH: C2H4 + 3O2 → 2CO2 + 2H2O
Tác dụng với dung dịch brom (phản ứng cộng);
PTHH: CH2= CH2 + Br2 → Br – CH2 – CH2 – Br
Nhìn chung các chất liên kết đôi (tương tự etilen) dễ tham gia phản ứng cộng
Các phân tử etilen kết hợp với nhau (phản ứng trùng hợp)
Ở điều kiện thích hợp các phân tử etilen kết hợp với nhau tạo ra chất có phân tử lượng rất lớn gọi là polime.
PTHH: ....+ CH2= CH2 + CH2= CH2 +....→ ....- CH2- CH2 - CH2- CH2-....
V. Ứng dụng
- Etilen dùng để điều chế axit axetic, rượu etylic, poli (vinyl clorua),...
- Khí Etilen có đặc tính kích thích tăng sinh trưởng của các tế bào thực vật nên được ứng dụng vào mục đích này luôn. Đồng thời, kích thích ra hoa, etilen làm chín trái cây, kích thích quả chín ở các loại cây ăn trái.
Không những vậy, etilen có tác dụng kích thích sự nảy mầm ở khoai tây, kích thích hạt nảy mầm.
Ngoài ra, Etylen ứng dụng kích thích trái cây nhanh chín hơn và độ chín đều hơn so với các phương pháp giấm quả khác như sử dụng đất đèn,…
Tác dụng của etilen – Etylen Kích thích ra quả trái vụ ở dứa.
Một trong những ứng dụng quan trọng của etilen là cạo mủ cao su. Khí Etylen còn được ứng dụng thu hoạch trong các loại cây lấy mủ tăng hiệu quả và chất lượng như cao su, thông, trôm,…đây cũng được xem là ứng dụng chính của etilen
VI. Bài tập vận dụng về Etilen
Bài 1: Hãy tính số liên kết đơn, liên kết đôi giữa những nguyên tử cacbon trong phân tử các chất sau:
a) CH3– CH3;
b) CH2 = CH2;
c) CH2 = CH – CH = CH2
Giải
CH3 – CH3
Có 1 liên kết đơn giữa hai nguyên tử cacbon C – C
CH2 = CH2
Có 1 liên kết đôi giữa hai nguyên tử cacbon C – C
CH2 = CH – CH2 = CH2
Có 1 liên kết đơn (C-C) và hai liên kết đôi (C = C) trong phân tử chất
Bài 2: Điền từ thích hợp “có” hoặc “không” vào các cột sau:
|
|
Có liên kết đôi |
Làm mất màu dung dịch |
Phản ứng trùng hợp |
Tác dụng với oxi |
|
Metan |
Không |
Không |
Không |
Có |
|
Etilen |
Có |
Có |
Có |
Có |
Bài 3 Hóa 9 trang 119: Hãy nêu phương pháp hoá học loại bỏ khí etilen có lẫn trong khí metan để thu được metan tinh khiết.
Dẫn hỗn hợp khí qua bình đựng dung dịch brom dư, khí etilen phản ứng hết tạo thành đibrometan là chất lỏng ở trong dung dịch. Khí thoát ra là CH4.
CH2 = CH2 + Br2 → Br-CH2-CH2-Br
-------------------------------
Ngoài Trong phòng thí nghiệm Etilen được điều chế bằng cách đã được VnDoc giới thiệu, mời các bạn cùng tham khảo thêm Chuyên đề Hóa học lớp 9, Trắc nghiệm Hóa học 9, Lý thuyết môn Hóa học lớp 9 để hoàn thành tốt chương trình học THCS.
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu học tập THCS miễn phí trên Facebook: Tài liệu học tập lớp 9. Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu mới nhất.

