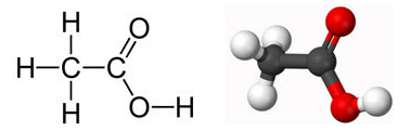
Công thức cấu tạo của CH3COOH
Chúng tôi xin giới thiệu bài Công thức cấu tạo của CH3COOH được VnDoc sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy môn Hóa học lớp 9. Hi vọng rằng đây sẽ là những tài liệu hữu ích trong công tác giảng dạy và học tập của quý thầy cô và các bạn học sinh.
Lưu ý: Nếu bạn muốn Tải bài viết này về máy tính hoặc điện thoại, vui lòng kéo xuống cuối bài viết.
Công thức cấu tạo của CH3COOH
Câu hỏi: Công thức cấu tạo của CH3COOH?
Trả lời:
Công thức cấu tạo của Axit axetic:
I. Axit axetic là gì?
Axit axetic là một hợp chất hữu cơ có tính axit mạnh, chúng có công thức hóa học CH3CO2H (cũng viết là CH3COOH). Đây là loại hóa chất đã được sản xuất từ rất lâu đời và được ứng dụng rất nhiều trong sản xuất công nghiệp, sản xuất thực phẩm hay y học...
Chúng còn có nhiều tên gọi khác nhau như: etanoic, Hydro axetat (HAc), Ethylic acid, Axit metanecarboxylic, dấm, acetic acid, Acid ethanoic…
II. Tính chất vật lý của axit axetic C2H4O2
- Axit axetic CH3COOH là chất lỏng, không màu, vị chua, tan vô hạn trong nước. Dung dịch axit axetic nồng độ từ 2 – 5 % dùng làm giấm ăn.
III. Tính chất hóa học của axit axetic
Axit axetic là một axit hữu cơ có tính axit yếu. Nó làm quỳ tím hóa đỏ, phenolphtalein hóa xanh và tác dụng với một số kim loại, oxit bazơ, muối và dung dịch kiềm.
1. Axit axetic tác dụng với kim loại
Axit axetic tác dụng với một số kim loại (Fe, Mn, Zn…) tạo thành muối và giải phóng khí H2.
2CH3COOH + Zn → (CH3COO)2Zn + H2 ↑
2. Axit axetic tác dụng với oxit bazơ
CH3COOH tác dụng với oxit bazơ tạo thành muối và nước.
2CH3COOH + CuO → (CH3COO)2Cu + H2O
3. Axit axetic tác dụng với dung dịch kiềm
Axit axetic tác dụng với dung dịch kiềm tạo thành muối và nước.
CH3COOH + NaOH → CH3COONa + H2O
4. Axit axetic tác dụng với dung dịch muối
CH3COOH tác dụng với dung dịch muối tạo thành muối mới và axit mới.
2CH3COOH + K2CO3 → 2CH3COOK + CO2 ↑ + H2O
5. Axit axetic tác dụng với rượu etylic
Axit axetic tác dụng với rượu etylic tạo thành etyl axetat trong môi trường H2SO4 đặc, đun nóng. Đây là một este có mùi thơm, ít tan trong nước và thường được ứng dụng làm dung môi trong công nghiệp.
CH3–CH2–OH + CH3–COOH (H2SO4 đặc, t°) ⇔ CH3–COO–CH2–CH3 + H2O
Sản phẩm của phản ứng trên là CH3-COO-CH2-CH3 là một este. Phản ứng trên được gọi là phản ứng este hóa.
IV. Ứng dụng của axit axetic.
Hơn 60 % axit axetic CH3COOH được dùng trong các polyme tổng hợp từ vinyl axetat hoặc xenlulozo este. Các vinyl axetat phần lớn được dùng trong công nghiệp sơn, giấy bọc và nhựa plastic.
Dẫn xuất của axit axetic được sử dụng rộng rãi như:
+ Aluminum axetat: Al(OH)2CO2CH3 dùng làm thuốc nhuộm vải.
+ Muối amoni axetat CH3CO2NH4 được sử dụng để sản xuất axetamid- một chất dung môi, giúp lợi tiểu và toát mồ hôi trong y học.
+ Muối Kali dùng trong công nghiệp sơn.
+ Metyl axetat dùng làm dung môi cho xenlulozo nitrat, este và các hợp chất khác.
+ N- butyl axetat dùng làm dung môi trong công nghiệp sơn và gốm sứ.
+ Axit phenylaxetic dùng trong công nghiệp nước hoa và tổng hợp penicinil.
+ Dung dịch axit axetic băng loãng dùng trong các phòng thí nghiệm lâm sàng để dung giải hồng cầu và đếm bạch cầu.
- Axit axetic là một hóa chất có nhiều ứng dụng trong đời sống và công nghiệp:
+ Giấm ăn
+ Sản xuất chất dẻo
+ Ứng dụng trong công nghiệp dệt nhuộm, thuốc diệt côn trùng
+ Sản xuất tơ nhân tạo
+ Sản xuất este
+ Ứng dụng trong dược phẩm
V. Sản xuất axit axetic
Axit axetic (CH3COOH) được sản xuất theo 2 con đường chính là sinh học và tổng hợp. Trong đó, phương pháp sinh học chỉ chiếm khoảng 10% sản lượng. Dưới đây là một số phương pháp sản xuất axit axetic.
– Lên men oxi hóa từ rượu etylic:
C2H5OH + O2 → CH3COOH + H2O
– Lên men kỵ khí từ đường:
C6H12O6 → 3CH3COOH
– Cacbonyl hóa metanol:
CH3OH + O2 → CH3COOH
– Oxi hóa axetaldehyt:
2CH3CHO + O2 → 2CH3COOH
Và nhiều phương pháp khác…
-------------------------------
Ngoài Công thức cấu tạo của CH3COOH đã được VnDoc giới thiệu, mời các bạn cùng tham khảo thêm Chuyên đề Hóa học lớp 9, Trắc nghiệm Hóa học 9, Lý thuyết môn Hóa học lớp 9 để hoàn thành tốt chương trình học THCS.
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu học tập THCS miễn phí trên Facebook: Tài liệu học tập lớp 9. Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu mới nhất.