Đặc điểm cấu tạo phân tử hợp chất hữu cơ
Đặc điểm cấu tạo phân tử hợp chất hữu cơ được chúng tôi sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy môn Hóa học lớp 9. Hi vọng rằng đây sẽ là những tài liệu hữu ích trong công tác giảng dạy và học tập của quý thầy cô và các bạn học sinh.
Lưu ý: Nếu bạn muốn Tải bài viết này về máy tính hoặc điện thoại, vui lòng kéo xuống cuối bài viết.
Đặc điểm cấu tạo phân tử hợp chất hữu cơ
Câu hỏi: Nêu đặc điểm cấu tạo phân tử hợp chất hữu cơ?
Trả lời:
Đặc điểm cấu tạo phân tử hợp chất hữu cơ:
- Hóa trị và liên kết giữa các nguyên tử:
+ Trong các hợp chất hữu cơ, cacbon luôn có hóa trị IV, hiđro có hóa trị I, oxi có hóa trị II.
+ Mỗi hóa trị được biểu diễn bằng một gạch nối giữa hai nguyên tử liên kết.
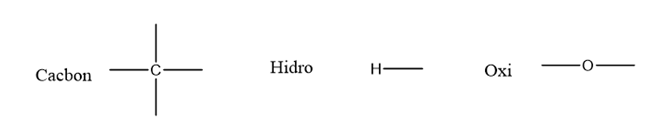
+ Các nguyên tử liên kết với nhau theo đúng hóa trị của chúng. Mỗi liên kết được biểu thị bằng một nét gạch nối giữa hai nguyên tử:
+ Ví dụ với phân tử CH4:
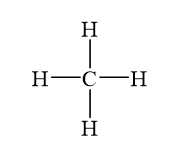
- Mạch cacbon:
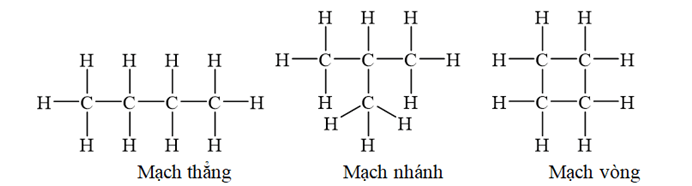
+ Trong hợp chất hữu cơ, các nguyên tử cacbon có thể liên kết trực tiếp với nhau tạo thành mạch cacbon.
+ Có 3 loại mạch cacbon là mạch không phân nhánh (mạch thẳng), mạch nhánh và mạch vòng.
- Trật tự liên kết giữa các nguyên tử trong phân tử
Mỗi hợp chất hữu cơ có một trật tự liên kết xác định giữa các nguyên tử trong phân tử.
Ví dụ:
Cùng công thức phân tử C2H6O nhưng trật tự liên kết giữa các nguyên tử khác nhau, tạo thành hai hợp chất khác nhau là rượu etylic và đimetyl ete.
I. Phân loại hợp chất hữu cơ
Nhóm chức
Khái niệm về các nhóm chức là trung tâm trong hóa học hữu cơ, vừa là phương tiện để phân loại các cấu trúc, vừa để dự đoán các thuộc tính của hợp chất. Một nhóm chức là một mô-đun phân tử, và khả năng phản ứng của nhóm chức đó được giả định, trong giới hạn, giống hệt nhau giữa nhiều loại phân tử. Các nhóm chức quyết định các tính chất hóa học và vật lý của các hợp chất hữu cơ. Các phân tử được phân loại dựa trên cơ sở các nhóm chức của chúng. Rượu, ví dụ: tất cả đều có nhóm C-O-H. Tất cả các loại rượu đều có xu hướng ưa nước, thường tạo thành este và thường có thể được chuyển đổi thành các halogen tương ứng. Hầu hết các nhóm chức có tính chất dị hợp tử (các nguyên tử khác với C và H). Các hợp chất hữu cơ được phân loại theo các nhóm chức bao gồm, rượu, axit cacboxylic, amin, vv.
Hợp chất không vòng
Các hydrocarbon không vòng được chia thành ba nhóm dãy đồng đẳng theo trạng thái bão hòa của chúng:
+ ankan (parafin): hydrocarbon không vòng, không có liên kết đôi hoặc ba, chỉ có liên kết đơn C-C, C-H
+ anken (olefin): hydrocarbon không vòng có chứa một hoặc nhiều liên kết đôi, tức là di-olefin (dien) hoặc poly-olefin.
+ alkynes: hydrocarbon không vòng có một hoặc nhiều liên kết ba.
Phần còn lại của nhóm được phân loại theo các nhóm chức năng có mặt. Các hợp chất này có thể là "chuỗi thẳng", mạch nhánh hoặc mạch vòng. Mức độ phân nhánh ảnh hưởng đến các đặc điểm, chẳng hạn như số octan hoặc số cetane trong hóa học dầu khí.
Hợp chất thơm
Hydrocarbon thơm chứa liên kết đôi liên hợp. Điều này có nghĩa là mọi nguyên tử cacbon trong vòng được lai hóa sp2, tăng tính ổn định. Ví dụ quan trọng nhất là benzen, cấu trúc được phát hiện ra bởi Kekulé, người đầu tiên đề xuất nguyên tắc phân định hoặc cộng hưởng để giải thích cấu trúc của nó. Đối với các hợp chất vòng "thông thường", mùi thơm được tạo ra bởi sự có mặt của các electron pi 4n + 2 bất định, trong đó n là một số nguyên. Sự không ổn định đặc biệt (tính không thơm) được cho là do sự hiện diện của các electron pi liên hợp 4n.
Hợp chất dị vòng
Các đặc tính của hydrocarbon mạch vòng một lần nữa bị thay đổi nếu có các dị hợp tử, có thể tồn tại dưới dạng các nhóm thế gắn vào vòng ở bên ngoài (exocyclic hay ngoại vòng) hoặc là thành viên của chính mạch vòng đó (endocyclic hay nội vòng). Ở trường hợp sau, vòng này được gọi là một dị vòng. Pyridine và furan là những ví dụ về dị vòng thơm trong khi piperidine và tetrahydrofuran là các dị vòng tương ứng. Các dị hợp tử của các phân tử dị vòng nói chung có thể là oxy, lưu huỳnh hoặc nitơ, nguyên tố cuối đặc biệt phổ biến trong các hệ thống sinh hóa.
Dị vòng thường được tìm thấy trong một loạt các sản phẩm bao gồm thuốc nhuộm anilin và thuốc. Ngoài ra, chúng phổ biến trong một loạt các hợp chất sinh hóa như alkaloids, vitamin, steroid và axit nucleic (ví dụ: DNA, RNA).
Các vòng có thể hợp nhất với các vòng khác với một cạnh để tạo ra các hợp chất đa vòng. Các nucleoside thuộc nhóm purine là dị vòng thơm đa vòng đáng chú ý. Các vòng cũng có thể hợp nhất trên một "góc" sao cho một nguyên tử (hầu như luôn luôn là cacbon) có hai liên kết với một vòng và hai liên kết với vòng kia. Các hợp chất như vậy được gọi là hợp chất xoắn hay hợp chất spiro và nó rất quan trọng trong một số sản phẩm tự nhiên.
Polyme
Một tính chất quan trọng của cacbon là nó dễ dàng tạo thành chuỗi, hoặc mạng, được liên kết bởi các liên kết cacbon-cacbon. Quá trình liên kết được gọi là trùng hợp, trong khi các chuỗi, hoặc mạng, được gọi là polyme. Các hợp chất nguồn được gọi là một monome.
Hai nhóm polyme chính tồn tại: polyme tổng hợp và polyme sinh học. Polyme tổng hợp được sản xuất nhân tạo và thường được gọi là polyme công nghiệp. Polyme sinh học xảy ra trong một môi trường tự nhiên, hoặc không có sự can thiệp của con người.
Các polyme hữu cơ tổng hợp phổ biến là polyetylen (polythene), polypropylen, ni lông, polytetra floetylen (PTFE), polystyren, polyesters, polymethylmethacrylate (được gọi là Perspex và plexiglas), và polyvinyl chloride (PVC).
II. Đặc điểm chung của hợp chất hữu cơ
- Hợp chất hữu cơ nhất thiết phải chứa C, hay có H thường gặp O ngoài ra còn có halogen, N, P...
- Liên kết chủ yếu trong hợp chất hữu cơ là liên kết cộng hóa trị.
- Các hợp chất hữu cơ thường dễ bay hơi, dễ cháy, kém bền nhiệt.
- Các phản ứng trong hoá học hữu cơ thường chậm, không hoàn toàn, xảy ra theo nhiều hướng thường phải đun nóng và có xúc tác.
III. Chất vô cơ và chất hữu cơ có những điểm gì khác nhau?
|
Bảng so sánh điểm khác nhau giữa chất vô cơ và chất hữu cơ |
||
|
Yếu tố so sánh |
Chất vô cơ |
Chất hữu cơ |
|
Thành phần nguyên tố |
Có đa dạng các nguyên tố. |
Chủ yếu là các nguyên tố C, H, O, N. |
|
Tính chất vật lý chung |
Đều không cháy. Chịu được nhiệt độ cao và dẫn điện tốt. |
Đa phần là cháy được và dễ cháy. Chịu nhiệt kém, dễ bay hơi và dẫn điện kém. |
|
Tính chất hóa học |
Thường phản ứng nhanh. Tính chất hóa học cụ thể sẽ phụ thuộc vào các hợp chất khác nhau như muối, axit, bazo. |
Thường xảy ra chậm và theo nhiều chiều hướng khác nhau trong cùng một điều kiện. Sản phẩm tạo ra thường là hỗn hợp các chất. |
|
Sự phân ly |
Phần lớn là phân ly thành dạng ion trong các dung dịch. |
Rất ít hoặc hầu như không phân ly thành các ion. |
|
Sự có mặt |
Trong các khoáng vật tự nhiên hay được tổng hợp nhân tạo. |
Là các phân tử protein, chất béo, cacbohydrat. |
|
Ứng dụng trong nông nghiệp |
Sử dụng để sản xuất phân bón vô cơ. |
Sử dụng để sản xuất phân bón hữu cơ. |
-------------------------------
Ngoài Đặc điểm cấu tạo phân tử hợp chất hữu cơ đã được VnDoc giới thiệu, mời các bạn cùng tham khảo thêm Chuyên đề Hóa học lớp 9, Trắc nghiệm Hóa học 9, Lý thuyết môn Hóa học lớp 9 để hoàn thành tốt chương trình học THCS.
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu học tập THCS miễn phí trên Facebook: Tài liệu học tập lớp 9. Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu mới nhất.

