Các dạng bài tập hóa 10 từ khó đến nâng cao
Chúng tôi xin giới thiệu bài Các dạng bài tập hóa 10 từ khó đến nâng cao được VnDoc sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy. Nội dung tài liệu sẽ giúp các bạn học sinh học tốt môn Hóa học lớp 10 hiệu quả hơn. Mời các bạn tham khảo.
Các dạng bài tập hóa 10
I. Dạng 1: Tính độ hòa tan của một chất tan trong dung dịch
Phân biệt nồng độ phần trăm và độ hòa tan, nồng độ phần trăm và nồng độ mol là một dạng toán khá thường gặp. Chúng ta cần tìm hiểu một số công thức quan trọng trước khi tiền hành làm dạng bài tập này:
- Nồng độ phần trăm:
![]()
- Độ hòa tan:
![]()
- Nồng độ mol:
![]()
- Mối liên hệ giữa C% và

Sau khi đã tìm hiểu những công thức có thể vận dụng vào dạng bài tập này thì các bước giải sẽ là những điều cần nhớ tiếp theo với các bạn. Phương pháp giải dạng bài tập tính độ hòa tan của một chất ở trong dung dịch như sau:
- Thực hiện việc tính khối lượng của chất tan ở trong tinh thể dạng thể ngậm nước.
- Thực hiện việc tính khối lượng của tinh thể.
- Tiếp đến là tính khối lượng của chất tan.
- Sử dụng quy tắc tam suất để tiến hành lập luận và đưa ra đáp án phù hợp nhất, thỏa mãn đề bài đã cho
Ví dụ 1: Ở 20oC, hòa tan 14,36g muối ăn vào 40g H2O được dung dịch bão hòa. Tính độ tan, nồng độ phần trăm của dung dịch bão hòa của muối ăn:
Giải:
Độ hòa tan của NaCl ở 20oC là:
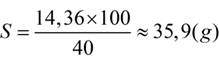
Nồng độ phần trăm của dung dịch bão hòa sẽ là:

Đáp số:
- Độ tan muối: 35.9
- Nồng độ % của dd bão hòa: 26.4%
Ví dụ 2: Tính khối lượng CuSO4 trong 500g CuSO4.5H2O (Bài toán thiên về muối ngậm nước)
Giải
![]()
- Cứ 250g tinh thể có 160g CuSO4
- Khi đó 500g tinh thể sẽ có 320 g CuSO4
Khối lượng CuSO4 trong tinh thể là:

Bài tập vận dụng
- Tính độ tan của muối ăn ở 20oC, biết rằng ở nhiệt độ đó 50 gam nước hòa tan tối đa 17,95 gam muối ăn
- Có bao nhiêu gam muối ăn trong 5 kg dung dịch bão hòa muối ăn ở 20oC, biết độ tan của muối ăn ở nhiệt độ đó là 35, 9 gam .
- Độ tan của A trong nước ở 10oC là 15 gam , ở 90oC là 50 gam. Hỏi làm lạnh 600 gam dung dịch bão hòa A ở 90oC xuống 10oC thì có bao nhiêu gam A kết tinh ?
- Có bao nhiêu gam tinh thể NaCl tách ra khi làm lạnh 1900 gam dung dịch NaCl bão hòa từ 90oC đến 0oC . Biết độ tan của NaCl ở 90oC là 50 gam và ở 0 oC là 35 gam
- Xác định lượng AgNO3tách ra khi làm lạnh 2500 g dung dịch AgNO3bão hòa ở 60oC xuống còn 10oC. Cho biết độ tan của AgNO3 ở 60oC là 525 g và ở 10oC là 170 g .
II. Dạng 2: Tính số oxi hóa của các hợp chất
Để làm tốt dạng bài tập này ta cần nắm vững một số qui tắc như sau:
- Số oxi hóa của đơn chất, hợp chất bằng không.
- Số oxi hóa ion: bằng điện tích ion đấy
Trong hợp chất hoặc ion đa nguyên tử:
- Số oxi hóa của H, kim loại kiềm là +1
- Số oxi hóa của O là -2
Ngoài ra, cần lưu ý một số trường hợp đặc biệt về số oxi hóa:
- Trong FeS2, H2S2 số oxi hóa của S là -1
- Trong peroxit, Na 2O2, BaO2, H2O2 số oxi hóa của O là -1
- Trong Fe3O4 số oxi hóa của Fe là +8/3
Ví dụ 1: Tính số oxi hóa của Mn trong KMnO4 của S trong SO42-
Giải
KMnO4 có số oxi hóa bằng 0. Đặt x là số oxi hóa của Mn. Ta lập phương trình như sau:
1+ x + 4x(-2) = 0 → x = +7
SO42- có số oxi hóa -2. Đặt x là số oxi hóa của S, lập phương trình:
x+4x(-2) = -2→ x = +6
Lưu ý:
- Số oxi hóa là điện tính hình thức, không phải hóa trị thực sự của nguyên tố đó trong hợp chất.
- Số oxi hóa là điện tích hình thức nên có thể nguyên, không nguyên, dương, âm hoặc bằng không.
- Trong nhiều trường hợp, giá trị tuyệt đối của số oxi hóa bằng giá trị hóa trị.
- Vì số oxi hóa là số đại số nên khi viết số oxi hóa ta đặt dấu (+) hoặc (-) trước con số; còn khi viết ion ta đặt dấu (+) hoặc (-) sau con số.
- Số oxi hóa dương cực đại trùng với số thứ tự nhóm của nguyên tố đó trong bảng tuần hoàn.
Các quy tắc trên sẽ giúp chúng ta rất nhiều trong quá trình xác định số oxi hóa của một số hợp chất phức tạp. Không còn thắc mắc trong quá trình xác định số oxi hóa khử.
Một số quy tắc khi cân bằng:
- Quy tắc số 1: Cân bằng số nguyên tử trước khi cân bằng số oxi hóa.
- Quy tắc số 2: Nếu một hợp chất có nhiều nguyên tố thay đổi oxi hóa thì ta tính sự tăng hoặc giảm số oxi hóa của từng nguyên tố rồi ghép lại thành sự tăng hoặc giảm số oxi hóa của hơp chất.
- Quy tắc số 3: Ta có thể cân bằng theo phương pháp thăng bằng electron nghĩa là sau khi cân bằng quá trình oxi hóa bằng quá trình khử xong ta cân bằng điện tích hai vế.
- Quy tắc số 4: Chỉ có thành phần nào trong hợp chất hữu cơ có thay đổi số oxi hóa thì mới tính số oxi hóa và nên lập sơ đồ nhường, nhận electron để dễ cân bằng.
III. Dạng 3: Tách chất ra khỏi hỗn hợp
Trường hợp 1: Tách khí CO 2: Cho hỗn hợp có khí CO 2 vào dung dịch Ca(OH) 2 có dư, CO 2 tạo kết tủa CaCO3. Lọc, nung CaCO3 ở nhiệt độ cao để thu lại CO 2
Các phương trình phản ứng diễn ra trong quá trình tách chất gồm:
CO 2 + Ca(OH) 2 → CaCO3 + H 2O
CaCO3 → CaO + CO 2 (to)
Trường hợp 2: Tách khí NH3: Cho hỗn hợp khí có NH3 vào dung dịch HCl tạo muối NH4.Cl. Cô cạn rồi nung muối NH4Cl thu lại NH3
Các phương trình phản ứng diễn ra trong quá trình tách chất gồm:
NH3 + HCl → NH4Cl
NH4Cl → NH3 + HCl (to)
Trường hợp 3: Tinh chế muối Nacl có lẫn các chất khác: Dùng các phản ứng hóa học để chuyển các chất khác thành NaCl rồi cô cạn dung dịch để được muối NaCl nguyên chất.
Ví dụ: Tinh chế NaCl có lẫn NaBr, NaI, Na2CO3
Ta thực hiện các bước sau đây:
Hòa tan hỗn hợp vào nước tạo dung dịch hỗn hợp NaCl, NaBr, NaI, Na2CO3.
Thổi khí HCl vào chỉ có Na2CO3 phản ứng thu được là:
Na2CO3 + 2HCl → 2NaCl + H2O + CO2
Thổi tiếp Cl2 có dư vào ta có các phản ứng sau:
2NaBr + Cl2 → 2NaCl + Br2
2NaI + Cl2 → 2NaCl + I2
Cô cạn dung dịch H2O, Br2, I2 bay hơi hết còn lại NaCl nguyên chất. Đến đây thì quá trình tinh chế NaCl đã hoàn tất.
IV. Dạng 4: Bài tập hiệu suất phản ứng
Trong phản ứng: Nguyên liệu A → Sản phẩm B ta có thực hiện tính một số loại hiệu suất như sau:
- Hiệu suất tính theo sản phẩm
- Hiệu suất tính theo nguyên liệu
- Hiệu suất tính theo chuỗi quá trình
- Hiệu suất chung của chuỗi quá trình
Trong phản ứng: Nguyên liệu A → Sản phẩm B ta có thực hiện tính một số loại hiệu suất như sau:
- Hiệu suất tính theo sản phẩm
- Hiệu suất tính theo nguyên liệu
- HIệu suất tính theo chuỗi quá trình
- Hiệu suất chung của chuỗi quá trình
Hiệu suất tính theo sản phẩm
![]()
Hiệu suất tính theo nguyên liệu
![]()
Tính hiệu suất theo chuỗi quá trình
![]()
Hiệu suất chung của chuỗi quá trình là
![]()
Ví dụ 1: Khi nung 200g CaCO3 thu 44g CO2. Tính hiệu suất phản ứng điều chế CO2 từ CaCO3?
Giải
CaCO3 → CaO + CO2
100g 44g

Vậy hiệu suất của quá trình điều chế CO2 từ CaCO3 là 50%.
Một số lưu ý khi làm các dạng bài tập hóa 10
Một vài chia sẻ dưới đây sẽ giúp các bạn chinh phục các dạng bài tập hóa 10 tốt hơn.
- Luôn ôn tập lại lý thuyết trước khi làm bài tập
Để làm được bài tập thì lý thuyết là điều các bạn cần phải nắm vững trước tiên. bạn sẽ chẳng thể nào giải quyết được một phương trình nho nhỏ nếu như không nhớ được hóa trị hay cách cân bằng phương trình cả. Vì thế mà việc ôn tập lý thuyết luôn luôn cần được ưu tiên trước khi tiến hành làm các bài tập vận dụng.
- Phân biệt đúng các dạng và các chất
Hóa học là môn học mà các chất sẽ có những sự biến đổi dựa trên nhiều điều kiện và yếu tố khác nhau. Các dạng bài tập cũng sẽ có sự linh hoạt trong cách giải tùy thuộc vào sự thay đổi của các chất. Vì thế mà việc xác định đúng dạng bài tập và đúng chất là điều quan trọng để định hướng cách giải tốt nhất.
- Cẩn thận trong từng bước tính toán
Hóa học không đơn giản là bạn tính các con số về khối lượng mà bạn có thể sẽ phải tính nhiều loại số khác nhau, như số mol, số e, hóa trị hay số nguyên tử để cân bằng,... Vì thế mà mỗi một công đoạn tính toán đều cần được chính xác tuyệt đối, bỏi nếu bạn sai 1 chỗ thôi, có thể rất nhỏ thì khả năng sai cả bài của bạn cũng sẽ rất lớn.
- Thường xuyên luyện tập để thành thạo hơn
Sẽ không có cách nào giúp bạn ghi nhớ và có thêm nhiều kiến thức cũng như thành thạo các quy trình giải bài tập hóa 10 bằng cách luyện tập thường xuyên. Việc làm nhiều sẽ giúp bạn hình thành được phản ứng nhanh hơn với các dạng bài tập tương tự
----------------------------------------
Trên đây VnDoc đã giới thiệu tới các bạn nội dung bài Các dạng bài tập hóa 10 từ khó đến nâng cao. Để có kết quả học tập tốt và hiệu quả hơn, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Hóa học 10, Chuyên đề Vật Lý 10, Chuyên đề Hóa học 10, Giải bài tập Toán 10. Tài liệu học tập lớp 10 mà VnDoc tổng hợp biên soạn và đăng tải.






