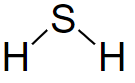
Công thức cấu tạo H2S
Công thức cấu tạo H2S được chúng tôi sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy. Nội dung tài liệu sẽ giúp các bạn học sinh học tốt môn Hóa học lớp 10 hiệu quả hơn. Mời các bạn tham khảo.
Công thức cấu tạo H2S
Câu hỏi: Công thức cấu tạo H2S
Trả lời:
Công thức cấu tạo H2S là:
1. H2S là gì?
♦ Khí H2S hay khí Hiđro sunfua không màu, có mùi trứng thối và nặng hơn không khí (d ≈ 1,17). Hóa lỏng ở nhiệt độ −60oC và hóa rắn ở −86oC.
♦ H2s có tan trong nước không: Khí H2S có thể tan trong nước, H2S có độ tan S = 0,38g/100g H2O ở mức nhiệt 20oC và 1atm
2. Tính chất vật lý
- Hiđro sunfua (H2S) là chất khí rất độc, không màu, mùi trứng thối, nặng hơn không khí.
- Hóa lỏng ở -60oC, hóa rắn ở -86oC.
- Độ tan trong nước S = 0,38g/100g H2O (ở 20oC, 1atm).
3 . Tính chất hóa học
3.1.Tính axit yếu
- Hiđro sunfua tan trong nước tạo thành dung dịch axit rất yếu (yếu hơn axit cacbonic), có tên là axit sunfuhiđric (H2S).
- Axit sunfuhiđric tác dụng với kiềm tạo nên 2 loại muối: muối trung hòa, như Na2S chứa ion S2− và muối axit như NaHS chứa ion HS−.
3.2. Tính khử mạnh
Trong hợp chất H2S, nguyên tố lưu huỳnh có số oxi hóa thấp nhất là −2. Khi tham gia phản ứng hóa học, tùy thuộc vào bản chất và nồng độ của chất oxi hóa, nhiệt độ,… mà nguyên tố lưu huỳnh có số oxi hóa −2 (S−2) có thể bị oxi hóa thành lưu huỳnh tự do (S0), hoặc lưu huỳnh có số oxi hóa +4 (S+4), hoặc lưu huỳnh có số oxi hóa +6 (S+6). Vì vậy, hiđro sunfua có tính khử mạnh.
Các thí dụ sau đây chứng minh cho tính khử của hiđro sunfua.
- Hidrosunfua tác dụng với oxi:
+ Dung dịch axit sunfuhiđric tiếp xúc với không khí, nó dần trở nên vẩn đục màu vàng, do oxi của không khí đã oxi hóa H2S thành S0:
2H2S + O2 → 2H2O +2S
- Ở nhiệt độ cao, khí H2S cháy trong không khí với ngọn lửa xanh nhạt, H2S bị oxi hóa thành SO2:
Nếu không cung cấp đủ không khí hoặc ở nhiệt độ không cao lắm thì H2S bị oxi hóa thành S0:
- Clo có thể oxi hóa H2S thành H2SO4:
H2S + 4Cl2+ 4H2O → H2SO4 + 8HCl
4. Trạng thái tự nhiên, điều chế
4.1. Trạng thái tự nhiên
- Trong tự nhiên, hiđro sunfua có trong một số nước suối, trong khí núi lửa, khí thoát ra từ chất protein bị thối rữa,...
4.2. Điều chế
- Trong công nghiệp không sản xuất hiđro sunfua. Trong phòng thí nghiệm điều chế bằng phản ứng của dung dịch axit clihiđric với sắt (II) sunfua:
FeS + 2HCl → FeCl2 + H2S↑
5. Tính chất của muối sunfua
- Muối sunfua của các kim loại nhóm IA, IIA (trừ Be) như Na2S, K2S tan trong nước và tác dụng với các dung dịch axit HCl, H2SO4 loãng sinh ra khí H2S:
Na2S + 2HCl → 2NaCl + H2S↑
- Muối sunfua của một số kim loại nặng như PbS, CuS, ... không tan trong nước, không tác dụng với dung dịch HCl, H2SO4 loãng.
- Muối sunfua của những kim loại còn lại như ZnS, FeS, ... không tan trong nước, nhưng tác dụng với dung dịch HCl, H2SO4 loãng sinh ra khí H2S:
ZnS + 2H2SO4 → ZnSO4 + H2S↑
- Một số muối sunfua có màu đặc trưng: CdS màu vàng, CuS, FeS, Ag2S, ... màu đen.
----------------------------------------
Trên đây VnDoc đã giới thiệu tới các bạn nội dung bài Công thức cấu tạo H2S. Để có kết quả học tập tốt và hiệu quả hơn, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Hóa học 10, Chuyên đề Vật Lý 10, Chuyên đề Hóa học 10, Giải bài tập Toán 10. Tài liệu học tập lớp 10 mà VnDoc tổng hợp biên soạn và đăng tải.