C2H4 + HCl → C2H5Cl
Ethylene HCl: C2H4 ra C2H5Cl
C2H4 + HCl → C2H5Cl được VnDoc biên soạn hướng dẫn các bạn học sinh viết và cân bằng đúng phương trình phản ứng khi cho C2H4 tác dụng với HCl thu được C2H5Cl.
1. Phương trình phản ứng C2H4 ra C2H5Cl
C2H4 + HCl → C2H5Cl
2. Điều kiện đề C2H4 tạo ra C2H5Cl
Ánh sáng khuyếch tán
3. Tính chất hóa học của Ethylene
CTCT:
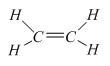
3.1. Tác dụng với dung dịch Br2
Ở phản ứng này, một liên kết kém bền trong liên kết đôi bị đứt ra và phân tử etilen kết hợp thêm một phân tử brom.
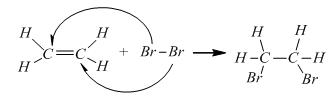
Phương trình hóa học: C2H4 + Br2 → C2H4Br2
Dung dịch Br2 ban đầu có màu vàng nâu. Sục khí Ethylene vào dung dịch => dung dịch mất màu
3.2. Phản ứng cộng với các chất khác như HCl, H2
Ngoài brom, trong những điều kiện thích hợp, Ethylene còn có phản ứng cộng vởi một số chất khác như: H2, Cl2, HCl...
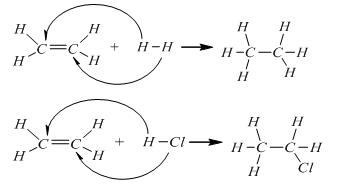
Phản ứng cộng acid
CH2= CH2 + HCl (khí) → CH3CH2Cl
C2H4 + HBr → C2H5Br
Phản ứng cộng nước (có điều kiện nhiệt độ và sự xúc tác của acid)
C2H4 + H2O → C2H5OH
3.3. Phản ứng cháy
Tác dụng với oxygen: Khi đốt trong oxygen, Ethylene cháy tạo thành khí CO2 và H2O, tỏa nhiều nhiệt.
![]()
Tổng quát: ![]()
* Đốt cháy alkene cho ![]()
3.3. Phản ứng trùng hợp
Khi có xúc tác và nhiệt độ thích hợp, liên kết kém bền trong phân tử etilen bị đứt ra làm cho các phân tử etilen kết hợp với nhau, tạo thành chất có phân tử lượng rất lớn gọi là polyethylene. Phản ứng đó gọi là phản ứng trùng hợp.
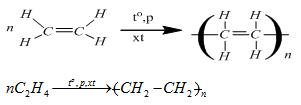
Tham khảo thêm các phản ứng hóa học khác của C2H4:
3C2H4 + 2KMnO4 + 4H2O → 3C2H6O2 + 2KOH + 2MnO2
C2H4 + 2Na → C2H4Na2
4. Bài tập vận dụng liên quan
Câu 1: Etilen có nhiều tính chất khác vớ Methane như: phản ứng cộng,trùng hợp, oxi hóa là do trong phân tử alkene có chứa:
A. liên kết σ bền.
B. liên kết π
C. liên kết π bền .
D. liên kết π kém bền .
Etilen có nhiều tính chất khác vớ Metan như: phản ứng cộng,trùng hợp,oxi hóa là do trong phân tử alkene có chứa: liên kết π kém bền .
Câu 2: Trong công nghiệp, Ethylene được điều chế bằng cách:
A. tách hydro từ alkane
B. crackinh alkane
C. tách nước từ alcohol
D. a,b đều đúng.
Câu 3: Tính chất nào sau đây không phải là tính chất vật lí của Ethylene?
A. tan trong dầu mỡ
B. nhẹ hơn nước
C. chất không màu
D. tan trong nước
Câu 4: Trong phòng thí nghiệm, Ethylene được điều chế bằng cách:
A. tách hydro từ alkane
B. crackinh alkane
C. tách nước từ alcohol
D. Cracking propane
Trong phòng thí nghiệm etilen được điều chế bằng cách đun nóng ethyl alcohol với H2SO4 đậm đặc
Phản ứng điều chế C2H4 từ C2H5OH
C2H5OH → C2H4 + H2O
Câu 5: Sản phẩm trùng hợp etilen là:
A. Polyvinyl chloride
B. Polyethylene
C. Poliepilen
D. Polypropylene
Câu 6. Khi dẫn khí C2H4 vào dung dịch Bromine (dư) đựng trong ống nghiệm có thể quan sát thấy
A. màu của dung dịch bromine nhạt dần, có chất kết tủa
B. màu của dung dịch bromine nhạt dần, có chất lỏng không tan chìm dưới đáy ống nghiệm.
C. màu của dung dịch bromine nhạt dần, có khí thoát ra.
D. màu của dung dịch bromine không thay đổi
Dẫn khí etilen qua dung dịch brom dư. Hiện tượng quan sát được là: Màu vàng của dung dịch nhạt hơn lúc đầu
C2H4 + Br2 → C2H4Br2
Vì Br2 dư nên dung dịch không trong suốt mà chỉ nhạt màu
Câu 7. Dãy sau đây gồm các chất tác dụng được với etilen trong điều kiện thích hợp?
A. Hydrogen, nước, oxygen, bromine, Hydrogen bromide
B. Hydrogen, nước, oxygen, bromine, Sodium hydroxide
C. Hydrogen, nước, oxygen, bromine, Carbonic acid
D. Hydrogen, nước, oxygen, bromine, Acetic Acid
C2H4 + H2 → C2H6
C2H4 + H2O ![]() C2H5OH
C2H5OH
C2H4 + 3O2 ![]() 2CO2 + 2H2O
2CO2 + 2H2O
C2H4 + Br2 → C2H4Br2
C2H4 + HBr → C2H5Br
Câu 8. Dẫn m gam hỗn hợp gồm metan và etilen đi qua dung dịch nước brom thì thấy lượng brom tham gia phản ứng là 8 gam. Khí bay ra được đốt cháy hoàn toàn và dẫn sản phẩm cháy đi qua dung dịch Ba(OH)2 dư thì thu được 29,55 gam kết tủa. Giá trị của m là:
A. 4 gam
B. 2,2 gam
C. 3,8 gam
D. 2,8 gam
nCO2 = nBaCO3 = 29,55/(137 + 12 +16.3) = 0,15 (mol)
nBr2 = 0,05 mol
C2H4 + Br2 → C2H4Br2
0,05________0,05
⇒ nCH4 + 2nC2H4 = nCO2
⇔ nCH4 + 0,05.2 = 0,15(mol)
⇒ nCH4 = 0,05 (mol)
m = mCH4 + mC2H4
⇔ mkhí = 0,05.16 + 0,05.28 = 2,2 (g)
Câu 9. Phát biểu nào dưới đây không đúng:
A. Điều chế etilen trong phòng thí nghiệm bằng cách đun etylic với H2SO4đặc tới khoảng 170oC
B. Tất cả các ancol khi đun nóng với H2SO4 đặc tới khoảng 170oC đều thu được anken
C. Đun nóng ancol với H2SO4đặc ở nhiệt độ khoảng 140oC sẽ thu được ete
D. Đun nóng propan-1-ol với H2SO4 đặc ở nhiệt độ 170oC chỉ thu được 1 olefin duy nhất
Câu 10. Phương pháp điều chế etilen trong phòng thí nghiệm là:
A. Crackinh ankan.
B. Cho C2H2 tác dụng với H2, xúc tác Pd/PbCO3.
C. Tách H2 từ etan.
D. Đun C2H5OH với H2SO4 đặc ở 170oC.
Phương pháp điều chế ethylene trong phòng thí nghiệm là đun C2H5OH với H2SO4 đặc ở 170oC.
..............................................
