CH3COONa + NaOH → CH4 + Na2CO3
Sodium acetate ra Methane: Điều chế Methane trong phòng thí nghiệm
CH3COONa + NaOH → CH4 + Na2CO3 được VnDoc biên soạn hướng dẫn các bạn viết và cân bằng phương trình hóa học, đây cũng là phương trình hóa học điều chế khí methane, từ CH3COONa ra CH4.
1. Phương trình điều chế Methane trong phòng thí nghiệm
CH3COONa + NaOH → CH4 + Na2CO3
2. Điều kiện phản ứng CH3COONa ra CH4
Nhiệt độ: nhiệt độ Xúc tác: CaO
3. Cách tiến hành phản ứng điều chế CH4 trong phòng thí nghiệm
Methane được điều chế bằng cách đun nóng natri axetat khan với hỗn hợp vôi tôi xút.
4. Điều chế Methane trong phòng thí nghiệm
Điều chế Metan CH4 trong phòng thí nghiệm
4. 1. Hóa chất và dụng cụ
Hóa chất: CH3COONa, NaOH, CaO, H2O
Dụng cụ: ống nghiệm, giá đỡ, chậu thủy tinh, nút cao su, ống dẫn khí bằng thủy tinh, đèn cồn.
4.2. Phương pháp thu khí Methane
Sử dụng phương pháp đẩy nước, vì Methane là chất khí ít tan được trong nước.
4.3. Điều kiện xảy ra phản ứng.
Điều kiện đun nóng hỗn hợp, có xúc tác CaO
4.4. Cách thực hiện thí nghiệm
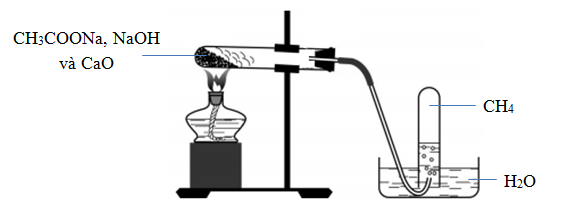
4.5. Phương trình điều chế CH4 trong phòng thí nghiệm
CH3COONa + NaOH → CH4 + Na2CO3
5. Câu hỏi vận dụng liên quan
Câu 1: Phản ứng hóa học đặc trưng của Methane là:
A. Phản ứng thế.
B. Phản ứng cộng.
C. Phản ứng oxi hóa – khử.
D. Phản ứng phân hủy.
Câu 2. Các tính chất vật lí cơ bản của Methane là:
A. Chất lỏng, không màu, tan nhiều tron nước
B. Chất khí, không màu, không mùi, nhẹ hơn không khí, tan ít trong nước
C. Chất khí không màu, tan nhiều trong nước
D. Chất khí không màu, không mùi, nặng hơn không khí, tan ít trong nước
Các tính chất vật lí cơ bản của Methane là:
B. Chất khí, không màu, không mùi, nhẹ hơn không khí, tan ít trong nước
Câu 3: Trong phòng thí nghiệm có thể thu khí CH4 bằng cách:
A. Đẩy không khí (ngửa bình)
B. Đẩy acid
C. Đẩy nước (úp bình)
D. Đẩy base
CH4 không tan trong nước nên cần phải thu bằng phương pháp đẩy nước.
Câu 4: Để chứng minh sản phẩm của phản ứng cháy giữa Methane và oxygen có tạo thành khí carbonic hay không ta cho vào ống nghiệm hóa chất nào say đây?
A. Nước cất
B. Nước vôi trong
C. Nước muối
D. Thuốc tím
Khi cho nước vôi trong Ca(OH)2 vào ống nghiệm thấy dung dịch bị vẩn đục chứng tỏ có khí CO2. CO2 phản ứng với Ca(OH)2 tạo kết tủa làm dung dịch bị vẩn đục.
Câu 5: Điều kiện để phản ứng giữa Methane và Chlorine xảy ra là:
A. Có bột sắt làm xúc tác
B. Có acid làm xúc tác
C. Có nhiệt độ
D. Có ánh sáng
Điều kiện để phản ứng giữa Methane và Chlorine xảy ra là:
Có ánh sáng
Câu 6: Dẫn khí Methane và khí chlorine vào ống nghiệm, đặt ngoài ánh sáng. Sau đó, đưa mảnh giấy quỳ tím ẩm vào ống nghiệm. Hiện tượng quan sát được là:
A. Quỳ tím chuyển thành màu xanh
B. Quỳ tím bị mất màu
C. Quỳ tím chuyển thành màu đỏ
D. Quỳ tím không đổi màu
Câu 7: Đốt cháy hoàn toàn 3,4 gam hỗ hợp CH4 và H2 thì thu được 12,395 lít hơi H2O (đkc). Thành phần phần trăm theo khối lượng của mỗi khí trong hỗn hợp ban đầu là:
A. 90% CH4 và 10% H2
B. 60% CH4 và 40% H2
C. 94,12% CH4 và 5,88% H2
D. 91,12% CH4 và 8,88% H2
nH2O = 12,395/24,79 = 0,5 mol
CH4 + 2O2 ![]() \(\overset{t^{o} }{\rightarrow}\)CO2 + 2H2O
\(\overset{t^{o} }{\rightarrow}\)CO2 + 2H2O
x------------------------>2x
2H2 + O2 ![]() \(\overset{t^{o} }{\rightarrow}\)2H2O
\(\overset{t^{o} }{\rightarrow}\)2H2O
y----------------->y
Ta có:
16x + 2y = 3,42
x + y = 0,5
x = 0,2 mol
y = 0,1 mol
=> %CH4 = (0,2.16)/3,4.100%= 94,12 %
=>%H2 = 100 % - 94,12% = 5,88%
Câu 8. Khi clo hóa một ankan có công thức phân tử C6H14, người ta chỉ thu được 2 sản phẩm thế monoclo. Danh pháp IUPAC của alkane đó là :
A.2,2-dimethylbutane.
B.2-methylpentane.
C.n-hexane.
D.2,3-dimethylbutane.
Viết đồng phân alkane
Xét các vị trí thế chlorine của mỗi đồng phân
Vì clo hóa một alkane có công thức phân tử C6H14, chỉ thu được 2 sản phẩm thế monoclor
=> Danh pháp IUPAC của alkane
Câu 9. Các tính chất vật lí cơ bản của methane là:
A. Chất lỏng, không màu, tan nhiều tron nước
B. Chất khí, không màu, không mùi, nhẹ hơn không khí, tan ít trong nước
C. Chất khí không màu, tan nhiều trong nước
D. Chất khí không màu, không mùi, nặng hơn không khí, tan ít trong nước
Câu 10. Chọn phát biểu đúng? Chọn phát biểu đúng?
A. Chất béo là trieste của glycerol với acid.
B. Chất béo là triete của glycerol với acid vô cơ.
C. Chất béo là trieste của glycerol với acid béo
D. Chất béo là trieste của alcohol với acid béo.
Câu 11. Cho dung dịch acetic Acid nồng độ a% tác dụng vừa đủ với dung dịch NaOH nồng độ 20%, thu được dung dịch muối có nồng độ 20,5%. Hãy tính a.
A. 15%
B. 20%
C. 25%
D. 30%
Bài toán dạng này ta sẽ quy ban đầu số mol của NaOH là 1 (mol)
Phương trình hóa học: CH3COOH + NaOH → CH3COONa + H2O
Theo phương trình phản ứng: nCH3COOH = nCH3COONa = nNaOH = 1(mol)
=>mdd NaOH = (1×40)/20%.100% = 200 gam
mddCH3COOH = (1× 60)/a%.100% = 6000/a gam
mddsau = (1×82)/20,5%.100% = 400 (g)
Mà mddsau = mddCH3COOH + mddNaOH
=> 400 = 6000/a + 200
⇒ 200 = 6000/a ⇒ a = 30%
Câu 12. Cho các chất sau: ZnO, Na2SO4, NaOH, K2CO3, Ag, Fe. Số chất có thể tác dụng với dung dịch acetic Acid là
A. 1.
B. 2.
C. 3.
D. 4.
Các chất có thể tác dụng với acetic Acid là: ZnO, NaOH, K2CO3, Fe.
2CH3COOH + ZnO → (CH3COO)2Zn + 2H2O
CH3COOH + NaOH → CH3COONa + H2O
2CH3COOH + K2CO3 → 2CH3COOK + CO2 + H2O
2CH3COOH + Fe → (CH3COO)2Fe + H2
.........................................
