Na2SO3 + H2SO4 → Na2SO4 + SO2 + H2O
H2SO4 ra SO2: Điều chế SO2 trong phòng thí nghiệm
Na2SO3 + H2SO4 → Na2SO4 + SO2 + H2O là phương trình phản ứng điều chế SO2 trong phòng thí nghiệm từ Na2SO4 ra SO2. Với nội dung tài liệu này VnDoc hy vọng bạn đọc có thể viết và cân bằng phương trình phản ứng một cách chính xác.
1. Phương trình phản ứng H2SO4 ra SO2
Na2SO3 + H2SO4 → Na2SO4 + SO2↑ + H2O
2. Điều kiện phản ứng Na2SO3 ra SO2
Nhiệt độ thường
3. Cách tiến hành điều chế SO2 trong phòng thí nghiệm
Trong phòng thí nghiệm, khí SO2 được điều chế bằng cách cho muối sunfit là muối của axit yếu tác dụng với axit mạnh hơn thường là dung dịch axit sunfuric với muối natri sunfit
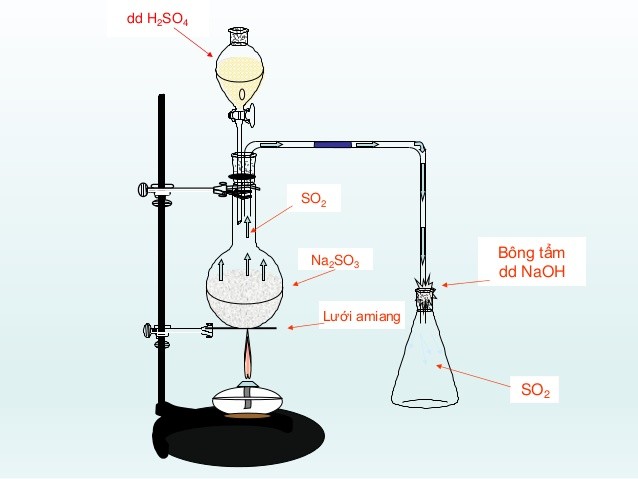
4. Hiện tượng nhận biết phản ứng điều chế lưu huỳnh đioxit
Có khí không màu, mùi hắc thoát ra.
Thu khí lưu huỳnh dioxit bằng phương pháp chuyển không khí. Dùng bông tẩm dung dịch natri hidroxit NaOH để hạn chế lượng khí SO2 thoát ra ngoài. Không dùng bông tẩm khí amoniac NH3 vì nó là khí dễ bay hơi khiến việc thu khí không đạt hiệu quả cao
5. Bài tập vận dụng liên quan
Câu 1. Phản ứng được dùng để điều chế SO2 trong công nghiệp là
A. Na2SO3 + H2SO4 → Na2SO4 + SO2↑ + H2O.
B. Cu + 2H2SO4 đặc, nóng → CuSO4 + SO2 + 2H2O.
C. 4FeS2 + 11O2 → 8SO2 + 2Fe2O3.
D. C + 2H2SO4 đặc → 2SO2 + CO2 + 2H2O.
Câu 2. Dùng hóa chất nào sau đây để nhận biết hai khí SO2 và SO3
A. dung dịch Br2
B. dung dịch NaOH
C. dung dịch nước vôi trong
D. Dung dịch BaCl2
Câu 3. Nhận xét nào sau đây không đúng về SO2?
A. khí này làm mất màu dung dịch nước brom và dung dịch thuốc tím.
B. Phản ứng được với H2S tạo ra S.
C. Liên kết trong phân tử là liên kết cộng hóa trị có cực
D. Được tạo ra khi sục khí O2 vào dung dịch H2S.
Câu 4. Cho các sơ đồ phản ứng sau:
(1) MnO2 + HCl → khí X;
(2) FeS + HCl → khí Y;
(3) Na2SO3 + HCl → khí Z;
(4) NH4HCO3 + NaOH (dư) → khí G.
Những khí sinh ra tác dụng được với NaOH là
A. Y, Z, G.
B. X, Y, G.
C. X, Z, G.
D. X, Y, Z.
(1) MnO2 + 4HCl → MnCl2 + Cl2 (X) + 2H2O
(2) FeS + 2HCl → FeCl2 + H2S (Y)
(3) Na2SO3 + 2HCl → 2NaCl + SO2 (Z) + H2O
(4) NH4HCO3 + 2NaOH (dư) → Na2CO3 + NH3 (G) + 2H2O
=> những khí tác dụng được với NaOH là: Cl2 (X), H2S (Y), SO2 (Z)
Câu 5. Khi làm thí nghiệm với H2SO4 đặc, nóng thường sinh ra khí SO2. Để hạn chế tốt nhất khí SO2 thoát ra gây ô nhiễm môi trường, người ta nút ống nghiệm bằng bông tẩm dung dịch nào sau đây:
A. cồn.
B. muối ăn.
C. xút.
D. giấm ăn
Để hạn chế khí SO2 bay ra, người ta sử dụng bông tẩm xút vì xút có khả năng phản ứng:
SO2 + 2NaOH → Na2SO3 + H2O
Câu 6. Dãy chất nào sau đây tác dụng được với Khí SO2
A. BaO, K2SO4, Ca(OH)2
B. KOH, CaO, H2O
C. Ca(OH)2, H2O, BaCl2
D. KCl, H2O, CaO
Câu 7. Hòa tan V lít khí SO2 (đktc) vào 100 ml dung dịch NaOH 1,2M thì thu được 10,02 gam hỗn hợp hai muối. Tìm giá trị của V
A. 2,016 lít.
B. 1,344 lít.
C. 0,672 lít.
D. 2,24 lít.
Câu 8. SO2 là một trong những khí gây ô nhiễm môi trường là do
A. SO2 là chất có mùi hắc, nặng hơn không khí.
B. SO2 vừa có tính khử, vừa có tính oxi hóa.
C. SO2 là khí độc, tan trong nước mưa tạo thành axit gây ra sự ăn mòn kim loại.
D. SO2 là một oxit axit mạnh
SO2 là một trong những khí gây ô nhiễm môi trường là do SO2 là khí độc, tan trong nước mưa tạo thành axit gây ra sự ăn mòn kim loại.
.................................
Trên đây VnDoc đã giới thiệu Na2SO3 + H2SO4 → Na2SO4 + SO2 + H2O thì. Để có kết quả học tập tốt và hiệu quả hơn, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Hóa học 10, Chuyên đề Vật Lý 10, Chuyên đề Hóa học 10, Giải bài tập Toán 10. Tài liệu học tập lớp 10 mà VnDoc tổng hợp biên soạn và đăng tải.
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu học tập THPT miễn phí trên Facebook, mời bạn đọc tham gia nhóm Tài liệu học tập lớp 10 để có thể cập nhật thêm nhiều tài liệu mới nhất.